что пить при гемангиоме печени у взрослых
Хирург «СМ-Клиника» рассказал о гемангиоме печени
Что такое гемангиома печени
Гемангиома (также известная как ангиома) печени – это доброкачественная опухоль, которая состоит из скоплений небольших сосудистых полостей, заполненных кровью.
Большинство гемангиом печени не вызывают симптомов, хотя более крупные образования, которые давят на ткани, могут стать причиной плохого аппетита, вызывать тошноту и рвоту.
Как правило, у пациента образуется всего одна гемангиома, но в некоторых случаях их может быть несколько. Гемангиомы не перерастают в рак и не распространяются на другие части тела.
Причины гемангиомы печени у взрослых
Почему в печени образуются гемангиома – достоверно неизвестно. Но отдельные исследования показывают, причиной могут быть определенные дефектные гены. Есть предположения, что роль в развитии опухоли могут сыграть:
Симптомы гемангиомы печени у взрослых
Большинство гемангиом печени не вызывают каких-либо неприятных симптомов, их обнаруживают, когда пациента осматривают по поводу другого заболевания.
Маленькие (от нескольких миллиметров до 2 см в диаметре) и средние (от 2 до 5 см) не лечат, но их следует регулярно контролировать. Такой мониторинг необходим, потому что около 10% гемангиом со временем увеличиваются в размерах по неизвестным причинам.
Гигантские гемангиомы печени (более 10 см) обычно имеют симптомы и осложнения, требующие лечения. Симптомы чаще всего включают боль в верхней части живота, поскольку большое образование давит на окружающую ткань и капсулу печени. Другие симптомы включают:
Лечение гемангиомы печени у взрослых
Диагностика
Есть ряд тестов, которые помогают отличить гемангиому печени от других типов опухолей:
Современные методы лечения
Лекарственных средств для лечения гемангиомы печени не существует. Для удаления опухоли может потребоваться операция – если она быстро растет или вызывает значительный дискомфорт или боль. Техника, называемая сосудистой эмболизацией, при которой перекрываются кровеносные сосуды, питающие гемангиому, может замедлить или обратить вспять ее рост.
Профилактика гемангиомы печени у взрослых в домашних условиях
Популярные вопросы и ответы
Какие могут быть осложнения при гемангиоме печени?
Когда нужна операция при гемангиоме печени?
В более сложной ситуации специалист подберет гормональную терапию, лучевую терапию или хирургическое вмешательство.
Можно ли лечить гемангиому печени народными средствами?
Народными средствами вылечить гемангиому нельзя. Лечение этой патологии индивидуально в каждом конкретном случае. Необходимо соблюдать диету, чтобы не спровоцировать ухудшение: исключить из рациона алкоголь, газированные напитки, шоколад, специи, хлеб, а также жирную и соленую пищу.
Эмболизация гемангиомы печени
В центре эндоваскулярной хирургии проводится терапия гемангиомы печени. Эмболизация сосудов позволяет остановить рост доброкачественной опухоли.
Основные особенности сосудистой доброкачественной опухоли печени
Гемангиома является одной из самых распространенных опухолей печени. Образование диагностируется примерно у 2 % жителей планеты. Как правило, опухоль развивается преимущественно у женщин в возрасте от 30 до 50 лет. Это связано с тем, что провоцируется рост образования женскими половыми гормонами.
Гемангиома является сосудистой опухолью. Она доброкачественна. Но это не значит, что образование не следует удалять! Гемангиомы могут стать причиной разрыва сосудов. В этом случае пациенту потребуется экстренная помощь врачей. Очень часто крупные образования сдавливают соседние органы. Также опухоль мешает нормальному кровоснабжению. В некоторых случаях возникает компрессия крупных стволов сосудов. В результате развивается сердечная недостаточность.
Существуют гемангиомы следующих типов:
Специалисты выделяют и еще одну опухоль печени. Ее называют атипичной. Встречается такое образование печени очень редко. Опухоль отличается нестандартной структурой. Ее сосудистые полости покрываются ороговевшей тканью.
Образование может быть как одиночным, так и множественным. Последний тип опухолей чаще становится причиной развития различных осложнений.
О наличии новообразования могут свидетельствовать следующие симптомы:
Как диагностируется опухоль?
Зачастую небольшие образования никак не проявляют себя. По этой причине диагностика затрудняется. Лишь при увеличении размеров опухоли врач может прощупать печень или даже сам опухолевый узел.
Специфических признаков наличия образования не покажут и общий, биохимический анализы крови. Тем не менее, специалист может определить увеличение показателей билирубина. Это свидетельствует о сдавливании желчных протоков. При разрастании гемангиомы повышается количество печеночных ферментов. При гигантских опухолях увеличивается СОЭ.
Наиболее информативным методом диагностики образования является УЗИ. При необходимости исследование дополняется контрастированием или доплером. Это повышает эффективность методики. В ходе исследования специалист обнаруживает образование с четкими границами. Для уточнения диагноза проводится КТ с контрастированием сосудов.
Максимально информативным методом диагностики образования является МРТ. Методика также может дополняться контрастированием. Благодаря МРТ можно определить не только локализацию опухоли, но и ее точные размеры. Также специалистам удается увидеть «дольчастость» строения образования и даже уровни жидкости в полостях сосудов.
В некоторых случаях дополнительно проводятся артериография, радиоизотопное исследование и биопсия.
Особенности лечения опухоли
Терапия не проводится при:
Терапия назначается при:
Консервативная терапия при опухолях представленного типа практически не проводится. Тем не менее, если обнаружить образование на начальных стадиях, можно попытаться остановить его рост с помощью гормональных препаратов. Для стабилизации давления в сосудах применяются и такие средства, как бета-блокаторы.
Для предотвращения разрастания образования могут назначаться:
Все эти методики пока не доказали высокой эффективности. Тем не менее, применяя их, вы можете упустить время.
Эффективным способом лечения является удаление образования.
До недавнего времени операции проводились с применением только двух методик:
В некоторых ситуациях традиционное удаление гемангиомы невозможно! В этом случае проводится эмболизация артерий, которые питают опухоль. Такое вмешательство осуществляется и при иных показаниях. Уточнить их может только опытный врач.
Эмболизация заключается во введении в сосуды опухоли специального раствора. Он буквально запаивает артерии гемангиомы. Благодаря этому образование уменьшается в размерах. В некоторых случаях эмболизационное вмешательство проводится как подготовительное перед хирургической операцией.
Особенности современной методики
Удаление гемангиомы путем эмболизации становится все более популярной методикой.
Наиболее опасным при резекции становится массивное кровотечение. Начаться оно может даже при случайных и небольших повреждениях печеночных или портальных стволов, а также внутрипеченочного отдела полой вены. Также кровотечение может начаться и из ветвей артерии. Современная методика позволяет устранить риски! В основе вмешательства лежит суперселективная катетеризация и селективное выключение из кровообращения отдельных ветвей печеночной артерии, которая обеспечивает кровью опухоль.
К достоинствам методики относят:
Мы рекомендуем эндоваскулярный метод лечения как малотравматичный и патогенетически оправданный.
Преимущества вмешательства в центре профессора Капранова
От чего зависит стоимость услуг
Диапазон цен и окончательная стоимость устранения образований печени зависят от многих внешних факторов (быстроты и удобства предоперационного обследования, комфортности и быстроты самой госпитализации и т. п.), не имеющих прямого отношения к лечебной деятельности. Даже при минимальных вложениях вы получаете полноценную профессиональную помощь.
Планируете приступить к лечению печени? Обращайтесь в наш центр! Вы всегда можете связаться с профессором Капрановым, воспользовавшись его личными телефонами:
Вы неспешно обсудите с врачом все особенности вмешательства, риски.
Также звоните в клиники, в которых работает Сергей Анатольевич. Администраторы расскажут вам о стоимости терапии гемангиомы, условиях пребывания в лечебном учреждении.
Некоторые гепатопротекторы в лечении заболеваний печени
В настоящее время отмечены большие успехи в развитии тех областей медицины, которые зависят от достижений в биологии, при почти полном отсутствии прогресса в областях, зависящих от прикладных дисциплин (сюда можно отнести и лечение болезней).
В настоящее время отмечены большие успехи в развитии тех областей медицины, которые зависят от достижений в биологии, при почти полном отсутствии прогресса в областях, зависящих от прикладных дисциплин (сюда можно отнести и лечение болезней). Особенно это заметно, если понаблюдать за пациентами, страдающими заболеваниями печени. Это связано с тем, что печень является органом, обеспечивающим энергетические и пластические потребности организма, а также в значительной степени выполняющим дезинтоксикационную функцию, то есть защиту организма от «экологической агрессии среды», в том числе и эндогенной, связанной с лечением многих заболеваний, так как метаболизм большинства лекарственных препаратов происходит в печени. Многие болезни печени, заканчивающиеся выздоровлением, оставляют «след» метаболического нарушения, который сохраняется на многие годы, и нередко переходит в болезнь, требующую лекарственной коррекции (примером может служить функциональная непрямая гипербилирубинемия, являющаяся следствием перенесенного острого вирусного гепатита).
На основании клинико-лабораторно-морфологических признаков можно выделить следующие виды повреждений печени:
Из вышеизложенного можно сделать следующий основной вывод: даже если острое повреждение печени не переходит в хронический процесс, а заканчивается выздоровлением, все равно «издержки» повреждения продолжают давать о себе знать той или иной степенью дистрофии, более высокой чувствительностью печени к повреждающим агентам, ферментной несостоятельностью, ведущей к функциональной неполноценности. Особенностью этой патологии является склонность к частым рецидивам, длительному течению, нарушающему трудоспособность, что переводит проблему из разряда медико-биологических в категорию медико-социальных. Этим обусловлено наличие в арсенале врача препаратов (средств) с протективным эффектом, восстанавливающих те или иные элементы нарушенной структуры, а также функции гепатоцита и гепатобилиарной системы в целом.
Гепатопротекторы (ГП) на сегодняшний день составляют 9,2% от общего количества лекарственных средств. В 1999 году группа ГП в России была представлена 31 торговым наименованием по 167 позициям. Все ГП можно разделить на три самостоятельные группы:
Группа гепатопротекторов растительного происхождения (в том числе гомеопатических) самая многочисленная и составляет 52% [9]. Это в значительной степени связано с большим спектром действия этой группы препаратов, доступностью их в ценовом отношении, минимальным количеством побочных эффектов. Одним из перспективных направлений в этом отношении является использование комплексных гомеопатических препаратов, содержащих малые дозы веществ растительного, минерального и животного происхождения. Таким образом, токсическое и аллергическое воздействие на организм человека при длительных терапевтических курсах практически исключено.
Наибольшую группу заболеваний составляют те, которые вызываются алкогольной болезнью печени (АБП). В последние годы решены принципиальные вопросы, касающиеся гепатотоксичности алкоголя. Известно, что около 85% этанола окисляется цитозольным ферментом алкогольдегидрогеназой (АДГ) желудка и печени до ацетальдегида. Ацетальдегид, в свою очередь, при помощи печеночного митохондриального фермента алкогольдегидрогеназы (АлДГ) подвергается дальнейшему окислению до ацетата через стадию ацетил — СоА.
Различия в скорости элиминации алкоголя в значительной степени обусловлены генетическим полиморфизмом ферментных систем.
10-15% этанола метаболизируются в микросомах гладкого эндоплазматического ретикулума микросомальной этанолокислительной системой (МЭОС), входящей в систему цитохром Р450 2Е1 и участвующей в метаболизме не только этанола, но и ряда лекарственных препаратов.
Значительную часть токсических эффектов этанола обусловливает ацетальдегид:
Наиболее тяжелый гепатотоксический эффект ацетальдегида — нарушение функции важнейшего структурного компонента клеточных мембран — фосфолипидов, что ведет к повышению проницаемости мембран, нарушению трансмембранного транспорта, нарушению функционирования клеточных рецепторов и мембраносвязанных ферментов.
Морфологическим субстратом АБП является жировая дистрофия (стеатоз печени), сначала во 2-й и 3-й зонах дольки, а затем и диффузно. При развернутой картине острого алкогольного гепатита гепатоциты находятся в стадии балонной и жировой дистрофии. В той или иной степени выражены фиброз с перисинусоидальным расположением коллагеновых волокон, лобулярная инфильтрация полиморфно-ядерными лейкоцитами с участками фокального некроза. При нарастании явлений фиброза формируется микронодулярный цирроз, нередко без признаков активного воспаления.
Лечение АБП комплексное. На всех этапах необходимо отказаться от дальнейшего употребления алкоголя. На ранних этапах в сочетании с полноценной диетой этого достаточно для полного обратного развития процесса и восстановления печени. В центре медикаментозной терапии на всех этапах и при всех формах АБП применяются препараты «эссенциальных» фосфолипидов (субстанции ЕРL), являющихся высокоочищенным экстрактом бобов сои. ЕРL как основной компонент клеточных мембран восстанавливает их целостность. Это приводит к нормализации функции мембран и повышению их текучести, активации мембранных ферментов и увеличению синтеза эндогенных фосфолипидов. Второй важный компонент ЕРL — торможение трансформации клеток Ито в коллагенпродуцирующие. Третий компонент действия EPL — уменьшение активности цитохрома Р450 2Е1, что приводит к обратному развитию жировой дистрофии; таким образом эссенциальные фосфолипиды воздействуют на большинство процессов, возникших вследствие повреждающего действия этанола при АБП. За многие годы существования эссенциальных фосфолипидов накоплен громадный опыт лечения ими. Довольно сложную задачу в клинической практике всегда представляет оценка эффективности лечения. «Метаболическими тестами» являются ферментные показатели, а степень жировой дистрофии — это критерий морфологический, который, по существу, применяется редко. Мы предложили использовать феномен «затухания» ультразвукового сигнала, который в данной ситуации, оцениваемый в динамике, дает представление об уменьшении степени жировой инфильтрации печени.
В проводимом нами исследовании принимали участие 50 больных жировой дистрофией печени, преимущественно алкогольной этиологии. Использованы препараты эссенциале форте Н у 30 больных и эссенциале Н у 20 больных (у 10 в течение 3 месяцев и у 10 в течение 6 месяцев, препарат получали в дозе 2 капсулы 3 раза в день). Показаны хорошая переносимость и высокая эффективность препарата. Больным жировой дистрофией достаточно 8-недельного курса лечения; при сформированном гепатите требуется более продолжительное лечение, при этом тенденция к нормализации показателей трансаминаз проявляется на протяжении 3-4 месяцев, а положительное воздействие на степень жировой дистрофии, по данным УЗИ, наблюдается при продолжительности лечения не менее 6 месяцев (даже при отсутствии динамики со стороны трансаминаз).
Конкурирующим препаратом в лечении АБП является гептрал, однако исследований, посвященных длительному (6 месяцев и более) лечению этим средством, практически нет, да и с экономической точки зрения такая терапия представляется менее выгодной.
Этиология и механизмы развития холестаза многофакторны. Так, гепатоцеллюлярный и каналикулярный холестазы могут быть обусловлены вирусным, алкогольным, лекарственным, токсическим поражениями, застойной сердечной недостаточностью, метаболическими нарушениями (доброкачественный возвратный внутрипеченочный холестаз, холестаз беременных, муковисцидоз,
a1-недостаточность и др.). В основе формирования клинических проявлений холестаза лежат три фактора: избыточное поступление элементов желчи в кровь; уменьшение или отсутствие желчи в кишечнике; воздействие компонентов желчи на печеночные клетки и канальцы. Лабораторная диагностика основывается на определении содержания в крови щелочной фосфатазы, ГГТП, общего билирубина и его фракций, холестерина и аминотрасфераз (уровень которых зависит не столько от холестаза, сколько от активности патологического процесса в печени, лежащего в основе холестаза). Из препаратов, воздействующих на определенные звенья патогенеза холестаза, в настоящее время наиболее широко используются гептрал (адеметионин) и урсодеоксихолевая кислота. Кроме того, начали появляться сообщения об использовании препарата силимар (фирма «Вилар»). Гептрал участвует в двух важных биохимических процессах клеток: трансметилировании и транссульфидировании. В результате нормализуется проницаемость клеточной мембраны и повышается активность Na+ — K+ — AТФ-азы (то есть увеличивается энергетический потенциал клетки).
Прием урсодеоксихолевой кислоты приводит к уменьшению в энтерогепатической циркуляции гидрофобных желчных кислот (тем самым предупреждается их токсическое воздействие на мембраны гепатоцитов и на эпителий желчных протоков), а также снижает аутоиммунность процесса (препараты урсофальк, урсосан и др.). Препараты применяются в дозе 10-15 мг/кг до разрешения холестаза, в дальнейшем показано длительное лечение в поддерживающих дозах. Средняя доза гептрала в сутки составляет 1600 мг; так как эффект дозозависим, в некоторых случаях мы назначали гептрал в дозе 3200 мг, которая переносится нормально.
Силимар — препарат очищенного сухого экстракта, получаемого из плодов расторопши пятнистой, содержащей флаволигнаны (силибин, силиданин и др.) и другие флавоноиды. Используют 1-2 таблетки по 100 мг на прием 3 раза в день курсом 30 дней; при недостаточном эффекте лечение может быть продолжено до двух-трех месяцев. Механизм действия — торможение индикаторных ферментов усиливает активность цитохромов, восстанавливает проницаемость клеточных мембран.
Из других печеночных протекторов следует отметить хофитол — экстракт свежих листьев артишока полевого. Хофитол кроме гепатопротективного и желчегонного действия обладает диуретическим эффектом и снижает содержание мочевины в крови. Хофитол оказывает метаболическое, мембраностабилизирующее и энергетическое воздействие. Наиболее эффективен хофитол в лечении больных с токсическими формами поражения, холестазом, с сочетанной сердечной патологией и застойной сердечной недостаточностью, а также с поражением почек.
Из отечественных препаратов в первую очередь следует выделить гепатосан — препарат, получаемый из печени животных в результате сублимационной сушки. Попадая в организм человека, клетка оживает и начинает работать как гепатоцит на уровне кишки. Этот эффект зарегистрирован в ходе изучения короткоцепочечных жирных кислот. Ростовые факторы, распавшиеся в кишечнике, всасываются и начинается действие препарата на уровне печеночной клетки. Гепатосан оказывает метаболическое, мембраностабилизирующее и повышающее энергетический объем воздействия. Максимально эффективно препарат действует у больных с патологией печени в стадии цирроза. У этой группы больных он должен использоваться продолжительно (наш опыт лечения охватывает период 12 месяцев), при этом уменьшается всасывание метаболитов толстокишечной микрофлоры и постепенно уменьшаются явления энцефалопатии.
В данной работе рассмотрены основные, максимально эффективные печеночные протекторы, которые влияют на основные виды расстройств функционирования печеночной клетки. Выбор препарата должен осуществляться в зависимости от ведущего клинического симптомокомплекса. Так, при АБП и нарушении целостности клеточной мембраны препаратом выбора должны быть эссенциальные фосфолипиды; при синдроме холестаза — гептрал, урсодеоксихолевая кислота и силимар; при токсическом, в том числе и лекарственном, повреждении — хофитол; при тех же расстройствах у больных в стадии цирроза печени — гепатосан. Естественно, всякий раз терапия носит комплексный, а лечение вышеназванными препаратами — базовый характер. Эти препараты создают основу терапии, а при наступлении ремиссии обеспечивают поддерживающее ее воздействие.
По вопросам литературы обращайтесь в редакцию
Современное лечение ГЕМАНГИОМ У ДЕТЕЙ
Гемангиомы у детей — наиболее часто встречающиеся доброкачественные сосудистые опухоли, которые составляют более 50% всех опухолей детского возраста [1, 4, 5, 9, 10, 11, 16]. В отношении морфологической принадлежности этих новообразований
Гемангиомы у детей — наиболее часто встречающиеся доброкачественные сосудистые опухоли, которые составляют более 50% всех опухолей детского возраста [1, 4, 5, 9, 10, 11, 16].
В отношении морфологической принадлежности этих новообразований можно с уверенностью сделать вывод об опухолевой, а не диспластической природе гемангиом [6, 13, 15].
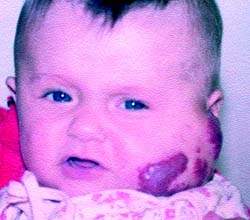 |
| Рисунок 1. Ребенок с ангиомой до лечения |
Многими авторами установлена высокая митотическая активность в клетках опухоли, в то же время отмечена возможность спонтанной регрессии гемангиом, что полностью соответствует опухолевой природе заболевания [6, 10, 14, 17].
Несмотря на свою доброкачественность, гемангиомы отличаются быстрым прогрессирующим ростом. Разрастаясь, они разрушают окружающие ткани и наносят ребенку значительный косметический ущерб. В первую очередь это относится к гемангиомам лица и головы. При локализации гемангиом на веках, ушной раковине, носу, а также на слизистой ротовой полости, помимо косметических проблем, могут возникать чисто физиологические в виде нарушений функций некоторых важных органов (зрение, слух, дыхание). Поэтому можно сказать, что гемангиомам присущи некоторые черты клинически злокачественного течения.
Особенностью течения гемангиом является непредсказуемость их “поведения”; порой небольшая, точечная гемангиома щеки в течение 2-3 недель может превратиться в обширную и глубокую ангиому сложной анатомической локализации (например, гемангиома околоушной области, без тенденции к остановке роста). Расчет на спонтанную регрессию в этих случаях оказывается неоправданным, а потеря времени идет явно не на пользу больному.
Помимо этого, сосудистые опухоли могут изъязвляться, вызывать кровотечения и инфицироваться. Характерная особенность изъязвившихся и нагноившихся гемангиом — продолжительное течение заболевания и отсутствие тенденции к быстрому заживлению язвенных поверхностей.
Отдельного разговора заслуживает спонтанная регрессия гемангиом. По нашим данным, спонтанной регрессии подвергаются около 7-8% простых гемангиом, находящихся на “закрытых” участках тела и только у доношенных детей в возрасте старше одного года. Кавернозные и комбинированные гемангиомы практически не регрессируют.
Надеяться на спонтанную регрессию большой и глубокой ангиомы в области лица у маленького недоношенного ребенка в возрасте до шести месяцев было бы ошибкой!
Процесс течения гемангиом достаточно сложный и требует постоянного внимания, причем чем меньше ребенок, тем внимательнее надо следить за состоянием гемангиомы. Особенно быстрый рост ангиом наблюдается в первое полугодие жизни ребенка, после этого рост замедляется, кроме гемангиом сложной анатомической локализации.
Поскольку в ранний возрастной период прогноз довольно сложен, лечение гемангиом, по нашему мнению, следует начинать как можно раньше, и даже недоношенность ребенка не является противопоказанием к раннему лечению.
Вероятно, универсального метода лечения гемангиом у детей нет и быть не может. И хотя морфологические данные явно свидетельствуют в пользу опухолевой природы ангиом, использование простых и эффективных хирургических и парахирургических методов лечения приводит к положительному результату.
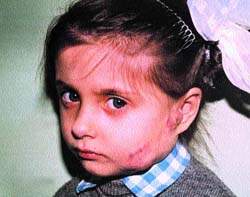 |
| Рисунок 2. После СВЧ-криогенного лечения |
Клиника детской хирургии РГМУ за 20 лет накопила опыт лечения 300 тыс. детей с гемангиомами различной локализации и вида.
Но занимаясь проблемой лечения гемангиом, мы столкнулись с группой больных с обширными и глубокими гемангиомами сложной анатомической локализации: лицо, околоушная область и шея.
Эти гемангиомы отличаются определенным своеобразием: бурным ростом опухоли, клинической злокачественностью течения, характеризующейся разным уровнем деструкции окружающих тканей, изъязвлениями, артериальными кровотечениями. Лечение таких гемангиом представляет значительные трудности для хирурга, так как традиционные методы чаще всего оказываются неэффективными.
Поэтому мы решили выделить этих больных в отдельную группу (см. табл.).
| Распределение детей с гемангиомами по виду и количеству последних | ||
| Вид ангиом | Количество больных | % |
| Простые | 215500 | 71,8 |
| Кавернозные | 19 500 | 6,6 |
| Комбинированные | 53000 | 17,7 |
| Смешанные | 10500 | 3,5 |
| Гемангиомы сложной анатомической локализации | 1500 | 0,5 |
| Всего | 300000 | 100 |
При анализе полученных данных подход к лечению детей с гемангиомами становится вполне очевиден. Наименьшую проблему представляют простые гемангиомы, наибольшую — гемангиомы сложной анатомической локализации, хотя в количественном отношении первые явно преобладают над последними.
Из ныне существующих методов наиболее удачным для лечения простых гемангиом является локальная криодеструкция аппаратом, где в качестве хладоагента применяется жидкий азот (с температурой –1960 С) [3, 8].
Криогенное лечение гемангиом проводится амбулаторно. Специальной подготовки ребенка к лечению не требуется. Метод прост, экономичен, не требует анестезии, абсолютно бескровен. Во время процедуры и после нее нарушений общего состояния ребенка, повышения температуры и патологических реакций не наблюдается.
Оптимальное время криовоздействия — 20-30 с для гемангиом, располагающихся на коже, и 7-15 с для гемангиом, локализующихся на слизистых оболочках.
При множественных гемангиомах, особенно если они были малых и средних размеров, мы проводили криодеструкцию одновременно двух или трех ангиом, но так, чтобы общая площадь криоповреждения не превышала 10 см2.
При локализации гемангиом в местах, наиболее подверженных травмированию, особенно в области промежности и ягодиц, площадь однократного криовоздействия не должна превышать 5 см2.
При крупных и обширных гемангиомах лечение должно проводиться в несколько этапов с интервалами между ними 10-14-21 день. За это время местная реакция в области криовоздействия стихает, и лечение может быть повторено.
Для предупреждения распространения опухолевого процесса и с целью ограничения роста гемангиомы рекомендуется начинать лечение с периферии.
Наиболее выраженный перифокальный отек наблюдается после криовоздействия на гемангиомы лица, век, сгибательных поверхностей, а также слизистой оболочки губ и половых органов. Образование сухой корочки отмечается на третий-четвертый день, эпителизации идет под струпом в течение 2-4 недель.
Успеха при криогенном лечении удается достичь в 100% случаев. Очень важной стороной лечения является получение хороших косметических и эстетических результатов (99,7%) благодаря особенностям регенерации кожи после криогенных вмешательств (органотипическая регенерация). Осложнения при криогенном лечении гемангиом наблюдаются крайне редко, в 0,2% случаев.
Среди общепринятых методик лечения наибольшей популярностью пользуется хирургическое иссечение опухоли с пластикой кожи или без нее.
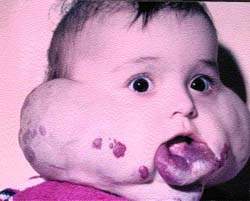 |
| Рисунок 3. Ребенок с двухсторонней ангиомой до лечения |
В 95% случаев клиника отказалась от традиционных хирургических методов лечения гемангиом, отдавая предпочтение эффективным консервативным способам. Причем за 20 лет частота оперативных вмешательств снизилась в 50 раз.
Хирургический способ наиболее целесообразен при локализации гемангиом на “закрытых” участках тела, тогда как при расположении опухолей в области лица и шеи иссечение представляет определенную косметическую проблему.
Оперативный метод лечения целесообразно также использовать при зрелых формах гемангиом, которые закончили свою дифференцировку. Операция в качестве корригирующего метода может быть использована при наличии избытка кожи на месте большой туберозной гемангиомы в случае ее полного спонтанного исчезновения.
Для лечения небольших кавернозных гемангиом лица и кончика носа с успехом применяется склерозирующая терапия. Она основана на принципе асептического воспаления или тромбирования сосудов, возникающих в гемангиоме в результате введения склерозирующих веществ.
 | 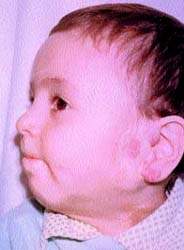 |
| Рисунок 4. Тот же ребенок после лечения (локальная гипертермия) | |
У всех больных для инъекций использовали 70%-ный спирт, отек на месте инъекции исчезал самостоятельно к 5 – 6 дню.
Недостатком инъекционного метода лечения является болезненность и длительность лечения, 76% больных потребовались дополнительные неоднократные инъекции спирта.
Диатермоэлектрокоагуляция применяется значительно реже, лишь при небольших точечных ангиомах, в тех случаях, когда опухоль располагается в областях, где нельзя воспользоваться другими методами лечения.
Эффективна, особенно в первом полугодии жизни ребенка, гормональная терапия гемангиом по альтернирующей схеме. Данный метод лечения был применен нами у 630 больных.
При подборе больных для кортикостероидной терапии мы руководствовались следующими критериями: сложность, т. е. критичность анатомической локализации; обширность поражения; быстрый рост гемангиом и поражение опухолью различных анатомических областей.
Мы считаем, что гормональной терапии подлежат самые обширные и самые сложные гемангиомы у детей.
Гормональное лечение проводилось преднизолоном по 4-6-8 мг на 1 кг веса ребенка. Суточная доза преднизолона в таблетках делилась на два приема: в 6 часов утра ребенок получал 2/3 дозы, в 9 часов утра 1/3 дозы. Препарат принимался через день без снижения дозировки. Продолжительность курса лечения составляла 28 дней.
Уже после второго или третьего приема преднизолона у большинства больных отмечались признаки регрессии ангиом, побледнение и некоторое уплощение опухоли. А к окончанию курса преднизолонотерапии все гемангиомы уменьшались в объеме, прекращался их рост и на поверхности опухоли появлялись белесоватые островки участков здоровой кожи, которые расчленяли ангиому на все меньшие и меньшие участки. После перерыва в 1-2 месяца, при необходимости, проводили повторные курсы гормонотерапии по той же методике.
Каких-либо осложнений во время лечения преднизолоном и после его отмены мы не наблюдали.
Гормонотерапия является довольно результативным методом лечения ангиом, однако при высокой его эффективности (98%) желаемого косметического результата достичь практически невозможно. Только у 2% детей ангиомы удалось полностью вылечить с помощью гормонотерапии, долечивание гемангиом другими методами позволяет решать лишь косметические проблемы.
Рентгенотерапия гемангиом относится к высокоэффективным методам. Она является весьма результативной, если лечение проводится у детей от 3 до 8 месяцев, так как в этом возрасте чувствительность ангиомной ткани к ионизирующему излучению очень высока, что обеспечивает излечение геманигиом с полным восстановлением нормальной кожи.
Близкофокусная рентгенотерапия применяется для лечения гемангиом таких областей, где другие методы невозможно использовать, например область орбиты, ретробульбарного пространства или простые гемангиомы большой площади.
Разовые очаговые дозы составляли от 0,8 до 1,6 Гр, в зависимости от возраста ребенка. Показанием к прекращению лучевой терапии при ангиомах являлось замедление роста и побледнение гемангиомы, т. е. лечение проводилось до появления симптомов регрессии, аналогичной естественной, после чего облучение прекращалось [7].
При лучевой терапии в дозах, не вызывающих местной реакции, изменения кожи и мягких тканей не развиваются. Надо учитывать, что этот метод лечения все же относительно сложен, и чтобы проявился эффект от лучевой терапии, требуется довольно длительное время.
При лечении кавернозных и комбинированных гемангиом с выраженной подкожной частью, чаще сложной анатомической локализации, следует проводить криоусиление за счет дестабилизации “связанной воды” путем предварительного СВЧ-воздействия на область замораживания. СВЧ-облучение проводится в физиотерапевтическом режиме в течение 3-5 минут, последующая криодеструкция выполняется в упомянутых выше режимах.
На наш взгляд, недоношенность не является противопоказанием к выполнению СВЧ-криодеструкции. В ряде случаев целесообразно проводить СВЧ-криогенное лечение по индивидуальным показаниям, например у новорожденных детей или в случае относительно большого объема опухоли.
Метод СВЧ-криодеструкции позволяет частично или полностью отказаться от хирургического лечения и добиться при этом хорошего результата (98%).
После обязательной ангиографии и эмболизации опухоли проводится лечение. Принимая во внимание преимущественную локализацию опухолей в проекции лицевого нерва, наиболее целесообразно было использовать СВЧ-криогенное вмешательство, так как этот способ гарантировал сохранность лицевого нерва, мимической мускулатуры и контуров лица ребенка.
Вмешательство не сопровождалось кровотечением и не было тяжелым для больного. В течение 5-6 месяцев гемангиома исчезала, оставляя после себя участки атрофированной кожи и атрофические рубцы.
К недостаткам этой методики мы отнесли развитие массивных отеков лица, которые держались до 5-7 дней, а затем исчезали самостоятельно, а также хоть и относительную, но все же хирургическую интервенцию.
На рис. 1, 2 представлен ребенок с ангиомой околоушной области до и после лечения (методом СВЧ-криодеструкции).
В последние годы исследуется и не без успеха применяется методика локальной СВЧ-гипертермии обширных и глубоких ангиом околоушной области. Данная методика была реализована у 180 больных. Метод заключается в повышении температуры в опухоли, регистрируемом введением под опухоль датчика в виде иглы. Температура доводится до 43-440С и поддерживается на этом уровне 5-6 минут.
Среди основных преимуществ методики основным является отказ от хирургического вмешательства, отсутствие отеков и возможность быстрой выписки ребенка домой. Косметические вмешательства, если ребенок в таковых будет нуждаться, можно выполнять в более старшем возрасте.
На рис. 3, 4 представлен ребенок с двухсторонней ангиомой сложной локализации до и после лечения (методом локальной гипертермии).
Таким образом, современное лечение гемангиом у детей и использование всего арсенала средств, имеющегося на вооружении в детской хирургии, позволяет добиться полного излечения опухоли с хорошим косметическим результатом. А следовательно, получить не только здорового, но и красивого ребенка!
Литература
1. Баиров Г. А. Хирургия пороков развития у детей. Л., 1968, с. 561-577.
2. Исаков Ю. Ф. Хирургические болезни у детей. М., 1993, с. 519-562.
3. Кандель Э. И. Криохирургия. М., 1974, с. 303.
4. Кондрашин Н. И. Клиника и лечение гемангиом у детей. М., 1963, с. 103.
5. Краковский Н. И., Таранович В. А. Гемангиомы. М., 1974, с. 168.
6. Лебкова Н. П., Кодрян А. А. О гистегенезе и механизме регрессии врожденных гемангиом кожи у детей // Архив патол., 1997, вып. 3. с. 44-50.
7. Свистунова Т. М. Низковольтная рентгенотерапия при гемангиомах у детей. Л., 1974, с. 142.
8. Ситковский Н. Б., Гераськин В. И., Шафранов В. В., Новак М. М. Лечение гемангиом у детей жидким азотом. Киев, 1968, с. 120.
9. Терновский С. Д. Хирургия детского возраста. М., 1959, с. 179-200.
10. Федореев Г. А. Гемангиомы. Л., 1974, с. 192.
11. Demuth R. J., Miller S. H., Keller F. Complications of embolization treatment for problem cavernous hemangiomas // Ann. Plast. Surg. 1984. V. 13. № 2. P. 135-144.
12. Edgerton M. T. Steroid therapy of haemangiomas // Symposium on Vascular Malformations and Melonotic Lesions. Ed. By Williams H. G. St. Louis, C. V. Mosby. 1983. P. 74-83.
13. Enjolras O., Herbretean F. Et al., Hemangiomes et Malformations vasculares superficielles: classification // J. Des Maladies Vasculaires. Paris. 1992. V. 17. № 1. P. 2-19.
14. Fingerhut A. Angiomas of the Smallintestine, Diagnostic and therapeutic problems // Gastroenterol. Clin. Biol. 1978. V. 2. № 12. P. 103-104.
15. Pasyk K. Classification and clinical and histopathological features of hemangiomas and other vascular malformations // Vascular Birthmarks. 1987. P. 1-54.
16. Peck J. E. The treatment of hemangiomas // British Med. J. 1974. V. 2. P. 198-200.
17. Traub E. F. Involution of Haemangiomas // Arch. Pediat. 1933. V. 50. P. 272-278.