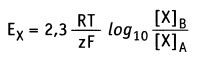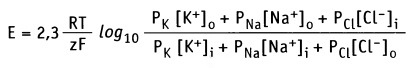Что такое электрохимический градиент
Что такое электрохимический градиент
• Мембранный потенциал возникает за счет электрохимического градиента, который существует по обеим сторонам мембраны, селективно проницаемой для ионов
• Величина мембранного потенциала как функции концентрации ионов рассчитывается по уравнению Нернста
• В клетке поддерживается отрицательное значение мембранного потенциала покоя. При этом внутренняя среда клетки, по сравнению с внешней, характеризуется несколько большим отрицательным зарядом
• Существование мембранного потенциала является необходимым условием генерации электрических сигналов, а также направленного транспорта ионов через мембрану
Важным свойством клеток является способность поддерживать такие внутриклеточные концентрации метаболитов, которые существенно отличаются от их содержания во внеклеточной среде. В случае ионов, различия в их концентрации по обеим сторонам мембраны приводят к различиям в электрическом заряде: внутриклеточная среда заряжена несколько более отрицательно, чем среда снаружи клетки. Совместное действие разности зарядов и концентраций проводит к возникновению электрохимического градиента. Электрохимический градиент поддерживается за счет действия селективных каналов и белков переносчиков в плазматической мембране.
Для того чтобы понять, каким образом возникает электрохимический градиент, вначале рассмотрим простой случай, когда мембрана оказывается проницаемой только для одного вида ионов. На рисунке ниже представлены два компартмента, А и В, разделенные тонкой мембраной. Эти компартменты содержат раствор КС1 разной концентрации. В растворе хлорид калия диссоциирован на гидратированные ионы К+ и Cl-. Поскольку оба компартмента содержат эквимолярные концентрации ионов, то каждый обладает нейтральным зарядом.
Если бы мембрана была непроницаема для ионов, то величина ее электрического потенциала, измеренная с помощью вольтметра, равнялась бы нулю.
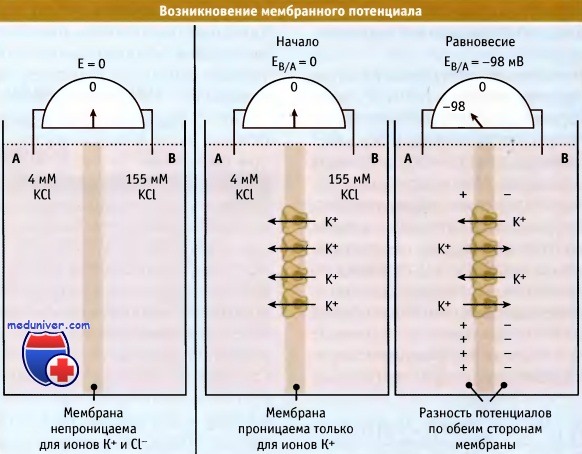
Теперь рассмотрим случай, когда мембрана проницаема только для ионов калия (например, когда в мембране находятся К+-каналы). Диффузия растворенных веществ по градиенту концентрации является энергетически выгодным процессом (выражается в виде отрицательной величины разности энергии AG). Поэтому ионы К+ будут диффундировать в сторону более низкой их концентрации, т. е. из компартмента В в компартмент А. При этом распределение заряда на мембране будет меняться. По мере накопления в компартменте А положительно заряженных ионов, возрастают силы отталкивания между ними. Эти силы затрудняют переход ионов К+ в компартмент А.
Когда в системе достигается электрохимическое равновесие, градиенты концентрации и электрических зарядов взаимно уравновешиваются, и движение ионов К+ через мембрану прекращается. При этом транспорт ионов К+ из одного компартмента сдерживается их транспортом из другого компартмента.
Однако в компартменте А содержится больше положительно заряженных ионов, чем в компартменте В. Этот избыток ионов К+ (в компартменте А) взаимодействует с избытком ионов Cl- (в компартменте В) через тонкую мембрану, в результате чего по обеим ее сторонам выстраиваются электрические заряды. Разница зарядов по обеим сторонам мембраны выражается в виде разности потенциалов и называется мембранный потенциал. Равновесный (мембранный) потенциал компартмента В по отношению к компартменту А имеет отрицательное значение.
Этот пример иллюстрирует необходимость наличия двух условий, необходимых для возникновения мембранного потенциала клетки, не равного нулю:
• различные концентрации ионов по обеим сторонам мембраны, которые приводят к разделению зарядов и
• мембрана, обладающая селективной проницаемостью по крайней мере к одному виду ионов.
Поэтому величина мембранного потенциала является функцией концентрации ионов. В состоянии равновесия эту функцию для ионов X можно выразить количественно с помощью уравнения Нернста:
В формировании мембранного потенциала в клетках животных, главным образом, участвуют ионы К+, Na+ и Cl-. Ионы Са2+ и Mg2+ в меньшей степени участвуют в формировании мембранного потенциала покоя. Плазматическая мембрана обладает селективной проницаемостью к перечисленным ионам (т. е. мембрана содержит ионные каналы, селективные к каждому типу ионов). Это обстоятельство, а также мембранная проницаемость (Р) для каждого иона учитывается в уравнении Гольдмана-Ходжкина-Каца, которое представляет собой расширенную форму уравнения Нернста.
Для основных ионов это уравнение выражает мембранный потенциал как функцию их проницаемости и концентрации внутри (i) и снаружи (о) клетки:
В отличие от большинства других К+-каналов, которым необходим сигнал для открытия, эти каналы в клетке, обладающей определенным потенциалом покоя, открыты постоянно. В покоящейся клетке также открыты несколько каналов для других ионов. Движение ионов К+ из клетки, по направлению электрохимического градиента, помогает клеточному содержимому поддерживать отрицательный заряд. Пока мы не знаем всех источников ионов калия, которые участвуют в этом процессе. В некоторых клетках, например у растений и бактерий, а также в митохондриях, мембранный потенциал покоя создается за счет градиента протонов, а не ионов К+.
Для того чтобы происходила диффузия ионов К+ из клетки через К+-каналы, их концентрация в клетке должна быть выше, чем в окружающей среде. Градиент концентрации создается в результате работы Na+/К+-АТФа-зы, которая закачивает в клетку два иона калия на каждые три иона натрия, которые этот ионный насос удаляет из клетки. Поэтому насос функционирует как генератор заряда: удаляется больше электрических зарядов, чем привносится к клетку. Таким образом, наряду с K+-каналами, лишенными воротного механизма, Na+/К+-АТФазы участвуют в создании отрицательного внутриклеточного потенциала. Если происходит инактивация Na+/K+-АТФаз, то концентрации ионов Na+ и К+ по обе стороны мембраны уравниваются. Это происходит потому, что липидный бислой очень плохо пропускает ионы. Иными словами, без прохождения первичных процессов активного транспорта с участием Na+/К+-АТФаз значение мембранного потенциала равнялось бы нулю.
Мембранный потенциал покоящейся клетки представляет собой довольно постоянную величину. Однако при связывании лигандов, механическом стрессе или при изменении электрического заряда происходит открытие специфических ионных каналов, и мембранный потенциал изменяется. Если ионные каналы находятся под контролем электрического заряда, то изменения мембранного потенциала влияют на прохождение через них ионов. Открытие и закрытие канала контролируются воротным механизмом (гейтингом). Мембранный потенциал зависит от тех ионов, для которых каналы в основном, открыты. Например, при открытии Na+- или Са2+-каналов происходит деполяризация мембраны.
С энергетической точки зрения, мембранный потенциал представляет собой некий энергетический резервуар, энергию которого можно использовать для выполнения определенной работы. По расположению отрицательно заряженных ионов в цитозоле и положительно заряженных на наружной стороне мембраны, клетка напоминает электрический конденсатор или батарею, т. е. приспособление, способное сохранять электрическую энергию и служить ее источником. Энергия высвобождается в виде ионов, мигрирующих по направлению их электрохимического градиента, и может использоваться в процессах транспорта других ионов или метаболитов против градиента концентрации.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
An электрохимический градиент это градиент из электрохимический потенциал, обычно для ион который может перемещаться по мембрана. Градиент состоит из двух частей: химического градиента или разницы в концентрация растворенного вещества через мембрану, и электрический градиент или разница в плата через мембрану. Когда есть неравные концентрации иона на проницаемой мембране, ион будет перемещаться через мембрану из области с более высокой концентрацией в область с более низкой концентрацией через простая диффузия. Ионы также несут электрический заряд, который образует электрический потенциал через мембрану. Если есть неравное распределение зарядов по мембране, то разница в электрических потенциалах создает силу, которая стимулирует диффузию ионов до тех пор, пока заряды не уравновесятся на обеих сторонах мембраны. [1]
Содержание
Обзор
Электрохимический потенциал важен в электроаналитическая химия и промышленные применения, такие как батареи и топливные элементы. Он представляет собой одну из многих взаимозаменяемых форм потенциальная энергия через которую энергия может быть консервированный.
В биологических процессах направление движения иона распространение или активный транспорт поперек мембраны определяется электрохимическим градиентом. В митохондрии и хлоропласты, протонные градиенты используются для генерации хемиосмотический потенциал это также известно как движущая сила протона. Эта потенциальная энергия используется для синтеза АТФ посредством окислительного фосфорилирования или фотофосфорилированиесоответственно. [2]
Электрохимический градиент состоит из двух компонентов. Во-первых, электрическая составляющая вызвана разностью зарядов на липидной мембране. Во-вторых, химический компонент вызван разной концентрацией ионы через мембрану. Комбинация этих двух факторов определяет термодинамически благоприятное направление движения иона через мембрану. [1] [3]
Электрохимический градиент аналогичен водному давление через гидроэлектростанция. Мембранные транспортные белки такой как натриево-калиевый насос внутри мембраны эквивалентны турбинам, которые преобразуют потенциальную энергию воды в другие формы физической или химической энергии, а ионы, которые проходят через мембрану, эквивалентны воде, которая попадает на дно плотины. Кроме того, энергию можно использовать для перекачки воды в озеро над плотиной. Аналогичным образом химическая энергия в клетках может использоваться для создания электрохимических градиентов. [4] [5]
Химия
Термин обычно применяется в контексте, в котором химическая реакция должен иметь место, например, один, связанный с переносом электрона на аккумулятор электрод. В аккумуляторе электрохимический потенциал, возникающий при движении ионов, уравновешивает энергию реакции электродов. Максимальное напряжение, которое может вызвать реакция батареи, иногда называют стандартный электрохимический потенциал этой реакции (см. также Электродный потенциал и Таблица стандартных электродных потенциалов). В случаях, относящихся конкретно к движению электрически заряженных растворенных веществ, потенциал часто выражается в единицах вольт. Увидеть: Концентрационная ячейка.
Биологический контекст
НАДН + 11 ч + (матрица) + 1/2 O2 → НАД + + 10 часов + (IMS) + H2О. [9]
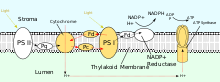
Подобно цепи переноса электронов, светозависимые реакции фотосинтеза перекачивают протоны в тилакоид просвет хлоропластов, чтобы управлять синтезом АТФ с помощью АТФ-синтазы. Протонный градиент может быть создан посредством нециклического или циклического фотофосфорилирования. Из белков, участвующих в нециклическом фотофосфорилировании, фотосистема II (PSII), пластихинон, и цитохром b6f комплекс непосредственно способствуют генерации протонного градиента. На каждые четыре фотона, поглощенные ФСII, в просвет перекачивается восемь протонов. [10] Общее уравнение для фотофосфорилирования:
2 НАДФ + + 6 часов + (строма) + 2 часа2O → 2 НАДФН + 8 Н + (люмен) + O2. [11]
Ионные градиенты
Δ г = р Т пер c я п c о ты т + z F V м е м б р а п е < displaystyle Delta G = RT ln < frac 
Концентрации клеточных ионов приведены в таблице ниже. X- представляет белки с чистым отрицательным зарядом.
Протонные градиенты
В частности, протонные градиенты важны для многих типов клеток как форма хранения энергии. Градиент обычно используется для управления АТФ-синтазой, жгутиковый ротация или транспортировка метаболиты. [23] В этом разделе мы сосредоточимся на трех процессах, которые помогают установить градиенты протонов в соответствующих клетках: бактериородопсин и нециклическое фотофосфорилирование и окислительное фосфорилирование.
Бактериородопсин
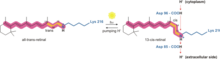
Как бактериородопсин генерирует протонный градиент в Археи проходит через протонный насос. Протонный насос полагается на переносчики протонов, чтобы отгонять протоны со стороны мембраны с низким H + концентрация в сторону мембраны с высоким H + концентрация. В бактериородопсине протонная помпа активируется за счет поглощения фотоны 568 нм длина волны что приводит к изомеризация из База Шиффа (SB) в сетчатка образуя K-состояние. Это отодвигает SB от Asp85 и Asp212, в результате чего H + переход от SB к Asp85, формирующий состояние M1. Затем белок переходит в состояние M2, отделяя Glu204 от Glu194, который высвобождает протон из Glu204 во внешнюю среду. SB это перепротонирован от Asp96, который формирует состояние N. Важно, чтобы второй протон происходил от Asp96, так как его депротонированный состояние нестабильно и быстро репротонируется протоном из цитозоль. Протонирование Asp85 и Asp96 вызывает повторную изомеризацию SB с образованием O-состояния. Наконец, бактериородопсин возвращается в состояние покоя, когда Asp85 высвобождает свой протон в Glu204. [23] [24]
Фотофосфорилирование
PSII также полагается на свет чтобы управлять образованием протонных градиентов в хлоропластах, однако PSII использует векторную окислительно-восстановительную химию для достижения этой цели. Вместо того, чтобы физически переносить протоны через белок, реакции, требующие связывания протонов, будут происходить на внеклеточной стороне, в то время как реакции, требующие высвобождения протонов, будут происходить на внутриклеточной стороне. Поглощение фотонов с длиной волны 680 нм используется для возбуждения двух электронов в п680 к более высокому уровень энергии. Эти электроны с более высокой энергией передаются связанному с белком пластохинону (PQА), а затем к несвязанному пластохинону (PQB). Это восстанавливает пластохинон (PQ) до пластохинола (PQH2), который высвобождается из ФСII после получения двух протонов из стромы. Электроны в P680 пополняются за счет окисления воды сквозь кислород-выделяющий комплекс (OEC). Это приводит к выпуску O2 и H + в просвет. [23] Показана суммарная реакция:
После выхода из PSII, PQH2 едет к цитохрому b6f, который затем переносит два электрона от PQH2 к пластоцианин в двух отдельных реакциях. Происходящий процесс аналогичен Q-циклу в комплексе III цепи переноса электронов. В первой реакции PQH2 связывается с комплексом на стороне просвета, и один электрон переносится на железно-серный центр который затем передает его цитохром f который затем переводит его в пластоцианин. Второй электрон переходит в гем бL который затем передает его гему bЧАС который затем передает его в PQ. Во второй реакции второй PQH2 окисляется, добавляя электрон к другому пластоцианину и PQ. Обе реакции вместе переносят четыре протона в просвет. [25] [26]
Окислительного фосфорилирования
В цепи переноса электронов Комплекс I (CI) катализирует то сокращение из убихинон (UQ) в убихинол (UQH2) передачей двух электроны от сокращенного никотинамид аденин динуклеотид (НАДН), который переносит четыре протона из митохондриального матрикса в IMS: [27]
НАДН + ЧАС + + UQ + 4 ЧАС + ⏟ м а т р я Икс ⟶ НАД + + UQH 2 + 4 ЧАС + ⏟ я M S < displaystyle < ce 
Комплекс III (CIII) катализирует Q-цикл. Первый шаг, связанный с переносом двух электронов из UQH2 восстанавливается ХИ до двух молекул окисленного цитохром с на Qо сайт. На втором этапе еще два электрона восстанавливают UQ до UQH.2 на Qя сайт. [27] Показана суммарная реакция:
2 c y т о c час р о м е c ⏟ о Икс я d я z е d + UQH 2 + 2 ЧАС + ⏟ м а т р я Икс ⟶ 2 c y т о c час р о м е c ⏟ р е d ты c е d + UQ + 4 ЧАС + ⏟ я M S < Displaystyle 2 underbrace < mathrm <цитохром c>> _ < mathrm <окисленный>> + < ce 
Комплекс IV (CIV) катализирует перенос двух электронов от цитохрома с, восстановленного с помощью CIII, до половины полного кислорода. Использование одного полного кислорода в окислительном фосфорилировании требует передачи четырех электронов. Затем кислород потребляет четыре протона из матрицы для образования воды, в то время как еще четыре протона закачиваются в IMS. [27] Показана суммарная реакция:
Электрохимический градиент
Электрохимический градиент или градиент электрохимического потенциала, сочетание концентрационного градиента и мембранных потенциалов, которая определяет направление движения ионов через мембрану. состоит из двух компонентов: химического вещества, градиент или разница в концентрации растворенного вещества по обе стороны мембраны, и электрический градиент или разница, расположены на противоположных сторонах мембраны. градиент возникает из-за неодинаковой концентрации ионов по разные стороны проницаемой мембраны. ионы перемещаются через мембрану из области высокой концентрации в область с более низкой концентрации путем простой диффузии. ионы несут электрический заряд, который формирует электрический потенциал на мембране. если есть неравномерное распределение зарядов по обе стороны мембраны, разность электрических потенциалов порождает силу, что приводит к ионной диффузии, в то время как сборы по обе стороны не сбалансированы.
2. Химия. (Chemistry)
Термин «электрохимический потенциал» обычно применяется в тех случаях, когда нужно вызвать химическую реакцию, например, перенос электрона в электрическом батареи. В аккумуляторах электрохимический потенциал, возникающий от движения ионов уравновешивает реакцию энергетической электродов. максимальное напряжение, которое может произвести реакцию батарея, называют стандартный электрохимический потенциал этой реакции. вместе с макроэргических соединений, химическая энергия может храниться в биологических мембранах, которые функционируют как конденсаторы, которые выступают в качестве изолирующего слоя для ионов.
5. Протонных градиентов. (Proton gradients)
Протонные градиенты важны как форма хранения энергии в различных типах клеток. обычно градиент, используемый для АТФ-синтазы, вращение жгутика, или перенос метаболитов через мембраны. Этот раздел будет посвящен трем процессы, которые помогают установить протонных градиентов в соответствующих ячейках: бактериородопсин, не циклическое фотофосфорилирование и окислительного фосфорилирования.
An электрохимический градиент это градиент из электрохимический потенциал, обычно для ион который может перемещаться по мембрана. Градиент состоит из двух частей: химического градиента или разницы в концентрация растворенного вещества через мембрану, и электрический градиент или разница в плата через мембрану. Когда есть неравные концентрации иона на проницаемой мембране, ион будет перемещаться через мембрану из области с более высокой концентрацией в область с более низкой концентрацией через простая диффузия. Ионы также несут электрический заряд, который образует электрический потенциал через мембрану. Если есть неравное распределение зарядов по мембране, то разница в электрических потенциалах создает силу, которая стимулирует диффузию ионов до тех пор, пока заряды не уравновесятся на обеих сторонах мембраны. [1]
Содержание
Обзор
Электрохимический потенциал важен в электроаналитическая химия и промышленные применения, такие как батареи и топливные элементы. Он представляет собой одну из многих взаимозаменяемых форм потенциальная энергия через которую энергия может быть консервированный.
В биологических процессах направление движения иона распространение или активный транспорт поперек мембраны определяется электрохимическим градиентом. В митохондрии и хлоропласты, протонные градиенты используются для генерации хемиосмотический потенциал это также известно как движущая сила протона. Эта потенциальная энергия используется для синтеза АТФ посредством окислительного фосфорилирования или фотофосфорилированиесоответственно. [2]
Электрохимический градиент состоит из двух компонентов. Во-первых, электрическая составляющая вызвана разностью зарядов на липидной мембране. Во-вторых, химический компонент вызван разной концентрацией ионы через мембрану. Комбинация этих двух факторов определяет термодинамически благоприятное направление движения иона через мембрану. [1] [3]
Электрохимический градиент аналогичен водному давление через гидроэлектростанция. Мембранные транспортные белки такой как натриево-калиевый насос внутри мембраны эквивалентны турбинам, которые преобразуют потенциальную энергию воды в другие формы физической или химической энергии, а ионы, которые проходят через мембрану, эквивалентны воде, которая попадает на дно плотины. Кроме того, энергию можно использовать для перекачки воды в озеро над плотиной. Аналогичным образом химическая энергия в клетках может использоваться для создания электрохимических градиентов. [4] [5]
Химия
Термин обычно применяется в контексте, в котором химическая реакция должен иметь место, например, один, связанный с переносом электрона на аккумулятор электрод. В аккумуляторе электрохимический потенциал, возникающий при движении ионов, уравновешивает энергию реакции электродов. Максимальное напряжение, которое может вызвать реакция батареи, иногда называют стандартный электрохимический потенциал этой реакции (см. также Электродный потенциал и Таблица стандартных электродных потенциалов). В случаях, относящихся конкретно к движению электрически заряженных растворенных веществ, потенциал часто выражается в единицах вольт. Увидеть: Концентрационная ячейка.
Биологический контекст
НАДН + 11 ч + (матрица) + 1/2 O2 → НАД + + 10 часов + (IMS) + H2О. [9]
Подобно цепи переноса электронов, светозависимые реакции фотосинтеза перекачивают протоны в тилакоид просвет хлоропластов, чтобы управлять синтезом АТФ с помощью АТФ-синтазы. Протонный градиент может быть создан посредством нециклического или циклического фотофосфорилирования. Из белков, участвующих в нециклическом фотофосфорилировании, фотосистема II (PSII), пластихинон, и цитохром b6f комплекс непосредственно способствуют генерации протонного градиента. На каждые четыре фотона, поглощенные ФСII, в просвет перекачивается восемь протонов. [10] Общее уравнение для фотофосфорилирования:
2 НАДФ + + 6 часов + (строма) + 2 часа2O → 2 НАДФН + 8 Н + (люмен) + O2. [11]
Ионные градиенты
Δ г = р Т пер c я п c о ты т + z F V м е м б р а п е < displaystyle Delta G = RT ln < frac 
Концентрации клеточных ионов приведены в таблице ниже. X- представляет белки с чистым отрицательным зарядом.
Протонные градиенты
В частности, протонные градиенты важны для многих типов клеток как форма хранения энергии. Градиент обычно используется для управления АТФ-синтазой, жгутиковый ротация или транспортировка метаболиты. [23] В этом разделе мы сосредоточимся на трех процессах, которые помогают установить градиенты протонов в соответствующих клетках: бактериородопсин и нециклическое фотофосфорилирование и окислительное фосфорилирование.
Бактериородопсин
Как бактериородопсин генерирует протонный градиент в Археи проходит через протонный насос. Протонный насос полагается на переносчики протонов, чтобы отгонять протоны со стороны мембраны с низким H + концентрация в сторону мембраны с высоким H + концентрация. В бактериородопсине протонная помпа активируется за счет поглощения фотоны 568 нм длина волны что приводит к изомеризация из База Шиффа (SB) в сетчатка образуя K-состояние. Это отодвигает SB от Asp85 и Asp212, в результате чего H + переход от SB к Asp85, формирующий состояние M1. Затем белок переходит в состояние M2, отделяя Glu204 от Glu194, который высвобождает протон из Glu204 во внешнюю среду. SB это перепротонирован от Asp96, который формирует состояние N. Важно, чтобы второй протон происходил от Asp96, так как его депротонированный состояние нестабильно и быстро репротонируется протоном из цитозоль. Протонирование Asp85 и Asp96 вызывает повторную изомеризацию SB с образованием O-состояния. Наконец, бактериородопсин возвращается в состояние покоя, когда Asp85 высвобождает свой протон в Glu204. [23] [24]
Фотофосфорилирование
PSII также полагается на свет чтобы управлять образованием протонных градиентов в хлоропластах, однако PSII использует векторную окислительно-восстановительную химию для достижения этой цели. Вместо того, чтобы физически переносить протоны через белок, реакции, требующие связывания протонов, будут происходить на внеклеточной стороне, в то время как реакции, требующие высвобождения протонов, будут происходить на внутриклеточной стороне. Поглощение фотонов с длиной волны 680 нм используется для возбуждения двух электронов в п680 к более высокому уровень энергии. Эти электроны с более высокой энергией передаются связанному с белком пластохинону (PQА), а затем к несвязанному пластохинону (PQB). Это восстанавливает пластохинон (PQ) до пластохинола (PQH2), который высвобождается из ФСII после получения двух протонов из стромы. Электроны в P680 пополняются за счет окисления воды сквозь кислород-выделяющий комплекс (OEC). Это приводит к выпуску O2 и H + в просвет. [23] Показана суммарная реакция:
После выхода из PSII, PQH2 едет к цитохрому b6f, который затем переносит два электрона от PQH2 к пластоцианин в двух отдельных реакциях. Происходящий процесс аналогичен Q-циклу в комплексе III цепи переноса электронов. В первой реакции PQH2 связывается с комплексом на стороне просвета, и один электрон переносится на железно-серный центр который затем передает его цитохром f который затем переводит его в пластоцианин. Второй электрон переходит в гем бL который затем передает его гему bЧАС который затем передает его в PQ. Во второй реакции второй PQH2 окисляется, добавляя электрон к другому пластоцианину и PQ. Обе реакции вместе переносят четыре протона в просвет. [25] [26]
Окислительного фосфорилирования
В цепи переноса электронов Комплекс I (CI) катализирует то сокращение из убихинон (UQ) в убихинол (UQH2) передачей двух электроны от сокращенного никотинамид аденин динуклеотид (НАДН), который переносит четыре протона из митохондриального матрикса в IMS: [27]
НАДН + ЧАС + + UQ + 4 ЧАС + ⏟ м а т р я Икс ⟶ НАД + + UQH 2 + 4 ЧАС + ⏟ я M S < displaystyle < ce 
Комплекс III (CIII) катализирует Q-цикл. Первый шаг, связанный с переносом двух электронов из UQH2 восстанавливается ХИ до двух молекул окисленного цитохром с на Qо сайт. На втором этапе еще два электрона восстанавливают UQ до UQH.2 на Qя сайт. [27] Показана суммарная реакция:
2 c y т о c час р о м е c ⏟ о Икс я d я z е d + UQH 2 + 2 ЧАС + ⏟ м а т р я Икс ⟶ 2 c y т о c час р о м е c ⏟ р е d ты c е d + UQ + 4 ЧАС + ⏟ я M S < Displaystyle 2 underbrace < mathrm <цитохром c>> _ < mathrm <окисленный>> + < ce 
Комплекс IV (CIV) катализирует перенос двух электронов от цитохрома с, восстановленного с помощью CIII, до половины полного кислорода. Использование одного полного кислорода в окислительном фосфорилировании требует передачи четырех электронов. Затем кислород потребляет четыре протона из матрицы для образования воды, в то время как еще четыре протона закачиваются в IMS. [27] Показана суммарная реакция: