Что такое электрокардиостимуляция чреспищеводная
Чреспищеводная кардиостимуляция
1. Общие сведения
Электрокардиостимуляция (ЭКС) – проведение к сердечной мышце дополнительных, внешних электрических импульсов. Как известно, ритмичная сократительная деятельность миокарда управляется и контролируется в организме биоэлектрическим способом, что дало возможность разработать ряд широко известных диагностических, терапевтических и реанимационных методов, построенных именно на электрофизиологических принципах.
Современные высокотехнологичные электрокардиостимуляторы, имплантируемые внутрь и рассчитанные на длительную автоматическую работу, оснащены микропроцессорным контроллером, который регистрирует основные показатели электрической активности сердца и подключает дополнительные стимулирующие разряды лишь в случае такой необходимости.
Чреспищеводная электрокардиостимуляция – одна из неинвазивных модификаций метода ЭКС, которая применяется как в диагностических целях, так и для купирования некоторых опасных состояний.
2. Суть метода
После предварительного обследования (включающего, разумеется, стандартную ЭКГ), в пищевод натощак вводится тонкий гибкий зонд, выполняющий одновременно функции электрода. При этом пациент обычно лежит на спине с запрокинутой головой; реже зонд вводится в положении сидя. Как правило, для внедрения зонда в пищевод используют носовой ход, предварительно убедившись в отсутствии полипов, выраженного искривления носовой перегородки и других возможных анатомических препятствий – в подобных случаях доступ может быть осуществлен через полость рта. Применяется лидокаиновое орошение для предотвращения дискомфортных ощущений и подавления возможного рвотного рефлекса. В большинстве случаев естественное глотательное движение позволяет легко и безболезненно подвести зонд-электрод на максимальное сближение с миокардом.
3. Показания
ЧПЭКС как диагностическая процедура применяется для выявления некоторых патологических феноменов, недоступных регистрации обычным электрокардиографом с чрескожными электродами: аритмий, тахикардий, нарушений в проводящей системе сердца, латентной патологии коронарных артерий и т.п. В определенных диагностически сложных ситуациях показана также электростимуляционная провокация.
Терапевтическое значение чреспищеводной электрокардиостимуляции заключается в купировании приступов наджелудочковой тахикардии и трепетания предсердий.
4. Противопоказания
Чреспищеводная электрокардиостимуляция не проводится при наличии подтвержденных заболеваний пищевода, включая новообразования, стриктуры (сужения с ограниченной проходимостью), воспалительные процессы (эзофагиты) и др. К противопоказаниям относится также ряд кардиологических заболеваний, в том числе атриовентрикулярная блокада выраженной степени, инфаркт, тромбоз, аневризмы, а также присутствие имплантированных искусственных клапанов. Наконец, ЧПЭКС противопоказана при респираторной или иной острой инфекции.
Чреспищеводное электрофизиологическое исследование сердца (ЧПЭФИ)
2-е кардиологическое отделение
Электрофизиологическое исследование (ЭФИ) сердца — это метод диагностики нарушений ритма и проводимости сердца. Во время исследования производится стимуляция различных отделов сердца для выявления возможных нарушений ритма. Главным преимуществом ЭФИ перед электрокардиографией или суточным мониторированием ЭКГ является возможность выявления нарушений ритма и проводимости, которые невозможно было обнаружить первыми двумя способами.
При ЭФИ нагрузка на сердце тоже возрастает, но не вследствие физической активности, а в результате электрической стимуляции миокарда. Такая стимуляция проводится с помощью электродов, которые начинают подавать к сердечной мышце электротоки физиологической мощности, но с высокой частотой. В итоге миокард сокращается быстрее, возникает спровоцированное учащение сердцебиения. А при высокой частоте сердечных сокращений возникают либо аритмия, либо ишемия, если у человека уже имеются патологические процессы в миокарде, являющиеся предпосылками к развитию этих заболеваний. Другими словами, ЭФИ позволяет спровоцировать искомые заболевания и зарегистрировать их на ЭКГ с целью дальнейшего лечения пациента
Существует два вида электрофизиологического исследования сердца: инвазивное (эндокардиальное, эпикардиальное, комбинированное) и неинвазивное (ЧПЭФИ).
Чреспищеводное ЭФИ (ЧПЭФИ). Электроды подводятся с помощью зонда, вводимого в просвет пищевода. Является неинвазивной методикой, а по технике напоминает обычную фиброгастроскопию.
ЧПЭФИ проводится чаще, так как имеет наименьшее число осложнений и побочных эффектов, если сравнивать с инвазивными методами.
Чреспищеводное электрофизиологическое исследование сердца осуществляется по следующим показаниям:
Возможности чреспищеводной электрокардиостимуляции в купировании трепетания предсердий (Трансляция из Новосибирска).
Оксана Михайловна Драпкина, профессор, доктор медицинских наук:
– Нас сейчас ждет подключение из Новосибирска. Здравствуйте, Алексей Николаевич. Профессор Туров Алексей Николаевич. Возможности чреспищеводной электрокардиостимуляции в купировании трепетания предсердий.
Алексей Николаевич Туров, доцент, доктор медицинских наук:
– Добрый день. Действительно мое сообщение будет посвящено такой очень узкой профессиональной технологии. Эта технология выполняется в основном аритмологом, а не кардиологом. Но я считаю, что каждый врач должен знать, когда направить пациента на проведение этой процедуры.
Я хотел бы начать с того, что трепетание предсердий – это все-таки не фибрилляция предсердий. Фибрилляция предсердий это множество хаотично циркулирующих RE-ENTRY, тогда как трепетание предсердий – это боле простая, более упорядоченная аритмия, это один круг RE-ENTRY, одна волна RE-ENTRY, которая циркулирует по строго анатомически определенному пути. Чаще всего этот путь проходит в правом предсердии, а значит она по механизму является моно RE-ENTRY, то есть напоминает механизм простых суправентрикулярных тахикардий, таких как синдром ВПВ, АВ-тахикардия, а значит она может купироваться также путем электрокардиостимуляции.
И здесь необходимо обратиться к анатомии и обратить внимание на то, что анатомия пищевода создает очень большие перспективы. Пищевод проходит по задней стенке левого предсердия, тесно соприкасаясь с ней. И это создает замечательные условия для того, чтобы проведя электрод в пищевод, мы могли проводить таким образом стимуляцию именно задней стенки левого предсердия.
И в этом сообщении я хотел бы обобщить наш собственный опыт. Это порядка 10 тысяч пациентов, которым на протяжении 16-ти лет была проведена процедура чреспищеводной стимуляции при трепетании предсердий. Возраст пациентов был от 12 до 85 лет, длительность эпизода трепетания от двух часов и до девяти месяцев. И подавляющее большинство этих пациентов (85%) были с компенсированной гемодинамикой, имели стабильную циркуляцию.
Поскольку наша клиника является кардиохирургической, то большинство пациентов (66%) были пациентами, которые перенесли кардиохирургическую операцию, и трепетание у них возникло в раннем послеоперационном периоде, то есть это были стационарные пациенты. Но примерно треть пациентов были амбулаторными, которые в нашу клинику пришли самостоятельно и имели приступ трепетания с относительно стабильной гемодинамикой.
Хочу подчеркнуть, что нанесение одиночного экстрастимула было неэффективным для купирования трепетаний. У этого пациента мы видим, что нанесение одного экстрастимула многократно не приводило к устранению трепетания предсердий, а нанесение единственного залпа частой стимуляции сразу же привело к восстановлению синусового ритма.
Поэтому мы в настоящее время проводим следующий протокол. Электрод чреспищеводно позиционируется в том месте, где имеется максимальный вольтаж предсердных потенциалов, и наносятся именно залпы частой стимуляции, начиная с частоты предсердных потенциалов и плюс 30 в минуту. Для чего используется именно такая частота? Для того чтобы подавить трепетание, естественно, мы должны использовать овердрайв, то есть частоту большую, чем частота трепетания. Но если мы увеличим частоту на 15-20 ударов, то это приведет к акселерации, ускорению тахикардии. Если мы будем использовать частоту больше 320 в минуту, то это приведет к переводу трепетания в фибрилляцию предсердий. И поэтому используется частота, которая соответствует вот этому белому диапазону, то есть частота, которая и может восстановить синусовый ритм у этих пациентов.
При наличии критериев вхождения происходит увеличение частоты и длительности залпа. Если такие критерии вхождения отсутствуют, то меняется положение электрода, увеличивается межполюсное расстояние, изменяется амплитуда и длительность импульса. Что же это за критерии вхождения, которые мы ищем? Это появление неритмичности комплекса QRS либо во время залпа, либо сразу после залпа частой стимуляции. Это изменение цикла трепетания предсердий после залпа либо появление кратковременного эпизода фибрилляции предсердий.
Здесь мы видим, что во время стимуляции трепетание предсердий становится неритмированным, то есть изменяется расстояние между интервалами во время залпа стимуляции. На этом слайде мы видим, что такое изменение происходит после залпа стимуляции. На этом примере мы видим, что после стимуляции происходит кратковременное изменение цикла трепетания предсердий. У этого пациента мы видим, что после залпа стимуляции возникает короткий эпизод фибрилляции предсердий.
Все эти критерии говорят о том, что стимуляция эффективно захватывает предсердный миокард, то есть это является предвестником купирования трепетания предсердий. И существует два варианта развития событий: либо это купирование восстановить синусовый ритм, как мы видим на примере этого пациента; либо в результате нанесения залпа стимуляции трепетание предсердий трансформируется в фибрилляцию предсердий. В нашем опыте лишь менее чем у 1% больных трепетание предсердий сохранилось в результате чреспищеводной стимуляции. У 44% больных произошло восстановление синусового ритма, у 55% трепетание было трансформировано в фибрилляцию предсердий. Но обратите внимание, что это только непосредственные результаты, то есть на момент окончания стимуляции.
Давайте посмотрим, что произошло дальше с пациентами, которые получили фибрилляцию предсердий. У 10% этих больных синусовый ритм восстановился в течение нескольких минут. Мы видим пример такой ситуации, когда трепетание предсердий было переведено в фибрилляцию, а она уже спонтанно перешла в синусовый ритм менее чем за одну минуту. У 8% больных синусовый ритм восстановился самостоятельно в течение нескольких часов после этой процедуры. Еще у 13% больных синусовый ритм восстановился в течение нескольких дней после этой процедуры на фоне антиаритмической терапии. И еще у 10% больных фибрилляция вновь перешла в трепетание предсердий, и оно опять же было купировано чреспищеводной стимуляцией.
Если мы посмотрим на окончательный итог, через несколько дней после процедуры чреспищеводной стимуляции, то у 81% больных мы имели совершенно физиологический синусовый ритм.
Эта процедура эффективна при любом виде трепетания предсердий. Это связано с тем, что если циркуляция происходит в левом предсердии, это левопредсердное трепетание, то, нанося залпы частой стимуляции, мы создаем участок абсолютной рефрактерности предсердной стенки, и волна циркуляции разбивается об этот участок. Если это трепетание правопредсердное, то, создавая определенный очаг фокусной стимуляции в левом предсердии, мы создаем волну возбуждения, которая сталкивается с правопредсердной волной в области межпредсердной перегородки, и таким образом трепетание в любом случае купируется.
Давайте посмотрим на эту категорию пациентов. Это очень небольшое количество больных, у которых трепетание предсердий сохранялось вопреки этой процедуре. Что это были за пациенты? Они укладываются всего лишь в эти три формы. Это пациенты, которые имели определенные изменения в задней стенке левого предсердия. Либо это воспаление постаблационное, то есть пациенты недавно перенесли катетерную абляцию фибрилляции предсердий. Либо это рубцовая деформация задней стенки в результате многократных предшествующих катетерных абляций или многократных атриотомий кардиохирургических, либо это синдром изолированной задней стенки левого предсердия, который бывает при ортотопической трансплантации в том случае, если задняя стенка изолирована катетерным способом или хирургическим способом для лечения фибрилляции предсердий.
Мы видим пример такой ситуации. Это пациент после трансплантации сердца. Мы видим на кардиограмме трепетание предсердий, а чреспищеводная электрограмма показывает спонтанный автоматизм с частотой примерно 30 в минуту, который исходит из задней стенки левого предсердия.
На этой кардиограмме мы видим по поверхностной ЭКГ трепетание предсердий, а на электрограмме мы видим, что задняя стенка находится в состоянии фибрилляции предсердий. Это пациент после хирургической процедуры «Лабиринт».
И вот как выглядит изолированная задняя стенка после катетерной абляции фибрилляции предсердий. Если мы проведем чреспищеводный электрод, то через такую заднюю стенку левого предсердия мы, естественно, купировать трепетание предсердий не сможем.
Существует большое заблуждение некоторых врачей о том, что трепетание является более злокачественной формой аритмии, чем фибрилляция предсердий, и необходимо всеми способами перевести трепетание в фибрилляцию предсердий. Действительно, при трепетании предсердий частота сердечных сокращений обычно более частая и труднее медикаментозно достичь нормоформы. Но это не абсолютное правило. И на примере этого пациента, который имел трепетание предсердий с частотой 80 ударов в минуту, мы видим, что после чреспищеводной стимуляции, когда мы получили фибрилляцию предсердий, она как раз протекала с большей частотой сердечных сокращений, чем трепетание предсердий.
Но тем не менее антикоагулянты по современным рекомендациям назначаются по одним и тем же правилам и при трепетании, и при фибрилляции предсердий. Однако риск тромбоза при трепетании значительно меньше, потому что предсердие все же активно сокращается. Обратите внимание, что катетерная абляция в очень большом проценте случаев не просто лечит трепетание, а излечивает его. То есть трепетание предсердий является более благоприятной аритмией в плане излечения у пациента. И поэтому перевод трепетания предсердий в фибрилляцию предсердий – более злокачественную, более хаотичную аритмию фактически лишает пациента дальнейшей надежды на излечение вот этого заболевания.
Поэтому, когда мы проводим эту процедуру, мы не стремимся восстановить синусовый ритм, а не перевести трепетание в фибрилляцию, но такой исход бывает. И мы для этого оценили такую шкалу, которую назвали DALHAFOC. Это шкала, которая позволяет прогнозировать вероятность возникновения фибрилляции предсердий при чреспищеводной стимуляции. Каждая буква этой шкалы отражает определенный фактор. D – это длительность трепетания более десяти дней. Age – это возраст старше 70 лет. L – это дилатация левого предсердия более 60 миллиметров. Затем сердечная недостаточность застойная или низкая фракция выброса (H). AF – это фибрилляция предсердий в анамнезе. О – это перенесенная операция кардиохирургическая, торакальная или катетерная радиочастотная абляция. И С – это цикл трепетаний предсердий менее 220 миллисекунд. На каждый из этих факторов приходится 10% риска, и лишь на два фактора – фибрилляцию и операцию приходится 20% риска.
Таким образом, если мы видим такого пациента – 72 лет, у которого уже в течение 15 дней имеется приступ трепетания предсердий, и он возник сразу после протезирования митрального клапана, а до операции у пациента была фибрилляция предсердий, то мы оцениваем четыре фактора риска, видим, что в сумме они составляют 60%. То есть у этого пациента кране высока вероятность, что при чреспищеводной стимуляции мы восстановим не синусовый ритм, а трепетание перейдет в фибрилляцию предсердий, поэтому такую процедуру проводить ему нежелательно, лучше ему проводить электрическую кардиоверсию.
Мы оценили эффективность антиаритмической терапии и чреспищеводной стимуляции к исходу 48-ми часов от начала приступа. И мы видим, что антиаритмическая терапия помогла восстановить ритм у 37% пациентов с трепетанием предсердий, а чреспищеводная стимуляция к концу вторых суток восстановила синусовый ритм у 79% больных.
Если сравнивать чреспищеводную стимуляцию с ее ближайшим родственником, тоже электрической процедурой – это электроимпульсная терапия или электрическая кардиоверсия, то, безусловно, второй метод является более эффективным в восстановлении ритма, требуется одинаковая антикоагулянтная подготовка. Но чреспищеводная стимуляция проводится амбулаторно, она может проводиться в поликлинических условиях, для этого не нужен анестезиолог, пациент находится в лечебном учреждении фактически не более чем полчаса, а сама процедура занимает лишь две-три минуты. И фактор стоимости имеет большое значение, поскольку чреспищеводная стимуляция это фактически труд одного врача.
Какие противопоказания к этой процедуре? Это декомпенсированная сердечная деятельность, кардиогенный шок. Это тромбоз левого предсердия или некорректная антикоагулянтная подготовка. Это затяжное трепетание более трех месяцев. Если у пациента имеются данные о том, что у него возможно имеется дисфункция синусового узла. И если пациент готовится к катетрной абляции, и у него в анамнезе имеется и атриотомия или катетерная абляция фибрилляции предсердий, то есть мы предполагаем, что это трепетание является инцизионным, то есть происходит совершенно по атипичной траектории, то крайне желательно, чтобы пациент попал на операционный стол именно в состоянии трепетания предсердий, чтобы хирург мог откартировать эту нетипичную траекторию. То есть крайне нежелательно именно у таких пациентов трепетание предсердий купировать, если они готовятся к катетерной абляции.
И, наконец, какое место занимает тот или иной подход в купировании трепетания предсердий. Безусловно, антиаритмическая терапия является первой линией в лечении трепетания предсердий. Электроимпульсную терапию нужно проводить, если приступ является гемодинамическим и стабильным. Если трепетание затяжное, продолжается более трех месяцев, если пациент имеет большой риск в последующей фибрилляции по шкале DALHAFOC. И чреспищеводная стимуляция проводится в качестве одной из первых мер, если трепетание возникло в специализированном кардиологическом стационаре, которое имеет соответствующее оборудование, если имеются уже данные о том, что чреспищеводная стимуляция помогала этому пациенту ранее во время предыдущих приступов, и если антиаритмическая терапия не помогла восстановить ритм в течение первых суток от начала приступа. Тогда вторые сутки должны быть посвящены проведению именно чреспищеводной стимуляции. Спасибо за внимание.
Чреспищеводная электрокардиостимуляция
Чреспищеводная электрокардиостимуляция – неинвазивная процедура, направленная на получение записи биологических потенциалов с внешней поверхности сердца, используя при этом специальный пищеводный электроды и регистрационную аппаратуру.
Проведение специальных видов стимуляции для изучения электрофизиологических свойств проводящей системы, миокарда предсердий и желудочков. Выявление субстратов аритмии, их локализации и электрофизиологических характеристик. Контроль лекарственной и/или нефармакологической терапии.
Ненвазивное электрофизиологическое исследование сердца (ЧПЭФИ)
Опыт применения ЧПЭС в кардиологии насчитывает более 30 лет.
В нашей стране первое сообщение о применении ЧПЭС у больных с ишемической болезнью сердца появилось в научной медицинской литературе более 10 лет назад.
За этот период времени отношение к любому методу исследования уже носит устойчивый характер, а возможности самого метода хорошо изучены.
Следует сказать, что отношение кардиологов к методу ЧПЭС в течение этого времени менялось в зависимости от развития самой кардиологии и технических возможностей применяемых стимуляторов.
Повышенный интерес к этому методу в настоящее время обусловлен с одной стороны, бурным развитием самой кардиологии, как науки, в частности ее аритмологии, а также появлением современных стимуляторов с хорошими техническими характеристиками, позволяющими производить исследование с минимальными неприятными ощущениями для больного.
Применение ЧПЭФИ помогает решить три основные задачи: диагностика, лечение (терапевтическое, подбор антиаритмических препаратов) и прогнозирование во многих клинических ситуациях.
Скачать руководство по ЧПЭС. «Основы клинической чреспищеводной электростимуляции сердца» А.Н.Толстов
Скачать руководство по ЧПЭС. » Неинвазивное электрофизиологическое исследование при аномалиях проводящей системы сердца» Ю.В.Шубик
Область применения ЧПЭС в кардиологии
У больных ишемической болезнью сердца:
1) диагностика коронарной недостаточности;
2) определение степени (функционального класса) коронарной недостаточности,
3) диагностика безболевой ишемии миокарда;
4) выделение группы больных с ишемической болезнью сердца (ИБС), имеющих высокий риск внезапной сердечной смерти;
5) подбор оптимальной эффективной дозы антиангинального препарата и наиболее рационального приема его в течение суток;
6) выделение группы больных, которым наиболее целесообразно проведение коронароангиографии и последующего оперативного лечения ИБС;
7) верификация крупноочаговых рубцовых изменений миокарда у больных с синдромом WPW;
8) одновременная регистрация эхокардиограммы по программе стресс ЭхоКГ при проведении дозированной частотной нагрузки при ЧПЭС позволяет диагности¬ровать скрытые формы коронарной и миокардиальной недостаточности.
У больных с нарушениями ритма сердца:
1) оценка функции синусового узла:
— диагностика синдрома слабости синусового узла (СССУ);
— диагностика функциональной дисфункции синусового узла (чаще всего связанной с повышенной активностью п.Vagus)
— оценка функционального состояния миокарда перед установкой постоянного эндокардиального кардиостимулятора;
2) оценка функции атриовентрикулярного (AB) узла;
3) дифференциальная диагностика пароксизмальных суправентрикулярных тахиаритмий с помощью метода провокации тахиаритмий и последующей регистрацией пищеводной электрограммы (ПЭ);
4) диагностика и изучение электрофизиологических свойств дополнительных, аномальных путей проведения (пучок Кента и пучок Джеймса);
— диагностика синдрома преждевременного возбуждения желудочков в случае функционирования п. Кента или п. Джеймса;
— диагностика пароксизмальных тахиаритмий при синдроме Вольфа-Паркинсона-Уайта (ВПУ) или Клерка-Леви-Кристеску (CLC), Лауна-Ганонга-Левина (LGL);
— выделение группы больных синдромом ВПУ и мерцательной аритмии угрожаемых по развитию фибрилляции желудочков;
5) подбор оптимальной эффективной дозы противоаритмического препарата:
— для купирования пароксизма тахиаритмии;
— для профилактики возникновения пароксизма тахиаритмии;
— выявление аритмогенного эффекта препарата;
6) купирование пароксизмальных суправентрикулярных тахиаритмий (кроме мерцательной аритмии);
7) поддержание необходимой частоты сердечного ритма (ЧСС) во время проведения операции в случае исходной брадикардии;
8] изучение электрофизиологических свойств суправентрикулярной зоны: предсердий, АВ-узла, дополнительных путей проведения (рефрактерные периоды структур);
9) регистрация тахизависимой экстрасистолии и внутрижелудочковых блокад;
ЧПЭС имеет широкий спектр применения от амбулаторно-поликлинических, до стационарных подразделений. Метод для клиницистов в их клинической деятельности наиболее доступен и менее обременителен для больного.
Диагностические возможности ЧпЭФИ ограничиваются стимуляцией левого предсердия. В ряде случаев, может быть достигнута стимуляция левого желудочка, но для этого необходимо подавать напряжение с амплитудой 30-60 В (мА), что практически невозможно без применения наркоза.
Применение ЧПЭС при нарушениях ритма сердца
Применение ЧПЭС при нарушениях ритма сердца было обосновано в результате быстрого развития аритмологии и исходя из ее проблем.
Применение ЧПЭС у этой категории больных решило многие проблемы суправентрикулярных аритмий и полноценно заменило собой такой метод исследования как внутрисердечное электрофизиологическое исследование (ЭФИ).
Поэтому, показания для ЭФИ в настоящее время сужены и могут быть определены следующими состояниями:
1 Уточнение диагноза и подбор терапии у бальных с желудочковыми тахикардиями.
2. Синкопальные состояния, неясной этиологии.
3. Перед проведением хирургического лечения аритмий.
4. Перед имплантацией кардиостимулятора или кардиовертера-дефибриллятора больным с тахиаритмиями.
5. Для проведения криодеструкции аномальных путей проведения в случае их правостороннего прохождения.
6. Больные с синдромом WPW и пароксизмальной мерцательной аритмией, протекающей с потерей сознания и угрозой трансформации в фибрилляцию желудочков.
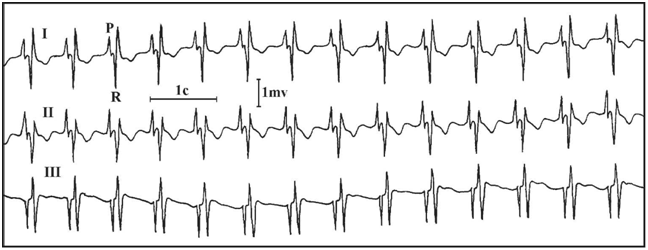
Рис. Чреспищеводная электрограмма, биполярная запись
Начиная исследование по программе нарушения ритма с помощью метода ЧПЭС, врач, проводящий его, должен быть уверен что все подготовлено на случай проведения реанимационных мероприятий: дефибриллятор подготовлен и включен, есть необходимый набор реанимационных лекарств и средств.
Кроме того, врач проводящий исследование, должен быть хорошо подготовлен по таким дисциплинам как клиническая кардиология с аритмологией, клиническая электрокардиография, знать электрофизиологию миокарда, вопросы неотложной кардиологии и реанимации.
ЧПЭС может проводится с диагностической и лечебной целью. В случае диагностического исследования должны отменяться все противоаритмические препараты.
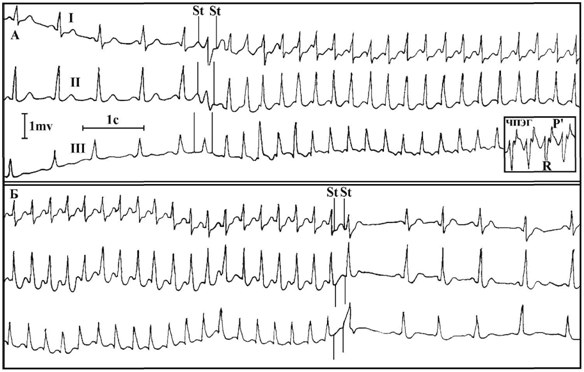
Рис.
А. Парной стимуляцией предсердий вызван пароксизм АВ реципрокной ортодромной тахикардии. RP’-интервал на ЧПЭГ меньше 1/2 RR-интервала и = 120 мс.
Б. Купирование пароксизма парной стимуляцией.
Оценка коронарного кровообращения методом ЧПЭС
Данная программа стимуляции является той основой с чего вообще начался метод ЧПЭС, как один из нагрузочных тестов (нагрузка ритмом) в кардиологии.
Применение программы стимуляции позволяет постепенно и дозированно увеличивать частоту сокращений желудочков с постоянной оценкой изменений конечной части желудочкового комплекса по монитору и при записи ЭКГ.
Применение ЧПЭС с целью оценки коронарного кровообращения позволяет кардиологу решать ряд важных задач:
1. устанавливать сам факт наличия у больного ишемической болезни сердца (ИБС) и ее форм, в частности, определять безболевую ишемию миокарда;
2. определять степень коронарной недостаточности;
3. определять оптимально эффективную дозу антиангинального препарата и кратность его приема;
4. выделять группу больных ИБС с тяжелой коронарной недостаточностью, которым настоятельно рекомендуется проведение коронароангиографии и возможным оперативным лечением ИБС;
5. определять прогноз и тактику ведения больных ИБС, после перенесенного инфаркта миокарда;
6. выделять группу больных ИБС, имеющих высокий риск внезапной сердечной смерти с целью проведения профилактического лечения;
7. проводить дифференциальную диагностику постинфарктного кардиосклероза у больных с синдромом Вольфа-Паркинсона-Уайта;
8. выявление скрытых форм нарушений ритма и проводимости;
9. при динамическом проведении ЧПЭС у одного и того же больного ИБС косвенно судить о скорости прогрессирования коронарного атеросклероза и эффективности проводимого лечения.
Кроме противопоказаний общего характера, проведение ЧПЭС по программе оценки коронарного кровообращения нецелесообразно в следующих случаях:
1. при наличии стойкой полной блокады левой ножки пучка Гиса;
2. при регистрации на ЭКГ-покоя явного (манифестирующего) синдрома преждевременного возбуждения желудочков, обусловленного функционированием пучка Кента;
3. у больного ИБС с 3 4 функциональным классом;
4. у больного с впервые возникшей стенокардией в течение первых 4-х недель и у больного с нестабильной стенокардией;
5. в течение первых 3-х недель неосложненного инфаркта миокарда;
6. при выраженной гипертрофии миокарда левого желудочка с вторичными изменениями конечной части желудочкового комплекса на ЭКГ.
ЧПЭС проводится по назначению лечащего врача через 2 часа после еды на фоне отмены коронароактивных препаратов в случае диагностического исследования. При этом необходимо согласие больного на проведение ЧПЭС, регистрация ЭКГ-покоя и эхокардиограммы (ЭхоКГ).
Программа стимуляции с целью оценки коронарного кровообращения довольно проста. После получения устойчивого ритма кардиостимулятора, превышающего собственную частоту ритма сердца на 20 имп./мин., проводят непрерывную ступенчатую стимуляцию. Длительность каждой ступени 1 минута.
При отсутствии изменений р конце ступени частоту стимуляции повышают на 10-20 имп./мин. до достижения максимальной частоты 160 имп/мин. По истечении каждой ступени стимуляции проводят оценку коронарного кровообращения по изменениям сегмента ST на ЭКГ.
Если после достижения максимальной частоты (160 имп./мин.) ишемических изменений на ЭКГ не наблюдается, то время стимуляции продлевается до 2 минут, после чего проводится окончательная оценка проведенного исследования. Считается нецелесообразным проводить оценку коронарного кровообращения при частоте стимуляции более 160 имп./мин., т.к. при этом значительно возрастает количество ложноположительных результатов, что отчасти связано с так называемым постдеполяризационным синдромом.
Постдеполяризационный синдром выражается в возникновении на ЭКГ депрессии сегмента ST и инверсии зубца «Т» после прекращения высокой частоты желудочков. Хорошо известно развитие этого синдрома после купирования пароксизма желудочковой тахикардии.
При отсутствии у больного верифицированной ИБС данный синдром свидетельствует о нарушениях процессов реполяризации желудочков не связанное с ухудшением коронарного кровообращения.
Осложнения при проведении ЧПЭС
Следует сразу оговориться, что пароксизмальные нарушения ритма, которые прежде рассматривались как осложнение метода ЧПЭС в настоящее время таковыми не являются.
Связано это с быстрым развитием аритмологии и изменением представлений. Однако, при этом необходимо иметь в виду, что врач, проводящий исследо¬вание, может столкнуться с двумя проблемами:
1. при проведении ЧПЭС врач сознательно пытается спровоцировать пароксизм суправентрикулярной тахиаритмии, используя различные режимы стимуляции, т. е. индукция тахикардии является целью самого исследования. Вряд ли эту ситуацию следует рассматривать как осложнение метода;
2. при проведении ЧПЭС, индукция тахикардии является неожиданностью для врача, проводящего исследование и возникает впервые в жизни больного. Пароксизм тахикардии может возникнуть при использовании любого режима стимуляции. В данной ситуации вопрос решается не однозначно, а в зависимости от конкретной формы пароксизма.
Сам факт возможности провокации тахикардии говорит о том, что в сердце больного сформировались все необходимые предпосылки для реализации механизма повторного входа и нужен лишь пусковой механизм для возникновения тахикардии.
Следует учитывать и конкретную форму спровоцированного пароксизма, исходя из сложности лечения и возможных осложнений данного пароксизма. Так, пароксизм узловой АВ-тахикардии или пароксизм реципрокной АВ-тахикардии у больного с синдромом WPW (ортодромный или антидромный вариант) достаточно легко купируются С помощью метода ЧПЭС и как правило не требуют внутривенного введения лекарств (не надо забывать и о возможности купировать данные пароксизмы с помощью вагусных проб).
Индукция впервые в жизни больного пароксизма мерцательной аритмии требует в дальнейшем применения лекарственных препаратов для ее купирования, т. к. метод ЧПЭС не купирует мерцательную аритмию.
Провокация у больного впервые в жизни мерцательной аритмии зачастую свидетельствует либо о критической дилатации предсердий, либо о выраженных дистрофических изменениях в миокарде предсердий [после перенесенного миокардита или хронической алкогольной интоксикации) после чего сохранение синусового ритма становится сложновыполнимой задачей.
1. Введение пищеводного электрода в трахею, вместо пищевода.
Это осложнение обычно случается у врачей, которые только начинают самостоятельно проводить исследование ЧПЭС и связано как правило с их торопливостью при введении зонда в пищевод. Это осложнение крайне редко возникает при неторопливом введении зонда в момент проглатывания слюны, когда происходит подъем надгортанника и закрытие трахеи.
Для избежания подобных случаев необходимо обращать внимание на крайне низкую амплитуду зубца «Р» на пищеводной электрограмме в начале исследования, а также появление кашля при включении стимуляции.
2. Ощущение жжения в области пищевода, за грудиной.
Появление этих ощущений обязательно при включении стимуляции, а их отсутствие у больного должно быть связано с неисправностью аппаратуры. Степень ощущений больного обычно невысокая или легко переносимая. При выраженных ощущениях и отказе больного от исследования, исследование прекращают.
3. При проведении стимуляции больной ощущает боли в области спины, связанные С сокращением позвоночных мышц. При выраженных болях исследование прекращают.
4. При включении стимулятора происходит эффективная стимуляция диафрагмы, что сопровождается ритмичными ее сокращениями с той частотой, которую в данный момент времени дает стимулятор. Больной при этом ощущает частую икоту или одышку, а врач, проводящий исследование наблюдает частое сокращение диафрагмы, которое исчезает сразу же после выключения стимулятора.
Наиболее часто это осложнение встречается у больных гиперстенического телосложения или с ожирением, т. к, расположение сердца в грудной клетке у таких больных таково, что сердце практически лежит на высоко расположенной диафрагме и полюса пищеводного электрода при ЧПЭС расположены в непосредственной близости не только к предсердиям, но и к диафрагме. Как правило, исследование при появлении этого осложнения прекращается.
Противопоказания к проведению ЧПЭС
1) постоянная форма мерцательной аритмии;
2) АВ-блокада 2-3 степени;
3) пороки сердца с выраженным нарушением внутрисердечной (по данным ЭхоКГ) и центральной гемодинамики (клиническая картина сердечной недостаточности выше 2 стадии или выше 2-го функционального класса);
4) дилатация полостей сердца;
5) аневризма сердца;
6) острая стадия любого заболевания (кроме пароксизма суправентрикулярной тахикардии и трепетания предсердий);
7) заболевания пищевода: опухоль, дивертикулез, стриктуры, ахалазия, эзофагит в стадии обострения, варикозное расширение вен;
8) артериальная гипертензия выше 220/120 мм.рт.ст. вне криза и обострения;
9) опухоли сердца (миксомы);
10) перикардит.
Кроме того, проведение ЧПЭС по программе ИБС нецелесообразно в следующих случаях:
1) при наличии стойкой полной блокады левой ножки пучка Гиса;
2) при регистрации явного [манифестирующего] синдрома WPW;
3) при нестабильной стенокардии в течение 4-х недель с момента установления диагноза;
4) в течение первых 3-х недель неосложненного инфаркта миокарда;
5) при стенокардии напряжения 3-4 функционального класса;
6) при выраженной гипертрофии миокарда левого желудочка с вторичными изменениями конечной части комплекса QRS-T на ЭКГ