Что такое окклюзия правой вса
Что такое окклюзия правой вса
Цереброваскулярные заболевания, являясь одной из основных причин смертности и стойкой утраты трудоспособности, представляют собой одну из наиболее актуальных проблем неврологии и сосудистой хирургии. процессы в ветвях дуги аорты практически в половине случаев инициируют ишемическое поражение головного мозга.
Окклюзии общей сонной артерии при проходимой внутренней сонной артерии сопровождаются неврологической симптоматикой в 1–5% случаев. В данной статье представлено клиническое наблюдение пациента с окклюзией левой ОСА, которому выполнена петлевая эндартерэктомия петлей из общей сонной артерии с последующим стентированием с хорошим клиническим эффектом.
Цереброваскулярные заболевания, являясь одной из основных причин смертности и стойкой утраты трудоспособности, представляют собой одну из наиболее актуальных проблем неврологии и сосудистой хирургии. процессы в ветвях дуги аорты практически в половине случаев инициируют ишемическое поражение головного мозга.
Окклюзии общей сонной артерии при проходимой внутренней сонной артерии сопровождаются неврологической симптоматикой в 1–5% случаев. В данной статье представлено клиническое наблюдение пациента с окклюзией левой ОСА, которому выполнена петлевая эндартерэктомия петлей из общей сонной артерии с последующим стентированием с хорошим клиническим эффектом.
Цереброваскулярные заболевания, являясь одной из основных причин смертности и стойкой утраты трудоспособности, представляют собой одну из наиболее актуальных проблем неврологии и сосудистой хирургии. процессы в ветвях дуги аорты практически в половине случаев инициируют ишемическое поражение головного мозга.
Окклюзии общей сонной артерии при проходимой внутренней сонной артерии сопровождается неврологической симптоматикой в 1–5% случаев [7]. Пусковым механизмом в развитии неврологической симптоматики может явиться как микроэмболия, так и гемодинамические расстройства. Статистические исследования, посвященные реконструкциям ОСА, невелики по количеству наблюдений. Основным методом коррекции окклюзии ОСА является шунтирования или трансторакальные реконструкции.
Первую операцию шунтирования при окклюзии общей и внутренней сонных артерий выполнили Lyons C. и Galbraith G. в 1957 году [4]. До настоящего времени данная операция чаще всего используется при поражениях общих сонных артерий (ОСА) [2, 5, 6, 8, 9, 10]. Альтернативой этим операциям является прямая энартерэктомия (ЭАЭ) или полузакрытая эндартерэктомия из ОСА. Aguiar [1] описал три случая полузакрытой ЭАЭ из ОСА с помощью Моля с хорошим непосредственным и отдаленным хорошим результатом. Отдаленные результаты прослежены через восемь месяцев, четыре и семь лет. У одного пациента отмечается асимтомный рестеноз 60%. Laszlo Pinter [3] описал один случай ЭАЭ с помощью Моля из правой ОСА с последующим стентированием ОСА. Ретроградная полузакрытая эндартерэктомии может сопровождаться такими осложненимяи, как диссекция и перфорация артерии, поэтому должна выполняться хирургами, имеющими опыт ЭАЭ петлей на других сосудистых бассейнах. Представлено клиническое наблюдение больного с окклюзией левой ОСА с проходимой ВСА и НСА, которому выполнена гибридная операция.
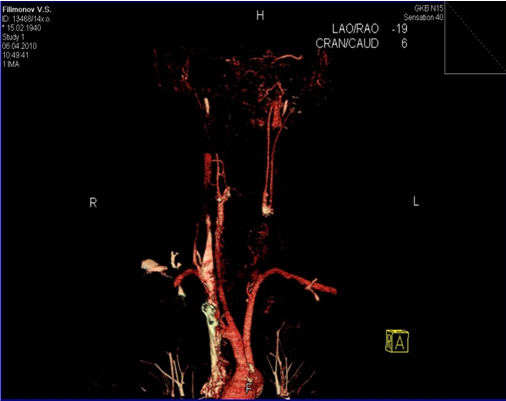
В отделении сосудистой хирургии в апреле 2010 года наблюдался пациент Ф., 70 лет с диагнозом: атеросклероз брахиоцефальных артерий и артерий нижних конечностей; окклюзия левой ОСА, стеноз правой ВСА 60%, левой ВСА 78%; хроническая ишемия головного мозга; ТИА в системе левой СМА; стеноз обеих наружных подвздошных артерий; ХИНК 2 Б степени. Поступал с жалобами на онемение и слабость в правой верхней конечности, проходящие самостоятельно, головокружение, потеря сознания. Жалобы беспокоят в течение года с частотой один раз в неделю. В неврологическом осмотре транзиторные ишемические атаки в системе левой СМА, появляющиеся в виде онемения в правой руке. По данным дуплексного сканирования брахиоцефальных артерий, в ампуле правой ОСА с переходом на устье ВСА гетерогенная циркулярная пролонгированная с кальцинозом бляшка, стеноз 60%. Левая ОСА окклюзирована. В левой ВСА гетерогенная пролонгированная циркулярная бляшка, стеноз 78%. Обе позвоночные артерии извиты до входа в канал. В обеих подключичных артериях гетерогенные бляшки, стеноз 50%. При ТКДГ: интракраниальный стеноз обеих ВСА. Функционирующий глазничный анастомоз слева из правой НСА. Коллатеральное кровообращение в бассейне левой ВСА из контрлатеральной ВСА. По данным МСКТ: окклюзия левой ОСА с ретроградным заполнением внутренней сонной артерии (рис. 1). Пациент имеет тяжелую сопутствующую патологию: ИБС, артериальная гипертензия, хронический бронхит. года выполнена операция — эндартерэктомия из левой ОСА и ВСА с последующим стентированием левой ОСА. Ход операции: типичным доступом выделены общая, наружная и внутренняя сонная артерии. После введения внутривенно 5000 ЕД гепарина, ВСА отсечена от ампулы. ОСА окклюзирована, ВСА стенозирована на 80%, НСА на 40%. Выполнена эверсионная эндартерэктомия из ВСА, получен хороший ретроградный кровоток.
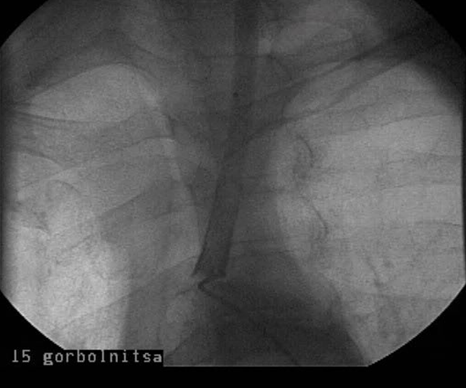
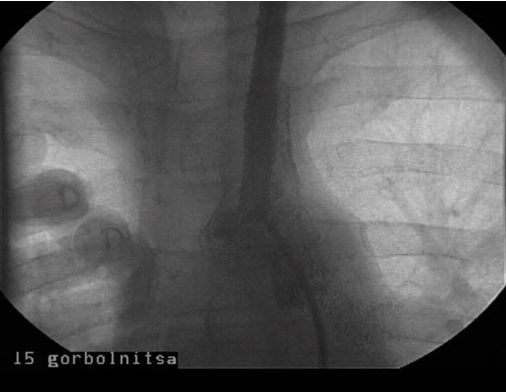
Из общей сонной артерии с помощью петли Вольмара выполнена эндартерэктомия, восстановлен адекватный антеградный кровоток. ВСА вшита в ОСА нитью пролен 7/0. На следующий день выполнена ангиография. Выявлен пристеночный дефект наполнения устья левой ОСА (рис. 2) и имплантированы два стента Eucatech AG 10.0×30 мм и 10.0×18 мм (рис. 3). При контрольной ангиографии интракраниальных отделов эмболических осложнений нет. Через четыре часа после завершения процедуры больной отметил слабость в правой верхней конечности. Больной осмотрен неврологом, выставлен диагноз ТИА в системе левой СМА. Неврологическая симптоматика регрессировала на следующий день. По данным КТ головного мозга от года, КТ картина энцефалопатии. Швы зажили первичным натяжением, больной выписан на восьмой день после операции.
Данное наблюдение говорит о возможности гибридной хирургии в лечении окклюзии общей сонной артерии при проходимой внутренней сонной артерии как альтернатива интраторакальным реконструкциям сонной артерии у симптомных пациентов.
Рисунок 1. МСКТ окклюзия левой ОСА
Рисунок 2. Пристеночный дефект наполнения устья левой ОСА
Рисунок 3. После имплантации стента Eucatech AG
Aguiar ET, Lederman A., Matsunaga P. retrograde common carotid endarterectomy: case report. Sao Paulo Med J 2002; 120: 154–7.
Fry W. R., Martin J. D., Clagett G. P., Fry carotid reconstruction: the subclavian_carotid artery bypass. J. Vasc. Surg. 1992; 15: 1: 83–89.
Laszlo Pinter, MD, Catherine Cagiannos, MD, Chris N. Bakoyiannis, MD, and Ralf Kolvenbach, MD,PhD, Hybrid treatment of common carotid artery occlusion with endarterectomy plus stenting, J Vasc Surg 2007; 46: 135–9.
Lyons C., Galbraith G. Surgical treatment of atherosclerotic occlusion of the internal carotid artery. Ann. Surg. 1957; 146: 487–494.
Martin R. S., Edwards W. H., Mulherin J. L. et al. Surgical treatment of common carotid artery occlusion. Am. J. Surg. 1993; 165: 3: 302–306.
Mikabe T., Tomita S., Watanabe S. et al. Subclavian artery to internal carotid artery bypass with saphenous vein graft in the treatment of bilateral common carotid artery occlusion (a case report). No. Shinkei. Geka.1992; 20: 7: 781–785.
Moore WS, Blaisdell W, Hall AD. Retrograde thrombectomy for chronic occlusion of the common carotid artery. Arch Surg1967; 95: 664–73.
Sullivan bypass to an «isolated» carotid bifurcation: a retrospective analysis. Ann. Vasc. Surg. 1996; 10: 3: 283–289.
Щеглов В. И., Уханов А. П., Васюков лечение окклюзирующих заболеваний брахиоцефальных артерий. Хирургия. 1990; 11: 49–51.
Атеросклероз (стеноз и окклюзия) сонных артерий

От инсульта ежегодно погибают или становятся инвалидами множество людей, хотя современная сосудистая хирургия позволяет предотвратить его у большинства пациентов. Только регулярная диагностика и доверие врачам позволит значительно снизить риск инсульта. Значительно проще лечить атеросклероз сонной артерии, чем ишемический инсульт и его последствия.
Причины и факторы риска
Сонные артерии парные крупные артериальные сосуды, которые кровоснабжают головной мозг в тех отделах, где расположены центры мышления, речи, личности, чувствительной и двигательной функции. Сонные артерии проходят по шее и через отверстия в черепе проникают в головной мозг.
При накоплении жировых веществ и холестерина образуется атеросклеротическая бляшка, которая сужает сонные артерии. Это уменьшает поток крови к мозгу и увеличивает риск ишемического инсульта. Инсульт происходит, когда поток крови не поступает в какие-либо отделы головного мозга. При инсульте внезапно выпадают некоторые функции мозга. Если отсутствие кровотока длится более трех-шести часов, то эти нарушения становятся необратимыми.
Почему при сужении сонной артерии развивается инсульт?
Факторы риска атеросклероза сонных артерий
Факторы риска для заболевания сонной артерии сходны с таковыми при других видах сердечно-сосудистых заболеваний. Они включают в себя:
 Клинические формы
Клинические формы
Атеросклеротические поражения сонных артерий чаще всего различаются по локализации основного процесса:
По УЗИ выделяется два основных типа атеросклеротических бляшек:
По степени сужения сонной артерии выделяют:
Жалобы и симптомы
Атеросклероз сонных артерий может протекать бессимптомно или вызывать жалобы, связанные с нарушением мозгового кровотока. Чаще всего пациенты могут жаловаться на временные нарушения функций мозга (транзиторная ишемическая атака) или стойкое их выпадение (ишемический инсульт).
Транзиторная ишемическая атака (ТИА)
При ТИА необходима неотложная медицинская помощь, поскольку невозможно предугадать, будет ли она прогрессировать в инсульт. Немедленное лечение может спасти жизнь и увеличить шансы на полное выздоровление.
Современные исследования показали, что пациенты, перенесшие ТИА имеют в 10 раз больше вероятность пострадать от обширного инсульта, чем человек, который не имел ТИА.
Ишемический инсульт имеет следующие признаки:
Ишемический инсульт и транзиторная ишемическая атака начинаются одинаково, поэтому любой ишемический инсульт можно назвать ишемической атакой, если симптомы полностью регрессируют в течение 24 часов от начала заболевания. Наличие временного промежутка между появлением симптомов инсульта и гибелью участков мозга позволяет выполнять срочную операцию по восстановлению мозгового кровотока.
Течение заболевания
Появившись, атеросклеротические бляшки уже не смогут рассосаться, но только постепенно прогрессируют. Скорость роста атерсклеротической бляшки зависит от многих факторов риска, от уровня холестерина. Всем людям старше 50 лет рекомендуется ежегодно выполнять УЗИ сонных артерий, для того, чтобы исключить развитие атеросклеротических бляшек и возникновение риска ишемического инсульта.
При развитии осложнений атеросклероза сонных артерий быстро прогрессирует дисциркуляторная энцефалопатия. Частые ТИА, а тем более ишемический инсульт, способствуют гибели части мозговой ткани и нарушению функций головного мозга. У пациентов с атеросклерозом сонных артерий нередко развивается сосудистая деменция (слабоумие).
После восстановления проходимости сонной артерии явления сосудисто-мозговой недостаточности купируются, вероятность повторных нарушений мозгового кровообращения значительно уменьшается.
Прогноз
Атеросклероз сонных артерий имеет значительный риск ишемического инсульта. При бессимптомном сужении внутренней сонной артерии более 70% риск ишемического инсульта превышает 5% в год. Если у пациента отмечались эпизоды нарушений мозгового кровообращения, то такой риск составляет уже 25% в год.
Риск ишемического инсульта при асимптомных атеросклеротических бляшках с сужением менее 70% не превышает такового у пациентов без атеросклероза.
После адекватного восстановления кровообращения по сонным артериям риск ишемического инсульта снижается более чем в 3 раза.
Преимущества лечения в клинике
Диагностика
Диагностика атеросклеротического поражения сонных артерий очень важна для профилактики ишемического инсульта. Своевременное выявление гемодинамически значимых стенозов позволяет снизить риск ишемического инсульта в 3 раза.
При осмотре сосудистым хирургом обязательно проводится выслушивание (аускультация) с обеих сторон шеи. Если при этом выслушивается грубый шум, то это свидетельствует о значимом поражении внутренних сонных артерий и требует дополнительных методов диагностики.
В обязательном порядке всем больным с подозрением на атеросклероз сонных артерий должен проводиться неврологический осмотр, чтобы исключить предшествующие поражения головного мозга.
Цели диагностики сужений сонных артерий:
Ультразвуковое исследование сонной артерии
Это неинвазивное, безболезненное исследование использует ультразвуковые волны для просмотра сонных артерий. Оно позволяет выявить атеросклеротические бляшки и тромбы и определяет степень их сужения. Доплеровское УЗИ показывает скорость потока крови по кровеносным сосудам.
Магнитно-резонансная ангиография (МРА)
Этот метод визуализации использует мощный магнит, чтобы собрать точную информацию о работе мозга и артерий. Затем компьютер использует эту информацию для создания изображения с высоким разрешением. МРА часто можно обнаружить даже небольшие бляшки в сосудах головного мозга и постинсультные очаги.
 Компьютерная томография в ангиорежиме (КТА)
Компьютерная томография в ангиорежиме (КТА)
Компьютерное томография с использованием контрастного вещества позволяет получить отчетливое изображение просвета сонных и мозговых артерий в трехмерном режиме. На компьютерной ангиографии хорошо видны атеросклеротические бляшки, тромбозы артерий, участки повреждения головного мозга. Доза рентгеновского излучения значительно меньше, чем при обычной рентгенографии.
Церебральная ангиография (каротидная ангиография)
Эта процедура считается «золотым стандартом» для визуализации сонных артерий. Эта процедура проводится через прокол в артерии, с подведением к интересующим сосудам специального катетера и введением контрастного вещества, которое хорошо видно при рентгеновском просвечивании. Ангиография позволяет точно определить показания к вмешательству на сонных артериях и выбрать необходимый метод лечения.
Подробнее о методах диагностики:
Лечение
Инновационный сосудистый центр применяет современные подходы к лечению атеросклероза сонных артерий. Мы внедрили в рутинную клиническую практику новые технологии лечения, делая профилактику инсульта максимально безопасной. В настоящее время мы отдаем предпочтение малоинвазивным методикам лечения, таким как стентирование сонных артерий и отходим от открытых операций.
Основной целью лечения при неосложненном атеросклерозе сонных артерий является профилактика дальнейшего прогрессирования атеросклеротической бляшки и сужения артерии. Для этого применяются медикаментозные препараты, снижающие уровень холестерина. Кроме того, назначаются препараты препятствующие образованию тромбов. Дозировка подбирается сосудистым хирургом, с учетом данных лабораторного обследования.
Для предупреждения развития ишемического инсульта пациент со стенозом сонных артерий должен выполнять несложные правила:
Какие препараты могут снизить риск инсульта?
Ваш врач может порекомендовать антиагрегантные препараты, такие как аспирин и клопидогрель (Плавикс), чтобы уменьшить риск инсульта, вызванного образованием тромбов. Ваш врач также может прописать лекарства для снижения уровня холестерина и артериального давления. При мерцательной аритмии может быть рекомендован препарат варфарин, чтобы уменьшить вероятность образования сгустков крови.
Хирургические вмешательства при стенозе сонных артерий
Что такое окклюзия правой вса
ФБГУ «Научный центр неврологии» РАН, Москва
Научный центр неврологии, Москва
Хирургическое лечение атеросклеротической окклюзии внутренней сонной артерии
Журнал: Журнал неврологии и психиатрии им. С.С. Корсакова. 2014;114(7): 67-72
Галкин П. В., Гуща А. О., Антонов Г. И. Хирургическое лечение атеросклеротической окклюзии внутренней сонной артерии. Журнал неврологии и психиатрии им. С.С. Корсакова. 2014;114(7):67-72.
Galkin P V, Gushcha A O, Antonov G I. Surgical treatment of the internal carotid artery atherosclerotic occlusion. Zhurnal Nevrologii i Psikhiatrii imeni S.S. Korsakova. 2014;114(7):67-72.
ФБГУ «Научный центр неврологии» РАН, Москва
Приблизительно у 15% пациентов c транзиторными ишемическими атаками или инфарктами в каротидном бассейне диагностируется окклюзия внутренней сонной артерии (ВСА). В обзоре обобщены результаты исследований эффективности лечения этой патологии путем наложения экстра-интракраниального микроартериального анастомоза (ЭИКМА). Исследования экстракраниального-интракраниального шунтирования (EC-IC Bypass) и хирургического лечения каротидной окклюзии (COSS) не выявили преимуществ хирургического лечения в сравнении с медикаментозной профилактикой у больных с симптомной окклюзией ВСА. Слабыми сторонами исследования COSS было избыточное доверие результатам, полученным в предшествующих работах, использование неубедительных диагностических критериев, разработанных для подтверждения декомпенсации церебральной гемодинамики, и высокая частота периоперационного инсульта. У больных с рецидивирующей ишемией головного мозга, которую не удается компенсировать медикаментозно, операция наложения ЭИКМА способна улучшить состояние, при условии низкой частоты периоперационного инсульта. Для более точной оценки возможностей улучшения функционального состояния и уменьшения выраженности когнитивных расстройств после реваскуляризации головного мозга необходимо проведение дополнительных исследований.
ФБГУ «Научный центр неврологии» РАН, Москва
Научный центр неврологии, Москва
Известно, что для обеспечения высокой активности метаболических процессов в головном мозге необходима постоянная поддержка его адекватного кровоснабжения [1, 2]. При нарушении кровоснабжения возникают патологические процессы, обусловленные ишемизацией мозговой ткани, что чаще всего связано с нарушениями структуры и функции мозговых сосудов.
В 1951 г. Ch. Fisher [3] была отмечена связь окклюзии внутренней сонной артерии (ВСА) с ишемическим инсультом. При этом автор подчеркнул, что окклюзия ВСА обычно развивается на фоне атеросклеротического поражения ее шейного сегмента, а предвещают приближающийся ишемический инсульт транзиторные ишемические атаки (ТИА).
Хотя до сих пор обсуждается патогенез развития ишемического инсульта у больных с окклюзией ВСА [4], она диагностируется приблизительно у 15% пациентов c ТИА или инфарктами в каротидном бассейне 5. При окклюзии крупных артерий церебральное перфузионное давление (ЦПД) снижается, и для его поддержания на требуемом уровне компенсаторно расширяются артерии среднего калибра (приводя к повышению сосудисто-мозгового объема) с одновременным усилением кровотока по существующим коллатералям. При этом показатели объемного мозгового кровотока не меняются. Данный механизм ауторегуляции мозгового кровотока соответствует I стадии гемодинамической декомпенсации. По мере дальнейшего снижения ЦПД, в том числе по причине недостаточно развитой коллатеральной сети, исчерпываются возможности компенсаторной вазодилатации, приводя к «срыву» ауторегуляции и понижению объемного мозгового кровотока. При этом метаболические процессы, обеспечивающие нормальное функционирование головного мозга, поддерживаются за счет повышенного потребления кислорода тканью мозга (II стадия) [9, 10]. Иногда II стадию декомпенсации церебральной гемодинамики называют «нищей» перфузией [11].
На сегодняшний день для исследования церебральной гемодинамики и оценки цереброваскулярного резерва применяются инструментальные методы, позволяющие оценить объем мозгового кровотока, в том числе с использованием внутривенной пробы с ацетазоламидом [12]. «Нищая» перфузия проявляется снижением объема мозгового кровотока на стороне окклюзии ВСА после введения ацетазоламида, тогда как в норме при этом он увеличивается 14. Исследование объема мозгового кровотока возможно с помощью позитронно-эмиссионной томографии (ПЭТ), однофотонной эмиссионной компьютерной томографии (КТ), КТ с ингаляцией ксенона, магнитно-резонансной томографии, транскраниальной допплерографии, а также перфузионной КТ (п-КТ) [15]. Преимуществами п-КТ являются ее общедоступность, простота и непродолжительность исследования, а также возможность получения количественных результатов [12, 16, 17]. Помимо объема мозгового кровотока, п-КТ оценивает сосудисто-мозговой объем и среднее время прохождения контрастного вещества по артериям в исследуемой области головного мозга [18].
Для улучшения коллатерального кровоснабжения головного мозга у больных с сосудисто-мозговой недостаточностью M. Yasargil и R. Donaghy в 1967 г. была разработана и внедрена в клиническую практику операция создания анастомоза между поверхностной височной артерией и ветвью средней мозговой артерии (цит. по [19]), получившая название «экстра-интракраниальный микроартериальный анастомоз» (ЭИКМА). Со временем операция ЭИКМА приобрела популярность в нейрохирургическом сообществе, например в 70-е годы в США ежегодно выполнялось несколько тысяч таких вмешательств [20, 21]. Однако проведенное в 1985 г. мультицентровое исследование (EC-IC Bypass Study) [22, 23], продолжавшееся 5 лет и включавшее 1377 больных, не выявило преимуществ операции ЭИКМА по сравнению с медикаментозной профилактикой ТИА и ишемического инсульта аспирином. Следует отметить, что исследование EC-IC Bypass оказалось недостаточно репрезентативным по больным, имеющим повышенный риск прогрессирования ишемии головного мозга, поскольку на момент его проведения отсутствовали диагностические методы, позволяющие выявить пациентов с декомпенсированной церебральной гемодинамикой 25.
В последующие 20 лет были разработаны нейровизуализационные методики, позволяющие облегчить отбор больных с окклюзирующими поражениями артерий головного мозга и с ожидаемой пользой от реваскуляризирующих вмешательств. Было проведено несколько исследований оценки риска развития ишемического инсульта в зависимости от выраженности расстройств церебральной гемодинамики. Например, в исследовании Каротидной Окклюзии St. Louis оценивалась возможность ПЭТ в выявлении «нищей» перфузии головного мозга. При повышении экстракции кислорода мозговой тканью было отмечено повышение риска ипсилатерального ишемического инсульта в течение 2 лет до 26,5% по сравнению с 5,3% у пациентов с нормальными показателями [10]. В исследовании из Японии [32] оценивался риск повторного ишемического инсульта методом ПЭТ при проведении нагрузочной пробы с ацетазоламидом. Ежегодный риск ишемического инсульта при наблюдении в сроки до 45,6 мес составил 10,6% для больных с повышенным потреблением кислорода мозговой тканью, тогда как при нормальном потреблении он отсутствовал [32].
COSS проводилось на территории США и Канады в 49 стационарах и 18 центрах, оснащенных позитронноэмиссионными томографами. Критериями включения пациентов в исследование было наличие ТИА либо ишемического инсульта (в одноименном полушарии с окклюзированной сонной артерией) в период до 120 дней с момента ишемического эпизода. Больные с асимметрией показателей экстракции кислорода ипсилатеральное/контралатеральное полушарие >1,13 рандомизировались в две группы: лечившиеся консервативным методом («консервативная») и хирургическим (ЭИКМА). Инсульт или летальный исход в течение 30 дней после операции либо ипсилатеральный ишемический инсульт в течение 2 лет стали определяющими критериями (конечная точка) для каждого клинического случая. После предварительного анализа результатов лечения 195 больных COSS было досрочно завершено по причине неубедительности полученных данных. Тем не менее представленные группой COSS наблюдения заслуживают внимания.
По данным COSS, определяющие критерии в течение 2 лет существенно не различались в выделенных группах, составив 21% в хирургической и 22,7% в «консервативной» группе соответственно.
В хирургической группе было зарегистрировано улучшение показателя экстракции кислорода по сравнению с исходным уровнем при проведении ПЭТ в сроки с 30-го по 60-й день после операции.
Для выяснения причин неэффективности критериев COSS, разработанных с целью выявления лиц с повышенным риском прогрессирования ишемии головного мозга, были оценены другие факторы, способствовавшие снижению заболеваемости инсультом в «консервативной» группе больных [36]. Во-первых, настолько ли специфична ПЭТ, чтобы ее использование было оправдано для отбора пациентов? Были проанализированы методики, использовавшиеся для оценки цереброваскулярного резерва с помощью ПЭТ. В исследовании Каротидной Окклюзии St. Louis, взятом «за основу» исследователями COSS, оценка экстракции кислорода мозговой тканью определялась как межполушарная разница показателей, т.е. полученные результаты имели относительный характер, тогда как в исследовании H. Yamauchi и соавт. [37] суждения о недостаточности кровоснабжения головного мозга принимались на основании абсолютных показателей экстракции кислорода. По мнению авторов, такой способ расчетов достовернее, поскольку: 1) даже при односторонней окклюзии ВСА страдает и контралатеральное полушарие вследствие развития синдрома обкрадывания, поскольку кровоснабжение полушария на ее стороне, как правило, осуществляется через переднюю соединительную артерию из бассейна контралатеральной ВСА; 2) при двусторонних либо множественных окклюзиях магистральных артерий головы судить о состоянии кровоснабжения полушарий головного мозга можно лишь на основании абсолютных показателей. Тем не менее анализ данных, полученных в исследовании Каротидной Окклюзии St. Louis, продемонстрировал, что методика расчета относительных показателей проще и имеет сходную чувствительность с расчетом абсолютных показателей в прогнозировании повышенного риска ишемии мозга [38]. Более того, в подгруппе больных с контралатеральными каротидными стенозами, включенных в исследование COSS, метод относительной (межполушарная) оценки экстракции кислорода вряд ли отражал истинное состояние кровоснабжения головного мозга, как и степень его компенсации. Обобщая сказанное, можно утверждать, что специально разработанные для выявления лиц с повышенным риском прогрессирования ишемии головного мозга критерии оценки результатов ПЭТ, использовавшиеся в исследовании COSS, оказались недостаточно эффективными. Во-вторых, исследователи COSS ориентировались на ретроспективный анализ подгрупп пациентов, вошедших в исследование Каротидной Окклюзии St. Louis, используя наиболее характерные клинические проявления, требовавшиеся для определения критериев, на основании которых в последующем вычленялись пациенты с повышенным риском прогрессирования ишемии мозга [39, 40]. Применение такого метода необоснованно, поскольку для прогнозирования того, что «возможно случится», использовался ретроспективный анализ данных, полученных не от всех больных, а лишь от определенных групп пациентов [41]. Неправомерность использования полученных на основании ретроспективного анализа результатов объясняется тем, что методика определения оптимальных точек пересечения при наслоении рисков предрасполагает к переоценке истинных различий и частоты развития конечного события в сравниваемых группах [42, 43].
Можно утверждать, что попытки «вычленения» пациентов с повышенным риском прогрессирования ишемии мозга и включения их в COSS оказались безуспешными из-за предвзятого отношения к результатам, полученным в предшествующих исследованиях, и неубедительных диагностических критериев, разработанных для подтверждения факта декомпенсации церебральной гемодинамики.
Исследование COSS продемонстрировало в хирургической группе больных тенденцию к снижению частоты ишемических эпизодов в отдаленные сроки после операции. Сходные результаты были получены японскими исследователями, предварительно сообщившими о снижении частоты инсульта после операции ЭИКМА. В исследовании JET [54, 55] риск периоперационного инсульта приблизился к нулю, что указывает на превосходство хирургического метода лечения над консервативным. К сожалению, окончательные результаты этого исследования пока не опубликованы. Исследование COSS однозначно продемонстрировало улучшение кровоснабжения головного мозга в послеоперационном периоде (подтверждено проведением ПЭТ в динамике). Полученные результаты согласуются с концепцией эффективности реваскуляризации головного мозга путем наложения экстра-интракраниального микроанастомоза, способного предупредить прогрессирование ишемии головного мозга при условии максимального уменьшения рисков периоперационного инсульта. Кумулятивные кривые Каплан-Мейера, смоделированные на 2-летний период и позволяющие сравнивать хирургический и консервативный методы по риску ишемического инсульта, не имеют достоверных отличий, однако не исключено, что их «продление» все-таки продемонстрирует преимущество оперативного метода. Это означает, что если все пациенты будут прослежены в сроки до 5 лет, исследование COSS сможет доказать эффективность хирургического метода (для этого риск развития инсульта должен оставаться неизменным в обеих группах более 2 лет).
О спонтанном улучшении кровоснабжения головного мозга без хирургического вмешательства (в основном за счет развития коллатералей) было сообщено в небольших обсервационных исследованиях, хотя опубликованные результаты носили противоречивый характер. В одном из них [56] сообщалось об улучшении состояния пациентов в отдаленные сроки наблюдения, тогда как в другом [57] улучшение состояния было зарегистрировано в течение первых месяцев с начала наблюдения и не имело продолжительного эффекта в виде снижения риска инсульта в отдаленные сроки. К сожалению, пациентам «консервативной» группы COSS ПЭТ в динамике не выполнялась, поэтому на сегодняшний день нельзя получить достоверных отдаленных результатов, как и прогнозировать вероятность пересечения кумулятивных кривых Каплан-Мейера при анализе результатов лечения.
Важно понимать, что исследование COSS было остановлено по причине неубедительности полученных результатов, не позволивших подтвердить гипотезу (риск развития инсульта 24% в хирургической и 40% в «консервативной» группе). Тем не менее, чтобы разница в рисках составила 10% в пользу хирургического метода лечения, требуется значительное увеличение (до 986) количества пациентов, включенных в исследование, что потребует привлечения дополнительных ресурсов и значительно удорожит его. Однако проведение такого исследования будет иметь значение для клинической практики и позволит получить ответ, который не дало исследование COSS [36].
Больные с рецидивирующей симптоматикой и грубым атеросклеротическим поражением магистральных артерий головы (у которых ишемия головного мозга провоцируется постуральными реакциями либо колебаниями артериального давления) как раз представляют тех пациентов, которым возможно улучшить кровоснабжение головного мозга путем реваскуляризирующих вмешательств. Такие пациенты не были «выделены» в исследовании COSS в отдельную подгруппу. Критерием включения в исследование был 120-дневный срок после ишемического «события», и одним из требований было стабильное состояние пациента, чтобы направить его для проведения ПЭТ (иногда даже требовался авиаперелет до ПЭТ-центра), чтобы принять окончательное решение о необходимости операции. Установлено, что обусловленная атеросклеротическим поражением магистральных артерий головы ишемия головного мозга наиболее часто рецидивирует в ранние сроки с момента появления первичных симптомов. Как правило, риск повторных ишемических атак у таких больных максимален в первые 2 нед с последующим снижением в дальнейшем 59. Согласно опубликованным результатам исследования COSS, среднее время от клинической манифестации до включения пациента в исследование составило 72 дня, что не исключает стабилизации кровоснабжения головного мозга у части больных. Отсутствие повторных ишемических атак в течение 6 дней с момента «включения» в исследование (до выполнения операции) наводит на мысль, что риски прогрессирования ишемии головного мозга у этих больных не были повышенными.
Хотя COSS прекращено, продолжается вспомогательное исследование, оценивающее когнитивные расстройства у больных с окклюзией ВСА «Рандомизированная оценка каротидной окклюзии и когнитивной функции» (RECON) [61]. Учитывая малое количество пациентов, перенесших реваскуляризацию головного мозга, исследование вряд ли сможет достоверно оценить влияние операции на когнитивные функции, но, вероятно, предоставит подтверждающие гипотезу доказательства, что прирост мозгового кровотока, помимо предупреждения повторного инсульта, также способствует ощутимому клиническому улучшению. Имеются сообщения 62 об уменьшении выраженности когнитивных расстройств как после операции ЭИКМА, так и после каротидной эндартерэктомии при стенозах сонных артерий. D. Jussen и соавт. [66], изучающие эффективность операций шунтирования артерий головного мозга у больных с неврологическими «выпадениями» после завершенного инсульта, сообщили об улучшении не только электрофизиологических показателей, но и клинического состояния после операций. Опубликованы результаты исследований [67, 68], предоставивших данные об увеличении мозгового кровотока в ишемизированных участках головного мозга после реваскуляризирующих вмешательств.
Приведенные в настоящем обзоре данные свидетельствуют, что на данный момент еще нет достаточных доказательств, способных подтвердить эффективность хирургического метода лечения. Это произошло, в основном, по причине переоценки ожидаемой заболеваемости инсультом в выбранной популяции больных. С момента завершения исследования EC-IC Bypass (1985) количество выполненных реваскуляризирующих вмешательств при окклюзии сонной артерии ограничилось ничтожно малой популяцией больных, прогрессирование ишемии головного мозга у которых не удавалось приостановить, используя даже максимально доступную антитромботическую терапию [52, 69]. Хотя COSS не предоставило доказательств в поддержку расширения показаний к хирургическому лечению, вероятно, у определенной категории пациентов можно добиться улучшения состояния в виде снижения риска инсульта при условии проведения операций в специализированных центрах и низких периоперационных осложнениях. Если посмотреть шире на проблему реваскуляризации головного мозга при окклюзии ВСА, то помимо предупреждения прогрессирования ишемии, шунтирование артерий головного мозга способно не только уменьшить выраженность когнитивных расстройств, но и улучшить функциональное состояние пациента уменьшением его зависимости либо полным избавлением от посторонней помощи, что должно стать предметом будущих научных исследований.
 Клинические формы
Клинические формы Компьютерная томография в ангиорежиме (КТА)
Компьютерная томография в ангиорежиме (КТА)