Что такое органические заболевания сердца
Какие бывают органические заболевания сердца?
На сегодня смертность из-за сердечно-сосудистых заболеваний повышена именно за счет органических патологий сердца. При этом на первое место по смертности во всем мире вышла ишемическая болезнь сердца.
Успешность лечения органических заболеваний сердца немало зависит от своевременной диагностике. Поэтому в определенном возрасте, начиная примерно с 50 лет, крайне важно регулярно проходить осмотры врачей, в том числе у кардиолога. При необходимости используются инструментальные методы диагностики в виде УЗИ сердца, электрокардиографии. В сложных случаях проводится электрофизиологическое исследование, часто используемое для определения формы аритмии.
Видео: Болезни сердца
Классификация болезней сердца
Сердце относится к жизненно важным органам, поэтому любые нарушения, связанные с его структурой или функционированием, приводят к тяжелым нарушениям во всем организме. Сегодня известен ряд органических болезней сердца, которые чаще всего приводят к деструкции тканей и в некоторых случаях становятся причиной гибели больного.
Условная классификация органических болезней сердца
Определение разновидности патологии позволяет установить причину его развития. В дальнейшем есть возможность провести эффективное лечение, что в результате повысит качество жизни больного, а в ряде случаев спасет его смерти.
Ишемическая болезнь сердца
В основе патологии лежит расстройство кровообращения по коронарным сосудам, питающим сердечную мышцу (миокард). Патология развивается на фоне атеросклероза сосудистой стенки, из-за чего ток крови по сосуду частично либо полностью прекращается. Также причиной ишемической болезни сердца (ИБС) может стать тромбоз коронарных сосудов, что также вызывает развитие клиники острого или хронического нарушения кровоснабжения.
Наиболее опасны острые формы ИБС, проявляющиеся нестабильной стенокардией, инфарктом миокарда и острым коронарным синдромом. Последнее заболевание становится причиной внезапной смерти. Дополнительно выделяют хронические формы ИБС, которым характерна на ярко выраженная клиника. В частности, сюда относится кардиосклероз, стабильная стенокардия и бессимптомная ишемия миокарда.
В каких случаях грозит развитие ИБС?
Ярко выраженная клиника ИБС включается в себя ряд характерных симптомов: жгучая загрудинная боль, проведение боли в область лопатки или по левой руке. Подобный приступ в зависимости от формы ИБС может продолжаться от нескольких минут до получаса. Появление болей указывает на недостаток кислорода в каком-то участке миокарда, поэтому при отсутствии лечения ишемии развивается инфаркт, со всеми отягчающими последствиями.
Инфаркт миокарда
Патогенез заболевания тесно связан с атеросклерозом, вследствие чего в своем развитии инфаркт миокарда проходит три этапа:
В большинстве случаев инфаркт миокарда развивается в типичной (ангинозной) форме, когда возникает сильная боль в области сердца, отдающая в левую руку, нижнюю челюсть, левую лопатку. Болезненные ощущения продолжаются длительно, около получаса и более.
Важно помнить, что при инфаркте миокарда не помогает нитроглицерин, поэтому такое лекарство рекомендуется принимать до оказания врачебной помощи с целью незначительного улучшения состояния больного.
Пороки сердца
Могут быть врожденные и приобретенные. Первая разновидность сердечных пороков чаще встречается у детей, когда при рождении у новорожденного определяются признаки нарушения развития сердца и сосудов (бледность или наоборот синюшность, плохое сосание, частые крики, одышка и пр.).
Основные формы врожденных пороков сердца:
В большинстве случаев при врожденных пороках требуется пластика дефекта либо ангиопластика. Лишь иногда, и то далеко не все пороки, могут самостоятельно разрешаться и ликвидироваться по достижению ребенком определенного возраста. Если же наоборот, у ребенка было все нормально, а затем при физической нагрузке начались проявляться симптомы болезни, нужно безотлагательно обратиться к кардиологу, чтобы было принято решение по оптимальному методу лечения.
Воспалительные заболевания
Инфекционные факторы воздействуют на сердце при наличии в организме хронического очага инфекции (кариозных зубов, пиелонефрита, хронических инфекционных заболеваний дыхательной системы). Если больной не лечит подобные очаги инфекции, или лечение недостаточно для ликвидации возбудителей, тогда они распространяются по всему организму, оседая на стенках сосудов и проникая дальше в ткани органов.
Воспалительные заболевания сердца:
Кроме воспалительных заболеваний ткани сердца могут подвергаться опухолевому процессу. В некоторых случаях развиваются кардиомиопатии, зачастую связанные с генетическими, аутоиммунными и прочими факторами воздействия.
Ревматические болезни сердца
В ходе развития ревматизма могут поражаться различные структуры сердца: эндотелий, миокард или эпикард. В некоторых случаях развивается в воспалительный процесс включаются все три оболочки сердца, тогда говорят о панкардите.
Ревматизм может протекать в острой, подострой, латентной и рецидивирующей форме.
При заболевании могут возникать как сердечные, так и неспецифические симптомы. К первым относится боль и ощущение давления за грудиной, аритмия, тахи или брадикардия, также может наблюдаться одышка. К неспецифическим проявлениям относят головокружение, головную боль, повышение температуры тела, воспалительные заболевания крупных и средних суставов.
Таким образом получается, что все заболевания сердца, нарушающие целость его структурных элементов, относятся к органическим. Их развитие нередко связано с серьезными гемодинамическими изменениями, поэтому крайне важно вовремя начать лечение, которое в основном проходит в условиях стационара.
Видео: Жить Здорово! Ревматический порок сердца
Ишемическая болезнь сердца

Причины
Ишемическая болезнь сердца начинается с повреждения коронарной артерии. Это может происходить даже в раннем возрасте. Данный процесс вызывают следующие факторы:
При нарушениях целостности стенок сосудов развивается атеросклероз. В месте повреждения накапливаются холестериновые отложения (бляшки) и другие клеточные продукты. В случае разрыва таких скоплений в этом месте появляется большое количество тромбоцитов, которые пытаются ликвидировать возникшее нарушение. Такой сгусток может стать причиной закупорки артерии и, как следствие, инфаркта.
Факторы риска
Перечисленные факторы риска зачастую провоцируют развитие друг друга, поэтому обычно не возникают по отдельности. Так, избыточный вес (ожирение) может приводить к появлению диабета и повышению АД. Соответственно, чем больше факторов риска, тем выше вероятность возникновения ишемической болезни сердца.
Симптомы
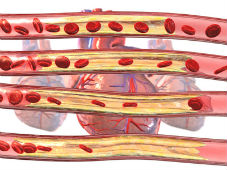
Стенокардия
Пациент ощущает сдавливание и тяжесть в груди. Боль возникает при физических или эмоциональных нагрузках и обычно проходит в состоянии покоя – через несколько минут после того, как прекращается действие провоцирующего фактора. Болевые ощущения также могут отдаваться в животе, спине или руке, особенно у женщин.
Одышка
Возникает в связи с тем, что сердце теряет способность перекачивать то количество крови, которое необходимо для нормальной работы организма. Одышка может сопровождаться быстрой утомляемостью при напряжении.
Инфаркт
Развивается при блокировке коронарной артерии. Характерные симптомы инфаркта: сильное сдавливание в груди, боль в плече или руке. Иногда приступ ИБС сопровождается одышкой и повышенным потоотделением. Менее типичные симптомы (чаще встречаются у женщин) включают тошноту, боль в спине или нижней челюсти. Инфаркт также может наступить внезапно, без каких-либо симптомов.
Последствия и осложнения
Ишемическая болезнь сердца – это самая распространенная (около 70 %) в мире причина внезапной смерти. В России же от ИБС ежегодно умирает около 700 тыс. человек. Приведенные показатели относятся в том числе к лицам трудоспособного возраста. В большей степени ИБС подвержены мужчины от 55 до 64 лет. Развитие разных форм ишемической болезни сердца нередко приводит к инвалидности. ИБС сопровождается такими изменениями, как снижение сократительной способности миокарда, дистрофия, некроз, склероз и др. Морфо-функциональные нарушения становятся причиной развития сердечной недостаточности.
Диагностика
На предварительном этапе диагностики ишемической болезни сердца для постановки диагноза врач выясняет медицинскую историю самого пациента и его семьи, проводит осмотр, назначает анализы. Для дальнейших уточнений могут понадобиться данные следующих обследований.
Позволяет обнаружить признаки инфаркта – как в момент приступа, так и перенесенного ранее. В некоторых случаях применяется суточное мониторирование по Холтеру, то есть запись работы сердца в течение суток. Определенные отклонения позволяют судить о недостаточности кровоснабжения.
ЭхоКГ
Данный вид ультразвуковой диагностики помогает установить, все ли части сердца работают правильно, позволяет выявить нарушения, связанные с кислородной недостаточности, или последствия инфаркта миокарда.
Стресс-тест
Проводится в виде испытания на велотренажере или беговой дорожке совместно с выполнением ЭхоКГ. Такая диагностика назначается, если симптомы ИБС возникают на фоне физической нагрузки. Функциональные пробы могут проводиться с использованием препаратов, стимулирующих работу сердца, вместо тренажеров.
Сердечная катетеризация (ангиография)
Этот вид диагностики позволяет проследить кровоток, идущий через сердце. Используемое в ангиографии контрастное вещество вводится в артерию (как правило, бедренную) через тонкую гибкую трубку. Применение рентгена позволяет выявить сужение/закупорку сосудов. Если существует блокировка, требующая лечения, то катетер дополняется раздувным баллоном, с помощью которого восстанавливается ток крови. Вставляемая далее металлическая трубка (стент) обеспечивает расширение артерии.
Данный способ диагностики также позволяет визуализировать артерии. Разновидностями метода компьютерной томографии являются КТ-ангиография и ультраскоростная компьютерная томография коронарных сосудов (УКТ). С помощью первого варианта обследования генерируется изображения артерий сердца, посредством второго можно выявить наличие кальция в жировых отложениях, которые сужают их.
МР-ангиография
Используя МРТ-технологии с введением контрастного вещества, можно визуализировать суженные или закупоренные участки сосудов. Однако данный вариант ангиографии считается менее информативным по сравнению с коронарной катетеризацией.
Лечение
Медикаментозное лечение
В лечении ишемической болезни сердца применяют лекарственные препараты различных групп, включая следующие:
Хирургическое вмешательство
В некоторых случаях требуется применение активных методов лечения, к которым относятся процедуры, направленные на восстановление и улучшение кровотока:
Профилактика
Наряду с медицинским лечением ишемической болезни сердца немаловажную роль играет диета. Коррекция питания предусматривает ограничение приема воды и соли (в том числе в пище), это позволяет снизить нагрузку на сердце. Низкожировая диета помогает замедлить прогрессирование атеросклероза и бороться с ожирением. По возможности рекомендуется ограничить или исключить сливочное масло, сало, жирное мясо, копчености, жареную пищу, сдобу, сладости и пр. Также важно соблюдать энергетический баланс: количество ежедневно расходуемых килокалорий должно превышать количество потребляемых минимум на 300. Кроме того, при различных проявлениях и формах ИБС показано ограничение режима активности, чтобы снизить потребность миокарда в кровоснабжении и кислороде. Среди других рекомендаций – отказ от курения, сокращение стресса, контроль давления.
В стремлении к сохранению здоровья сердца важно не пренебрегать регулярными медицинскими осмотрами, поскольку некоторые симптомы и факторы риска ишемической болезни обычно не проявляются на ранних стадиях заболевания. Чтобы проконсультироваться со специалистом и получить своевременное лечение, обращайтесь к специалистам клиники «ABC-медицина». Просто позвоните нам по номеру +7 (495) 223-38-83.
Заболевания сосудов
Что такое сердечно-сосудистые заболевания?

Основной причиной развития сердечно-сосудистых заболеваний является атеросклероз. И хотя невозможно исключить многие факторы риска развития атеросклероза, мы можем изменить, например, наш образ жизни и питания.
Факторы риска для сердечно-сосудистых заболеваний
Некоторые факторы риска сердечно-сосудистых заболеваний, потенциально обратимы или могут быть изменены. Они включают в себя:
Диета и сердечно-сосудистые заболевания
Внесение небольших изменений в вашем рационе является одним из самых простых и эффективных способов, уменьшения риска сердечно-сосудистых заболеваний. Вы можете сделать это следующим образом:
Холестерин и сердечно-сосудистые заболевания
Правильное питание и образ жизни
При уменьшении содержания жиров в пище, важно, не исключить из рациона «здоровые для сердца» жиры (моно- и полиненасыщенные жиры) в основном содержащиеся в растительных жирах и продуктах моря (рыбий жир).
Как изменить соотношение жиров в рационе:
Незаменимые жирные кислоты (Омега-3, Омега-6). Ранее известны, как витамин F. Витамин F важен для сердечно-сосудистой системы: препятствует развитию атеросклероза, улучшает кровообращение, обладает кардиопротекторным и антиаритмическим действием. Полиненасыщенные жирные кислоты уменьшают воспалительные процессы в организме, улучшают питание тканей. Незаменимые жирные кислоты содержатся в жирной рыбе. Для здоровья сердца необходимо съедать две порции рыбы в неделю, одна из которых должна быть жирной.
Станолы и стерины
Фрукты и овощи
Фрукты и овощи богаты многими важными питательными веществами, включая витамины С, Е, каротиноиды (антиоксиданты). Они могут помочь защитить сердце путем ограничения вредного воздействия холестерина на ткани организма. Что подтверждает необходимость ежедневного включения овощей и фруктов в рацион.
Цельнозерновые продукты и волокна
Исследования показали, что диеты, богатые по содержанию цельнозерновых могут уменьшить риск сердечно-сосудистых заболеваний на 30 процентов. Необходимо включать цельнозерновые продукты в каждый прием пищи, выбирая хлеб из непросеянной муки грубого помола и используя соответствующие сорта макарон и риса.
Соевый белок. Рекомендация диеты, которая включает в себя, по меньшей мере, 25 г сои в день, была связана с уменьшением холестерина и сердечнососудистых заболеваний. Соевые изофлавоны, в частности, снижают риск сердечнососудистых заболеваний, поскольку они подавляют рост клеток, которые образуются при закупорке артерий при атеросклерозе. Соевый белок также является отличной заменой мяса и доступен в удобной и вкусной форме во многих готовых блюдах. Еще один хороший источник белка соевое молоко и йогурт.
Отдых и релаксация
Курение
Регулярное наблюдение
Необходимо регулярно измерять кровяное давление, рост и вес, определять уровень холестерина в крови. Высокий уровень тестов должен служить основанием к назначению соответствующих рекомендаций.
Сердечная недостаточность
Сердечной недостаточностью страдает, по крайней мере, один из 100 человек, сердечная недостаточность является причиной одной из 20 госпитализаций, приводит к летальному исходу чаще, чем многие виды рака. В то же время позитивным моментом является возможность проведения эффективного лечения.
Что такое сердечная недостаточность?
Симптомы сердечной недостаточности
Основные жалобы больных при развитии сердечной недостаточности:
Причины сердечной недостаточности
Диагностика сердечной недостаточности
Электрокардиография (ЭКГ) помогает врачам выявлять признаки гипертрофии и недостаточности кровоснабжения (ишемии) миокарда, а также различные аритмии.
Эхокардиография (ЭхоКГ). С помощью этого метода можно не только установить причину сердечной недостаточности, но и оценить сократительную функцию желудочков сердца.
Рентгенологическое исследование органов грудной клетки при сердечной недостаточности выявляет застой крови в малом круге кровообращения и увеличение размеров полостей сердца (кардиомегалия).
Радиоизотопные методы исследования сердца, в частности, радиоизотопная вентрикулография, позволяют с высокой точностью у больных сердечной недостаточностью оценить сократительную функцию желудочков сердца, объем вмещаемой ими крови. Данные методы основаны на введении и последующем распределении в организме радиоизотопных препаратов.
Лечение сердечной недостаточности
При развитии острой сердечной недостаточности необходима госпитализация. Основной акцент в лечении делается как на устранении причин сердечной недостаточности (стресс, избыточное употребление поваренной соли, злоупотребление алкоголем, курение, повышенное кровяное давление, а также прием препаратов, способствующих задержке жидкости в организме и т.д.), так и на коррекцию ее проявлений. Ограничение физических нагрузок. Физическая нагрузка допустима и желательна, однако она не должна вызывать значительной усталости и неприятных ощущений. Диета должна быть с пониженным содержанием соли, с большим количеством фруктов и овощей. Очень важно добиться снижения избыточного веса, так как он создает значительную дополнительную нагрузку на больное сердце.
В настоящее время для лечения сердечной недостаточности применяют следующие лекарственные средства, способствующие:
При неэффективности лекарственных средств, используемых для лечения хронической сердечной недостаточности, может быть рекомендовано хирургическое лечение – кардиомиопластика, электрокардиостимуляция. Как правило, медицинское наблюдение за пациентами с сердечной недостаточностью необходимо в течение всей жизни.
ЭКСТРАСИСТОЛИЯ: клиническое значение, диагностика и лечение
Экстрасистолами называют преждевременные комплексы (преждевременные сокращения), выявляемые на ЭКГ. По механизму возникновения преждевременные комплексы подразделяются на экстрасистолы и парасистолы. Различия между экстрасистолией и парасистолией являютс
Экстрасистолами называют преждевременные комплексы (преждевременные сокращения), выявляемые на ЭКГ. По механизму возникновения преждевременные комплексы подразделяются на экстрасистолы и парасистолы. Различия между экстрасистолией и парасистолией являются чисто электрокардиографическими или электрофизиологическими. Клиническое значение и лечебные мероприятия при экстрасистолии и парасистолии абсолютно одинаковы. По локализации источника аритмии электросистолы разделяют на наджелудочковые и желудочковые.
Экстрасистолы, несомненно, являются самым распространенным нарушением ритма сердца. Они часто регистрируются и у здоровых лиц. При проведении суточного мониторирования ЭКГ статистической «нормой» экстрасистол считается примерно до 200 наджелудочковых экстрасистол и до 200 желудочковых экстрасистол в сутки. Экстрасистолы могут быть одиночными или парными. Три и более экстрасистолы подряд принято называть тахикардией («пробежки» тахикардии, «короткие эпизоды неустойчивой тахикардии»). Неустойчивой тахикардией называют эпизоды тахикардии продолжительностью менее 30 с. Иногда для обозначения 3–5 экстрасистол подряд используют определение «групповые», или «залповые», экстрасистолы. Очень частые экстрасистолы, особенно парные и рецидивирующие «пробежки» неустойчивой тахикардии, могут достигать степени непрерывно-рецидивирующей тахикардии, при которой от 50 до 90% сокращений в течение суток составляют эктопические комплексы, а синусовые сокращения регистрируются в виде единичных комплексов или коротких кратковременных эпизодов синусового ритма.
В практической работе и научных исследованиях основное внимание уделяют желудочковой экстрасистолии. Одной из наиболее известных классификаций желудочковых аритмий является классификация B. Lown и M. Wolf (1971).
Предполагалось, что высокие градации экстрасистол (классы 3–5) являются наиболее опасными. Однако в дальнейших исследованиях было установлено, что клиническое и прогностическое значение экстрасистолии (и парасистолии) практически целиком определяется характером основного заболевания, степенью органического поражения сердца и функциональным состоянием миокарда. У лиц без признаков поражения миокарда с нормальной сократительной функцией левого желудочка (фракция выброса больше 50%) экстрасистолия, включая эпизоды неустойчивой желудочковой тахикардии и даже непрерывно-рецидивирующей тахикардии, не влияет на прогноз и не представляет опасности для жизни. Аритмии у лиц без признаков органического поражения сердца называют идиопатическими. У больных с органическим поражением миокарда (постинфарктный кардиосклероз, дилатация и/или гипертрофия левого желудочка) наличие экстрасистолии считается дополнительным прогностически неблагоприятным признаком. Но даже в этих случаях экстрасистолы не имеют самостоятельного прогностического значения, а являются отражением поражения миокарда и дисфункции левого желудочка.
В 1983 г J. T. Bigger предложил прогностическую классификацию желудочковых аритмий.
Однако, как было отмечено, независимого прогностического значения желудочковая экстрасистолия не имеет. Сами по себе экстрасистолы в большинстве случаев безопасны. Экстрасистолию даже называют «косметической» аритмией, подчеркивая этим ее безопасность. Даже «пробежки» неустойчивой желудочковой тахикардии тоже относят к «косметическим» аритмиям и называют «энтузиастическими выскальзывающими ритмами» (R. W. Campbell, K. Nimkhedar, 1990). В любом случае лечение экстрасистолии с помощью антиаритмических препаратов (ААП) не улучшает прогноз. В нескольких крупных контролируемых клинических исследованиях было выявлено заметное повышение общей смертности и частоты внезапной смерти (в 2–3 раза и более) у больных с органическим поражением сердца на фоне приема ААП класса I, несмотря на эффективное устранение экстрасистол и эпизодов желудочковой тахикардии. Наиболее известным исследованием, в котором впервые было выявлено несоответствие клинической эффективности препаратов и их влияния на прогноз, является исследование CAST. В исследовании CAST («исследование подавления аритмий сердца») у больных, перенесших инфаркт миокарда, на фоне эффективного устранения желудочковой экстрасистолии препаратами класса I С (флекаинид, энкаинид и морицизин) выявлено достоверное увеличение общей смертности в 2,5 раза и частоты внезапной смерти в 3,6 раза по сравнению с больными, принимавшими плацебо. Результаты исследования заставили пересмотреть тактику лечения не только пациентов с нарушениями ритма, но и кардиологических больных вообще. Исследование CAST является одним из основных в становлении «медицины, основанной на доказательствах». Только на фоне приема β- адреноблокаторов и амиодарона отмечено снижение смертности больных с постинфарктным кардиосклерозом, сердечной недостаточностью или реанимированных пациентов. Однако положительное влияние амиодарона и особенно β-адреноблокаторов не зависело от антиаритмического действия этих препаратов.
Выявление экстрасистолии (как и любого другого варианта нарушений ритма) является поводом для обследования, направленного прежде всего на выявление возможной причины аритмии, заболевания сердца или экстракардиальной патологии и определения функционального состояния миокарда.
ААП не излечивают от аритмии, а только устраняют ее на период приема препаратов. При этом побочные реакции и осложнения, связанные с приемом практически всех препаратов, могут быть гораздо более неприятными и опасными, чем экстрасистолия. Таким образом, само по себе наличие экстрасистолии (независимо от частоты и «градации») не является показанием для назначения ААП. Бессимптомные или малосимптомные экстрасистолы не требуют проведения специального лечения. Таким больным показано диспансерное наблюдение с проведением эхокардиографии примерно 2 раза в год для выявления возможных структурных изменений и ухудшения функционального состояния левого желудочка. Л. М. Макаров и О. В. Горлицкая (2003) при длительном наблюдении за 540 больными с идиопатической частой экстрасистолией (более 350 экстрасистол в час и более 5000 в сутки) выявили у 20% больных увеличение полостей сердца («аритмогенная кардиомиопатия»). Причем более часто увеличение полостей сердца отмечалось при наличии предсердной экстрасистолии.
Показания для лечения экстрасистолии:
Лечение экстрасистолии
Необходимо объяснить больному, что малосимптомная экстрасистолия безопасна, а прием антиаритмических препаратов может сопровождаться неприятными побочными эффектами или даже вызвать опасные осложнения. Прежде всего необходимо устранить все потенциально аритмогенные факторы: алкоголь, курение, крепкий чай, кофе, прием симпатомиметических препаратов, психоэмоциональное напряжение. Следует немедленно приступить к соблюдению всех правил здорового образа жизни.
При наличии показаний для назначения ААП у больных с органическим поражением сердца используют β-адреноблокаторы, амиодарон и соталол. У больных без признаков органического поражения сердца, кроме этих препаратов, применяют ААП класса I: Этацизин, Аллапинин, Пропафенон, Кинидин Дурулес. Этацизин назначают по 50 мг 3 раза в день, Аллапинин — по 25 мг 3 раза в день, Пропафенон — по 150 мг 3 раза в день, Кинидин Дурулес — по 200 мг 2–3 раза в день.
Лечение экстрасистолии проводят методом проб и ошибок, последовательно (по 3–4 дня) оценивая эффект приема антиаритмических препаратов в средних суточных дозах (с учетом противопоказаний), выбирая наиболее подходящий для данного больного. Для оценки антиаритмического эффекта амиодарона может потребоваться несколько недель или даже месяцев (применение более высоких доз амиодарона, например по 1200 мг/сут, может сократить этот период до нескольких дней).
Эффективность амиодарона в подавлении желудочковых экстрасистол составляет 90–95%, соталола — 75%, препаратов класса I C — от 75 до 80% (B. N. Singh, 1993).
Критерий эффективности ААП — исчезновение ощущения перебоев, улучшение самочувствия. Многие кардиологи предпочитают начинать подбор препаратов с назначения β-адреноблокаторов. У больных с органическим поражением сердца при отсутствии эффекта от β-адреноблокаторов применяют Амиодарон, в том числе в комбинации с первыми. У больных с экстрасистолией на фоне брадикардии подбор лечения начинают с назначения препаратов, ускоряющих ЧСС: можно попробовать прием пиндолола (Вискен), эуфиллина (Теопек) или препаратов класса I (Этацизин, Аллапинин, Кинидин Дурулес). Назначение холинолитических препаратов типа белладонны или симпатомиметиков менее эффективно и сопровождается многочисленными побочными явлениями.
В случае неэффективности монотерапии оценивают эффект комбинаций различных ААП в уменьшенных дозах. Особенно популярны комбинации ААП с β-адреноблокаторами или амиодароном.
Есть данные, что одновременное назначение β-адреноблокаторов (и амиодарона) нейтрализует повышенный риск от приема любых антиаритмических средств. В исследовании CAST у больных, перенесших инфаркт миокарда, которые наряду с препаратами класса I C принимали β-адреноблокаторы не было отмечено увеличения смертности. Более того, было выявлено снижение частоты аритмической смерти на 33%!
Особенно эффективна комбинация β-адреноблокаторов и амиодарона. На фоне приема такой комбинации наблюдалось еще большее снижение смертности, чем от каждого препарата в отдельности. Если ЧСС превышает 70–80 уд./мин в покое и интервал P–Q в пределах 0,2 с, то проблемы с одновременным назначением амиодарона и β-адреноблокаторов нет. В случае брадикардии или АВ-блокады I–II степени для назначения амиодарона, β-адреноблокаторов и их комбинации необходима имплантация кардиостимулятора, функционирующего в режиме DDD (DDDR). Есть сообщения о повышении эффективности антиаритмической терапии при сочетании ААП с ингибиторами АПФ, блокаторами рецепторов ангиотензина, статинами и препаратами омега-3-ненасыщенных жирных кислот.
Некоторые противоречия существуют в отношении применения амиодарона. С одной стороны, некоторые кардиологи назначают амиодарон в последнюю очередь — только при отсутствии эффекта от других препаратов (считая, что амиодарон довольно часто вызывает побочные явления и требует длительного «периода насыщения»). С другой стороны, возможно, более рационально начинать подбор терапии именно с амиодарона как наиболее эффективного и удобного для приема препарата. Амиодарон в малых поддерживающих дозах (100–200 мг в день) редко вызывает серьезные побочные явления или осложнения и является скорее даже более безопасным и лучше переносимым, чем большинство других антиаритмических препаратов. В любом случае при наличии органического поражения сердца выбор небольшой: β-адреноблокаторы, амиодарон или соталол. При отсутствии эффекта от приема амиодарона (после «периода насыщения» — как минимум по 600–1000 мг/сут в течение 10 дней) можно продолжить его прием в поддерживающей дозе — 0,2 г/сут и, при необходимости, оценить эффект последовательного добавления препаратов класса I С (Этацизин, Пропафенон, Аллапинин) в половинных дозах.
У больных с сердечной недостаточностью заметное уменьшение количества экстрасистол может отмечаться на фоне приема ингибиторов АПФ и Верошпирона.
Следует отметить, что проведение суточного мониторирования ЭКГ для оценки эффективности антиаритмической терапии утратило свое значение, так как степень подавления экстрасистол не влияет на прогноз. В исследовании CAST выраженное увеличение смертности отмечено на фоне достижения всех критериев полного антиаритмического эффекта: уменьшения общего количества экстрасистол более чем на 50%, парных экстрасистол — не менее чем на 90% и полное устранение эпизодов желудочковой тахикардии. Основным критерием эффективности лечения является улучшение самочувствия. Это обычно совпадает с уменьшением количества экстрасистол, а определение степени подавления экстрасистолии не имеет значения.
В целом последовательность подбора ААП у больных с органическим заболеванием сердца, при лечении рецидивирующих аритмий, включая экстрасистолию, можно представить в следующем виде.
У больных без признаков органического поражения сердца можно использовать любые препараты, в любой последовательности или использовать схему, предложенную для больных с органическим заболеванием сердца.
Краткая характеристика ААП
β-адреноблокаторы. После исследования CAST и опубликования результатов метаанализа исследований по применению ААП класса I, в котором было показано, что практически все ААП класса I способны увеличивать смертность у больных с органическим поражением сердца, β-адреноблокаторы стали самыми популярными антиаритмическими препаратами.
Антиаритмический эффект β-адреноблокаторов обусловлен именно блокадой β-адренергических рецепторов, т. е. уменьшением симпатико-адреналовых влияний на сердце. Поэтому β-адреноблокаторы наиболее эффективны при аритмиях, связанных с симпатико-адреналовыми влияниями — так называемые «катехоламинзависимые» или «адренергические аритмии». Возникновение таких аритмий, как правило, связано с физической нагрузкой или психоэмоциональным напряжением.
Катехоламинзависимые аритмии в большинстве случаев одновременно являются «тахизависимыми», т. е. возникают при достижении определенной критической частоты сердечных сокращений, например во время физической нагрузки частая желудочковая экстрасистолия или желудочковая тахикардия возникают только при достижении частоты синусового ритма 130 сокращений в минуту. На фоне приема достаточной дозы β-адреноблокаторов больной не сможет достичь частоты 130 уд./мин при любом уровне физической нагрузки, таким образом предотвращается возникновение желудочковых аритмий.
β-адреноблокаторы являются препаратами выбора для лечения аритмий при врожденных синдромах удлинения интервала Q–T.
При аритмиях, не связанных с активацией симпатической нервной системы β-адреноблокаторы гораздо менее эффективны, но добавление β-адреноблокаторов нередко значительно увеличивает эффективность других антиаритмических препаратов и снижает риск аритмогенного эффекта ААП класса I. Препараты класса I в сочетании с β-адреноблокаторами не увеличивают смертность у больных с им поражением сердца (исследование CAST).
При так называемых «вагусных» аритмиях β-адреноблокаторы оказывают аритмогенное действие. «Вагусные» аритмии возникают в состоянии покоя, после еды, во время сна, на фоне урежения ЧСС («брадизависимые» аритмии). Вместе с тем в некоторых случаях при брадизависимых аритмиях эффективно применение пиндолола (Вискен) — β-адреноблокатора с внутренней симпатомиметической активностью (ВСА). Кроме пиндолола к β-адреноблокаторам с ВСА относятся окспренолол (Тразикор) и ацебутолол (Сектраль), однако в максимальной степени внутренняя симпатомиметическая активность выражена именно у пиндолола.
Дозы β-адреноблокаторов регулируют в соответствии с антиаритмическим эффектом. Дополнительным критерием достаточной β-блокады является снижение ЧСС до 50 уд./мин в состоянии покоя. В прежние годы, когда основным β-адреноблокатором был пропранолол (Анаприлин, Обзидан), известны случаи эффективного применения пропранолола при желудочковых аритмиях в дозах до 960 мг/сут и более, например до 4 г в день! (R. L. Woosley et al., 1979).
Амиодарон. Амиодарон таблетки 0,2 г. (оригинальным препаратом является Кордарон) обладает свойствами всех четырех классов ААП и, кроме того, оказывает умеренное a-блокирующее действие. Амиодарон, несомненно, является самым эффективным из существующих антиаритмических препаратов. Его даже называют «аритмолитическим препаратом».
Основным недостатком амиодарона является высокая частота экстракардиальных побочных эффектов, которые при длительном приеме наблюдаются у 10–75% больных. Однако необходимость в отмене амиодарона возникает у 5–25% (J. A. Johus et al., 1984; J. F. Best et al., 1986; W. M. Smith et al., 1986). К основным побочным эффектам амиодарона относятся: фотосенсибилизация, изменение цвета кожи, нарушение функции щитовидной железы (как гипотиреоз, так и гипертиреоз), повышение активности печеночных трансаминаз, периферические нейропатии, мышечная слабость, тремор, атаксия, нарушения зрения. Большинство этих побочных эффектов обратимы и исчезают после отмены или при уменьшении дозы амиодарона. Гипотиреоз можно контролировать с помощью приема левотироксина. Наиболее опасным побочным эффектом амиодарона является поражение легких («амиодароновое поражение легких») — возникновение интерстициального пневмонита или, реже, легочного фиброза. У большинства больных поражение легких развивается только при длительном приеме сравнительно больших поддерживающих доз амиодарона — более 400 мг/сут. Такие дозы крайне редко применяют в России. Поддерживающая доза амиодарона в России обычно составляет 200 мг/сут или даже меньше (по 200 мг в день 5 дней в неделю). B. Clarke и соавторы (1985) сообщают лишь о трех случаях из 48 наблюдений возникновения этого осложнения на фоне приема амиодарона в дозе 200 мг в сутки.
В настоящее время изучается эффективность дронедарона, деривата амиодарона без йода. Предварительные данные свидетельствуют об отсутствии экстракардиальных побочных эффектов у дронедарона.
Соталол. Соталол (Соталекс, Сотагексал) таблетки 160 мг применяется в средней суточной дозе 240–320 мг. Начинают с назначения 80 мг 2 раза в день. При рефрактерных аритмиях иногда используют прием соталола до 640 мг/сут. β-адреноблокирующее действие соталола проявляется начиная с дозы 25 мг.
На фоне приема соталола имеется повышенный риск развития желудочковой тахикардии типа «пируэт». Поэтому прием соталола желательно начинать в стационаре. При назначении соталола необходимо тщательно контролировать величину интервала Q–T, особенно в первые 3 дня. Корригированный интервал Q–T не должен превышать 0,5 с. В этих случаях риск развития тахикардии типа «пируэт» менее 2%. С увеличением дозы соталола и степени удлинения интервала Q–T значительно увеличивается риск развития тахикардии типа «пируэт». Если корригированный интервал Q–T превышает 0,55 с — риск тахикардии типа «пируэт» достигает 11%. Поэтому при удлинении интервала Q–T до 0,5 с необходимо уменьшить дозу соталола или отменить препарат.
Побочные эффекты соталола соответствуют типичным побочным эффектам β-адреноблокаторов.
Этацизин. Этацизин таблетки 50 мг. Наиболее изученный отечественный препарат (создан в СССР). Для лечения аритмий применяется с 1982 г. Быстрое достижение клинического эффекта позволяет с успехом использовать Этацизин у лиц без органического поражения сердца для лечения желудочковых и наджелудочковых нарушений ритма: экстрасистолии, всех вариантов пароксизмальных и хронических тахиаритмий, в том числе мерцательной аритмии, при синдроме Вольфа–Паркинсона–Уайта. Наиболее эффективен Этацизин у пациентов с ночными аритмиями, а также при желудочковой экстрасистолии.Средняя суточная доза Этацизина составляет 150 мг (по 50 мг 3 раза в день). Максимальная суточная доза — 250 мг. При назначении этацизина для предупреждения рецидивирования мерцательной аритмии, наджелудочковых и желудочковых тахикардий его эффективность, как правило, превосходит эффективность других АПП класса I. Препарат хорошо переносится, необходимость в отмене возникает примерно у 4% больных. Основные побочные эффекты: головокружение, головная боль, «онемение» языка, нарушение фиксации взора. Обычно побочные реакции наблюдаются сравнительно редко, и их выраженность уменьшается после первой недели приема Этацизина.
Аллапинин. Отечественный препарат Аллапинин, таблетки 25 мг (создан также в СССР) применяется в клинической практике с 1986 г. Назначают по 25–50 мг 3 раза в день. Максимальная суточная доза составляет 300 мг. Аллапинин довольно эффективен при наджелудочковых и желудочковых аритмиях. Основные побочные явления — головокружение, головная боль, нарушение фиксации взора. Необходимость в отмене возникает примерно у 6% больных. Одной из особенностей аллапинина и теоретически его недостатком является наличие β-адреностимулирующего действия.
Пропафенон (Ритмонорм, Пропанорм), таблетки 150 мг, ампулы 10 мл (35 мг). Назначают по 150–300 мг 3 раза в день. При необходимости дозу увеличивают до 1200 мг/сут. Пропафенон, кроме замедления проведения, слегка удлиняет рефрактерные периоды во всех отделах сердца. Кроме того, пропафенон обладает небольшим β-адреноблокирующим действием и свойствами антагонистов кальция.
К основным побочным эффектам пропафенона относятся головокружение, нарушение фиксации взора, атаксия, тошнота, металлический вкус во рту.
Хинидин. В настоящее время в России используют в основном Кинидин Дурулес, табл. по 0,2 г. Разовая доза составляет 0,2–0,4 г, средняя суточная доза — от 0,6 до 1,0 г. Максимальная суточная доза хинидина в прежние годы (когда хинидин был основным антиаритмическим препаратом) достигала 4,0 г! В настоящее время такие дозы не используются и примерной максимальной суточной дозой хинидина можно считать 1,6 г.
В небольших дозах (600–800 мг/сут) хинидин хорошо переносится. Побочные явления возникают обычно при более высоких дозах. К наиболее частым побочным эффектам при приеме хинидина относятся нарушения функции желудочно-кишечного тракта: тошнота, рвота, понос. Реже отмечаются головная боль, головокружения, ортостатическая гипотония. Самое опасное осложнение от приема хинидина — возникновение желудочковой тахикардии типа «пируэт». По данным литературы, это осложнение наблюдается у 1–3% больных, принимающих хинидин.
П. Х. Джанашия, доктор медицинских наук, профессор
С. В. Шлык, доктор медицинских наук, профессор
Н. М. Шевченко, доктор медицинских наук, профессор
РГМУ, Москва


