Что такое шванновские клетки
Шванновские клетки
Шванновские клетки (леммоциты) — вспомогательные клетки нервной ткани, которые формируются вдоль аксонов периферических нервных волокон. Создают, а иногда и разрушают, электроизолирующую миелиновую оболочку нейронов. Выполняют опорную (поддерживают аксон) и трофическую (питают тело нейрона) функции. Описаны немецким физиологом Теодором Шванном в 1838 году и названы в его честь.
Каждое периферическое нервное волокно одето тонким цитоплазматическим слоем — невролеммой или шванновской оболочкой. Волокно является миелинизированным, если между ним и цитоплазмой шванновской клетки имеется значительный слой миелина. Если волокна лишены миелина, то они называются немиелинизированными безмякотными. [1] Шванновские клетки могут осуществлять волнообразные движения, что, вероятно, способствует транспортировке различных веществ по отросткам нервных клеток.
С нарушением работы шванновских клеток связаны такие нервные заболевания, как синдром Гийена — Барре, болезнь Шарко-Мари, шванноматозис и хроническая воспалительная демиелинизирующая полинейропатия. Демиелинизация в основном происходит [2] из-за ослабления двигательных функций шванновских клеток, в результате чего они оказываются не способны образовывать миелиновую оболочку.
См. также
Примечания
Полезное
Смотреть что такое «Шванновские клетки» в других словарях:
ШВАННОВСКИЕ КЛЕТКИ — (леммоциты), клетки, покрывающие АКСОНЫ нервных волокон, образуя защитную жировую МИЕЛИНОВУЮ ОБОЛОЧКУ, которая служит для электрической изоляции нерва и позволяет ускорять передачу нервных импульсов. Между шванновскими клетками находятся… … Научно-технический энциклопедический словарь
Шванновские клетки — – клетки миелиновой оболочки аксонов центральной и периферической нервной системы. Шванновские клетки способствуют регенерации повреждённых аксонов, определяют направление их роста. Кроме того, из этих клеток образуются невриномы. В ЦНС… … Энциклопедический словарь по психологии и педагогике
ШВАННОВСКИЕ КЛЕТКИ — (по имени Т. Шванна) образуют оболочки периферических нервных волокон. Выполняют опорную и трофическую функции … Большой Энциклопедический словарь
ШВАННОВСКИЕ КЛЕТКИ — леммоциты (lemmocyti), разновидность клеток олигодендроглии, образуют оболочки отростков нейронов в периферич. нервах и ганглиях. Описаны Т. Шванном в 1838. В безмякотных нервных волокнах III. к. формируют тонкую шванновскую оболочку, заключающую … Биологический энциклопедический словарь
Шванновские клетки — (по имени Т. Шванна), образуют оболочки периферических нервных волокон. Выполняют опорную и трофическую функции. * * * ШВАННОВСКИЕ КЛЕТКИ ШВАННОВСКИЕ КЛЕТКИ (по имени Т. Шванна), образуют оболочки периферических нервных волокон. Выполняют опорную … Энциклопедический словарь
ШВАННОВСКИЕ КЛЕТКИ — Клетки, которые образуют невриномы, покрывающие миелиновой оболочкой аксоны периферийной нервной системе. Они отличаются от олигодендроглии (см. глия), находящейся в центральной нервной системе, тем, что помогают регенерации поврежденных аксонов … Толковый словарь по психологии
Шванновские клетки — леммоциты, клетки нервной ткани, образующие оболочки длинных отростков нервных клеток (Аксонов) в периферических нервах и ганглиях. Описаны Т. Шванном в 1838. Ядро Ш. к. овальное, с 1 2 ядрышками; хроматин образует скопления по внутренней … Большая советская энциклопедия
ШВАННОВСКИЕ КЛЕТКИ — (по имени Т. Шванна), образуют оболочки периферич. нерв. волокон. Выполняют опорную и трофич. функции … Естествознание. Энциклопедический словарь
шванновские клетки — (от г. Шванн) … Орфографический словарь русского языка
Клетки Фаланговые (Phalangeal Cells) — поддерживающие клетки, служащие опорой для волосковых сенсорных клеток кортиева органа, а также для нервных окончаний у оснований волосковых клеток (ред.) (см. Улитка (внутреннего уха)).КЛЕТКИ ШВАННОВСКИЕ (Schwann cells) клетки глии… … Медицинские термины
Что такое шванновские клетки
К периферическим нервам относят черепные и спинномозговые нервы, соединяющие центральную нервную систему (ЦНС) с периферическими органами и тканями. Спинномозговые нервы формируются при слиянии вентральных (передних) и дорсальных (задних) нервных корешков в месте их выхода из позвоночного канала. Задние нервные корешки образуют утолщения — спинальные ганглии (или задние корешковые ганглии). Спинномозговые нервы относительно короткие — их длина составляет менее 1 см. Проходя через межпозвоночное отверстие, спинномозговые нервы делятся на вентральную (переднюю) и дорсальную (заднюю) ветви.
Задняя ветвь обеспечивает иннервацию мышц, выпрямляющих позвоночник, а также кожи туловища в этой области. Передняя ветвь иннервирует мышцы и кожу передней части туловища; кроме того, от нее отходят чувствительные волокна к париетальной плевре и париетальной брюшине.
Передняя ветвь также дает начало ветвям шейного, плечевого и пояснично-крестцового нервных сплетений. Таким образом, значение понятия «ветвь» может изменяться в зависимости от контекста. (Подробное описание нервных сплетений представлено в главах, посвященных анатомии.)
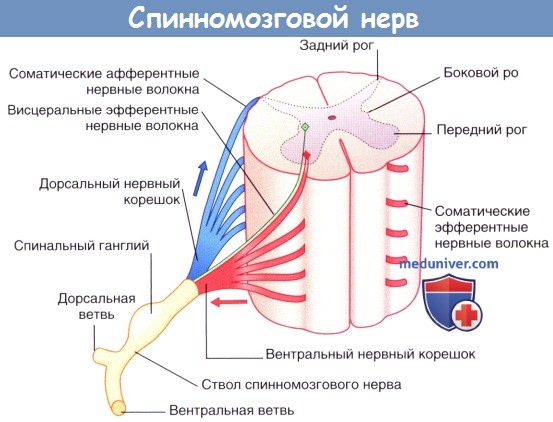
Стрелками указано направление проведения импульса. Зеленым цветом обозначено симпатическое нервное волокно.
Периферические нейроны частично расположены в ЦНС. Двигательные (эфферентные) нервные волокна, иннервирующие скелетную мускулатуру, начинаются от мультиполярных а- и у-нейронов, расположенных в переднем роге серого вещества. Строение этих нейронов соответствует общим принципам, характерным для мотонейронов. Более подробная информация представлена в отдельной статье на сайте. Задние нервные корешки берут начало от униполярных нейронов, тела которых расположены в спинальных ганглиях, а чувствительные (афферентные) центральные отростки входят в задний рог серого вещества спинного мозга.
В состав спинномозгового нерва входят соматические эфферентные нервные волокна, направляющиеся к скелетной мускулатуре туловища и конечностей, и соматические афферентные нервные волокна, проводящие возбуждение от кожи, мышц и суставов. Кроме того, в спинномозговом нерве расположены висцеральные эфферентные и, в некоторых случаях, афферентные вегетативные нервные волокна.
Общие принципы внутреннего строения периферических нервов схематично изображены на рисунке ниже. Только лишь по строению нервных волокон невозможно определить, являются они двигательными или чувствительными.
Периферические нервы окружены эпиневрием — внешним слоем, состоящим из плотной неравномерной соединительной ткани и располагающимся вокруг пучков нервных волокон и сосудов, кровоснабжающих нерв. Нервные волокна периферических нервов могут переходить из одного пучка в другой.
Каждый пучок нервных волокон покрыт периневрием, представленным несколькими отчетливо различимыми эпителиальными слоями, связанными плотными щелевидными соединениями. Отдельные шванновские клетки окружены эндоневрием, образованным ретикулярными коллагеновыми волокнами.
Менее половины нервных волокон покрыто миелиновой оболочкой. Немиелинизированные нервные волокна расположены в глубоких складках шванновских клеток.
Понятие «нервное волокно», как правило, применяют при описании проведения нервного импульса; в этом контексте оно заменяет термин «аксон». Миелинизированные нервные волокна представляют собой аксоны, окруженные концентрически расположенными слоями (пластинками) миелина, образованными плазматическими мембранами шванновских клеток. Немиелинизированные нервные волокна окружены отдельными немиелинизируюгцими шванновскими клетками; плазматическая мембрана этих клеток — нейролемма — одновременно покрывает несколько немиелинизированных нервных волокон (аксонов). Структура, образованная таким аксоном и шванновской клеткой, получила название «ганглий Ремака».
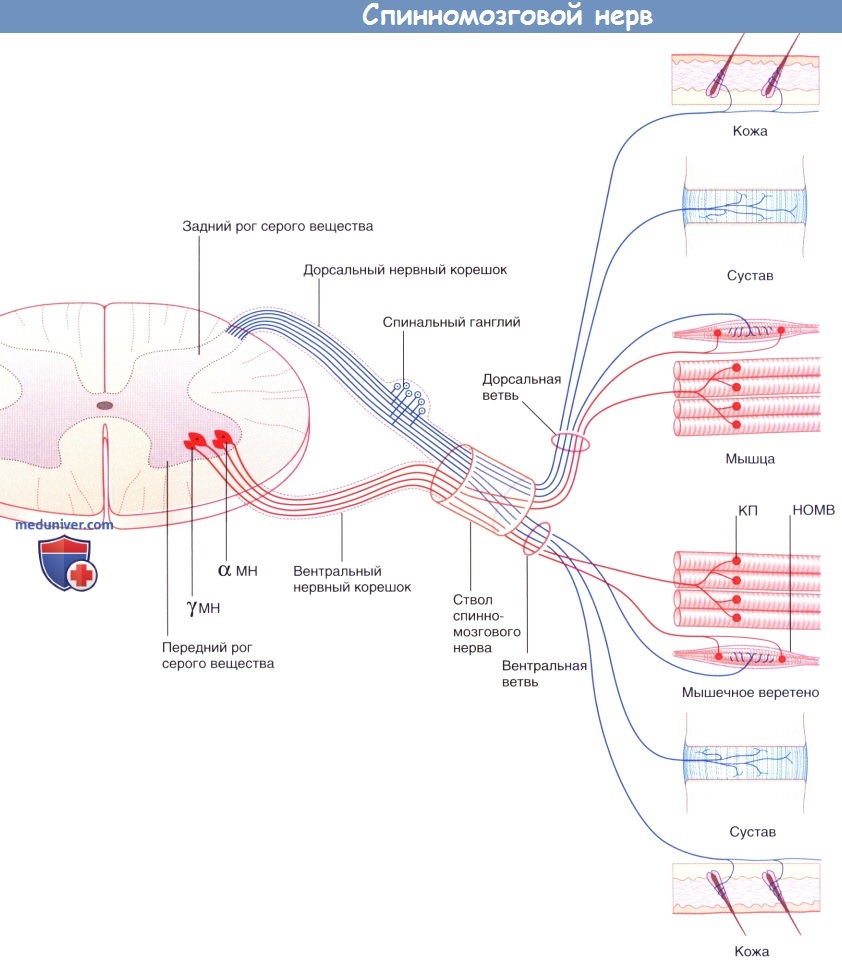
КП — концевая пластинка двигательного нерва на мышце; НОМВ — нервное окончание мышечного веретена; МН — мультиполярный нейрон.
а) Образование миелина. Шванновские клетки (леммоциты) — представители нейроглиальных клеток периферической нервной системы. Эти клетки образуют непрерывную цепочку вдоль периферических нервных волокон. Каждая шванновская клетка миелинизирует участок нервного волокна длиной от 0,3 до 1 мм. Видоизменяясь, шванновские клетки образуют в спинальных и вегетативных ганглиях сателлитные глиоциты, а в области нервно-мышечных соединений — клетки телоглии.
В процессе миелинизации аксона одновременно участвуют все окружающие его шванновские клетки. Каждая шванновская клетка оборачивается вокруг аксона, образуя «дупликатуру» плазматической мембраны,—мезаксон. Мезаксон поступательно смещается, накручиваясь на аксон. Последовательно формирующиеся слои плазматической мембраны располагаются друг напротив друга и, «вытесняя» цитоплазму, образуют главную (крупную) и межпромежуточную (мелкую) плотные линии миелиновой оболочки.
В области конечных участков миелинизированных сегментов аксона по обеим сторонам от перехватов Ранвье (промежутков между конечными участками соседних шванновских клеток) расположены паранодальные карманы.
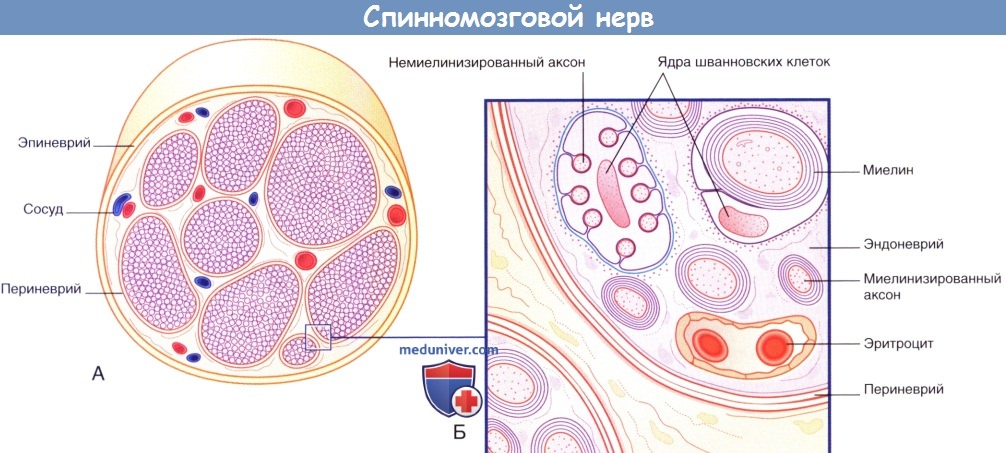
(А) Световая микроскопия. (Б) Электронная микроскопия. 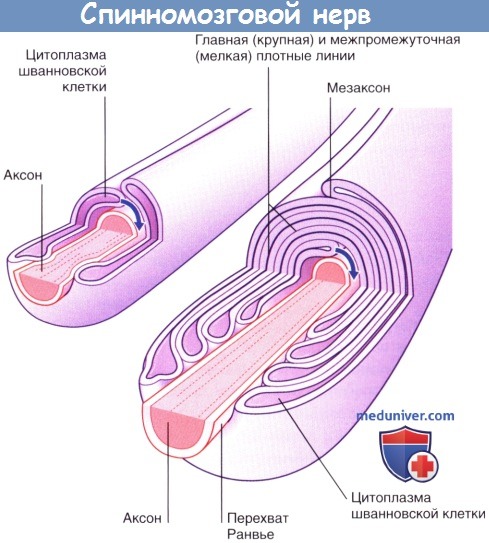
Стрелками указано направление накручивания цитоплазмы шванновской клетки.
1. Миелин ускоряет проведение импульсов. По аксонам немиелинизированных нервных волокон проведение импульса осуществляется непрерывно со скоростью около 2 м/с. Поскольку миелин выполняет функцию электроизолятора, возбудимая мембрана миелинизированных нервных волокон ограничена перехватами Ранвье. В связи с этим возбуждение распространяется от одного перехвата к другому сальтаторно — «скачкообразно», обеспечивая значительно большую скорость проведения нервного импульса, достигающую значений 120 м/с. Количество импульсов, проводимых за секунду, значительно выше у миелинизированных нервных волокон по сравнению с немиелинизированными.
Следует отметить, что чем крупнее миелинизированное нервное волокно, тем длиннее его межузловые сегменты, в связи с чем нервные импульсы, «делая большие шаги», распространяются с большей скоростью. Для описания зависимости между размером нервного волокна и скоростью проведения импульсов можно использовать «правило шести»: скорость распространения нервных импульсов по волокну, диаметр которого составляет 10 нм (включая толщину миелинового слоя), составляет 60 м/с, а по волокну диаметром 15 нм — 90 м/с и т. д.
С точки зрения физиологии периферические нервные волокна классифицируют по скорости проведения нервных импульсов, а также по другим критериям. Двигательные нервные волокна разделяют на типы А, В и С в соответствии с уменьшением скорости проведения импульсов. Чувствительные нервные волокна разделяют на группы I—IV по такому же принципу. Однако на практике эти классификации взаимозаменяемы: так, например, немиелинизированные чувствительные нервные волокна относят не к типу С, а к группе IV.
Подробная информация о диаметрах и местах локализации периферических нервных волокон представлена в таблицах ниже.
На электронно-микроскопическом изображении показаны миелинизированное периферическое нервное волокно и окружающая его шванновская клетка. На рисунках ниже представлена группа немиелинизированных нервных волокон, погруженных в цитоплазму шванновской клетки и продемонстрирован участок перехвата Ранвье аксона ЦНС.
б) Область перехода центральной нервной системы в периферическую нервную систему. В области моста мозга и спинного мозга периферические нервы входят в переходную зону между центральной и периферической нервной системой. Отростки астроцитов из ЦНС погружаются в эпиневрий корешков периферических нейронов и «переплетаются» со шванновскими клетками. Астроциты немиелинизированных волокон погружаются в пространство между аксонами и шванновскими клетками. Перехваты Ранвье миелинизированных нервных волокон в периферической части окружаются миелином шванновских клеток (демонстрируя некоторые переходные свойства), а в центральной части — миелином олигодендроцитов.
в) Резюме. Стволы спинномозговых нервов проходят в межпозвоночных отверстиях. Эти структуры образуются при соединении вентральных (двигательных) и дорсальных (чувствительных) нервных корешков и разделяются на смешанные вентральные и дорсальные ветви. Нервные сплетения конечностей представлены вентральными ветвями.
Периферические нервы покрыты эпиневральной соединительной тканью, пучковидной периневральной оболочкой и эндоневрием, образованным коллагеновыми волокнами и содержащим шванновские клетки. Миелинизированное нервное волокно включает аксон, миелиновую оболочку и цитоплазму шванновской клетки — нейролемму. Миелиновые оболочки формируются шванновскими клетками и обеспечивают сальтаторное проведение импульсов со скоростью, прямо пропорциональной диаметру нервного волокна.
Редактор: Искандер Милевски. Дата публикации: 12.11.2018
Опухоли шваннома
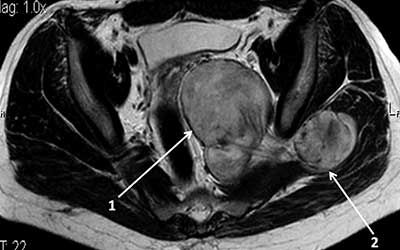
Шваннома является новообразованием доброкачественной природы, развивающимся из шванновских клеток. Последние формируют миелиновую оболочку нервных волокон и по неустановленным причинам способны начать слишком активное размножение, которое и приводит к появлению опухоли. Шваннома поражает разные нервы, однако чаще всего её диагностируют на слуховом. На её долю приходится 10% случаев церебральных, 20% спинномозговых и 50% опухолей периферических нервов.
Пройти хирургическое лечение шванномы в Москве приглашает отделение нейрохирургии ЦЭЛТ. Уже более 30-ти лет мы работаем на отечественном рынке платных медицинских услуг и располагаем всем необходимым для проведения лечения в соответствии с международными стандартами. Наши нейрохирурги имеют за плечами десятилетия опыта практической и научной работы и применяют эффективные щадящие методики.
Этиология шванномы
Несмотря на то, что учёным удалось установить связь между развитием шванномы и чрезмерно активным размножением шванновских клеток, причина последнего до сих пор не известна. Существует ряд теорий, согласно которым инициирующие факторы развития опухоли — следующие:
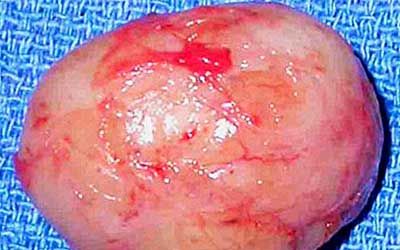
Новообразование растёт медленно и имеет вид круглого или овального узла с неровной поверхностью, покрытой капсулой. Внутри шванномы нередко обнаруживаются кисты разного размера, заполненные патологической жидкостью.
Клиника шванномы
Из-за медленного роста шванномы и практически полного отсутствия клинических проявлений, её обнаруживают достаточно поздно. Это происходит на том этапе, когда она начинает сдавливать соседние ткани, а поражённый нерв теряет способность нормально выполнять свои функции. Клиническая картина напрямую зависит от того, какой именно нерв повреждён:
Осложнения шванномы
Как уже упоминалось, часто шванному обнаруживают когда она уже выросла до внушительных размеров. Раннее диагностирование происходит, как правило, случайно: если пациент обращается к врачу по поводу другой проблемы. Своевременность лечения играет важную роль, поскольку позволяет исключить следующие осложнения:
Наши врачи
Диагностика и лечение шванномы в ЦЭЛТ
В нейрохирургии ЦЭЛТ работают кандидаты и доктора наук, врачи высшей категории, проводящие научную и практическую работы. Они располагают мощной диагностической базой, позволяющей точно ставить диагноз. Перед тем, как разработать тактику лечения шванномы, они проводят комплексную диагностику, позволяющая установить её размер, локализацию, влияние на окружающие ткани, кистозные изменения. Для этого назначают:
Пройти полное обследование и начать лечение можно в многофункциональной клинике ЦЭЛТ – последние достижения медицины на страже вашего здоровья.
Хотите узнать больше? Интересует стоимость удаления шванномы? Записывайтесь на приём к нашим специалистам и получайте ответы на любые вопросы: +7 (495) 788-33-88.
Шванновские клетки
Из Википедии — свободной энциклопедии
Шванновские клетки (леммоциты) — вспомогательные клетки нервной ткани, которые формируются вдоль аксонов периферических нервных волокон. Создают, а иногда и разрушают, электроизолирующую миелиновую оболочку нейронов. Выполняют опорную (поддерживают аксон) и трофическую (питают тело нейрона) функции, а также принимают участие в проведении возбуждения по нервным волокнам. Описаны немецким физиологом Теодором Шванном в 1838 году и названы в его честь.
Каждое периферическое нервное волокно одето тонким цитоплазматическим слоем — невролеммой или шванновской оболочкой. Волокно является миелинизированным, если между ним и цитоплазмой шванновской клетки имеется значительный слой миелина. Если волокна лишены миелина, то они называются немиелинизированными безмякотными. [1] Шванновские клетки могут осуществлять волнообразные движения, что, вероятно, способствует транспортировке различных веществ по отросткам нервных клеток.
С нарушением работы шванновских клеток связаны такие нервные заболевания, как синдром Гийена — Барре, болезнь Шарко — Мари — Тута, шванноматозис и хроническая воспалительная демиелинизирующая полинейропатия. Демиелинизация в основном происходит [2] из-за ослабления двигательных функций шванновских клеток, в результате чего они оказываются не способны образовывать миелиновую оболочку.
Журнал эволюционной биохимии и физиологии, 2019, T. 55, № 6, стр. 383-397
СОВРЕМЕННЫЕ ПРЕДСТАВЛЕНИЯ О ШВАННОВСКИХ КЛЕТКАХ: РАЗВИТИЕ, ПЛАСТИЧНОСТЬ, ФУНКЦИИ
ФГБНУ “Институт экспериментальной медицины”
Санкт-Петербург, Россия
Поступила в редакцию 16.12.2018
После доработки 19.03.2019
Принята к публикации 03.04.2019
В обзоре представлены данные о происхождении шванновских клеток, приведена фенотипическая характеристика их предшественников на разных стадиях онтогенеза, описаны функции шванновских клеток (SCs) согласно современным представлениям. Необходимость глубоких фундаментальных исследований SCs связана с разработкой новых способов стимуляции восстановления периферических нервных проводников, включая клеточную и генную терапию. Именно SCs, являясь основным структурным компонентом нерва, оказывают определяющее влияние на дегенеративные и репаративные процессы в нерве. Подчеркивается недостаток знаний о молекулярных механизмах, регулирующих дифференцировку SCs на разных этапах онтогенеза, и пластичность этих клеток при патологии нервных проводников.
ВВЕДЕНИЕ
Актуальность исследований морфофункциональных особенностей шванновских клеток (SCs) объясняется двумя причинами. Во-первых, в общебиологическом плане невозможно переоценить значение этих миелинобразующих клеток и самого процесса миелинизации для развития нервной системы. Во-вторых, необходимость глубоких фундаментальных знаний о закономерностях развития и механизмах функционирования SCs связана с разрабатываемыми в настоящее время способами стимуляции регенерации поврежденных нервных проводников.
Важное значение шванновских клеток, как клеток, осуществляющих миелинизацию нервных волокон, обусловлено высокой значимостью возникновения миелина в эволюции [1]. С его возникновением упростилась синхронизация мышечных сокращений, нервная система стала более компактной, появилась возможность более быстрой обработки сложной информации [2, 3]. Salzer и Zalc рассматривают миелинизацию аксонов как возникшую в эволюции адаптивную реакцию, способствующую развитию быстрой проводимости [4].
Одной из важнейших функций шванновских клеток является разделение (изоляция) соседних нервных волокон.
Вторая причина, обусловливающая важность изучения шванновских клеток, связана с необходимостью понимания молекулярно-клеточных механизмов восстановления поврежденных нервов. Изучению строения и регенерации периферических нервных проводников посвящено множество работ как отечественных, так и зарубежных авторов. Начало таким исследованиям было положено в XIX веке английским нейрофизиологом Августом Валлером (1816–1870) [5]. Комплекс процессов, которые происходят в дистальном конце нервного ствола после травмы нерва, был назван его именем – валлеровская дегенерация. Впоследствии многие исследователи, используя нейроморфологические, гистохимические, иммуногистохимические методы и электронную микроскопию, изучали клеточные взаимоотношения в поврежденном нерве. В классических исследованиях зарубежных и отечественных нейроморфологов показано, что основными структурными элементами, которые участвуют в дегенеративных и репаративных процессах в поврежденном нерве, являются моторные, вегетативные и чувствительные нейроны, отростки которых и составляют периферический нерв, шванновские клетки, макрофаги, клетки кровеносных сосудов и соединительнотканные элементы оболочек нерва [5–8].
Особый интерес к проблеме, касающейся молекулярных механизмов клеточных взаимоотношений структурных элементов периферических нервов в норме и после повреждения, возник в последние десятилетия. Это связано с разработкой клеточных и генных технологий, которые, как показано во многих работах и обобщено в нескольких обзорах [9–16], могут способствовать регенерации периферических нервных проводников после повреждения. Актуальность таких исследований связана с тем, что применяемые в микрохирургической практике способы лечения поврежденных нервов не всегда приводят к их полному функциональному восстановлению. Одной из причин является недостаток фундаментальных нейробиологических знаний, касающихся молекулярных механизмов регенерации нерва. Также нет полной ясности, каковы механизмы влияния пересаженных клеток (в том числе генетически модифицированных клеток со сверхэкспрессией ростовых факторов) на репаративные процессы в поврежденном нерве.
Учитывая важную эволюционную роль шванновских клеток, а также их значение для регенерации поврежденных нервных проводников, представляется важным обобщить имеющиеся в настоящее время данные о происхождении этих клеток, их морфофункциональных особенностях, развитии и дифференцировке, что и явилось целью настоящего обзора.
ШВАННОВСКИЕ КЛЕТКИ: МИЕЛИНИЗИРУЮЩИЕ И НЕМИЕЛИНИЗИРУЮЩИЕ
В середине XIX века немецкий физиолог Теодор Шванн впервые описал клетки, “обернутые вокруг аксонов периферической нервной системы” [17]. Эти клетки были названы его именем [18]. Следует отметить, что в ряде работ применяется еще один термин, обозначающий шванновские клетки, – “леммоциты”, введенный шведским невропатологом Nils Ragnar Eugene Antoni (1887–1968), изучавшим опухоли, характерные для оболочек нерва [19]. В трудах S. Ramon y Cajal глиальные элементы, описываемые автором в поврежденном нерве, называются “клетками Шванна” и “леммобластами” [6]. Термины “леммоцит” и “леммобласт” и сейчас используются отдельными авторами [8, 20]. По мнению Ноздрачева и Чумасова [8], леммобласты являются одной из стадий развития шванновских клеток и отличаются от более ранних предшественников способностью образовывать базальную пластинку. Следует отметить, что в современной отечественной гистологической номенклатере в качестве синонима “шванновской клетки” предложен термин “нейролеммоцит” [21].
Шванновские клетки (SCs) делятся на две группы: миелинизирующие и немиелинизирующие клетки. И те, и другие играют ключевую роль в поддержании трофики и регенерации аксонов нейронов в ПНС. Большинство периферических нервных проводников позвоночных животных миелинизированы. Немиелинизированными являются аксоны малого калибра. Следует отметить, что и в ЦНС, где в качестве миелинизирующих клеток выступают олигодендроциты, аксоны некоторых нейронов остаются немиелинизованными, например, тонкие аксоны клеток-зерен мозжечка, поднимающиеся в молекулярный слой коры мозжечка и ветвящиеся в нем [22].
Вопрос о том, к какой группе будут относиться шванновские клетки: к миелинизирующим или немиелинизирующим, определяется в эмбриогенезе на стадии незрелых шванновских клеток [23]. В настоящее время многие сигнальные пути, регулирующие развитие SCs и процесс миелинизации, изучены [1]. Считается, что вопрос о том, будет ли аксон миелинизироваться, зависит от типа аксона, с которым соседствуют предшественники, а также от микроокружения (белков экстрацеллюлярного матрикса, главным образом, ламинина). Основная роль отводится нейрегулину 1 третьего типа (NRG1-III). Аксонами большого диаметра вырабатывается высокий уровень NRG1-III, что способствует дифференцировке предшественников в миелинизирующие шванновские клетки. При этом одна клетка миелинизирует одно волокно. Для аксонов малого диаметра характерен низкий уровень секреции нейрегулина, это приводит к тому, что клетки-предшественники дифференцируются в направлении немиелинизирующих шванновских клеток [23–26]. В то же время NRG1-III необходим для дифференцировки как миелинизирующих, так и немиелинизирующих SCs [27]. Таким образом, в дополнение к уже изученным сигнальным путям в будущем предстоит выяснить, какие другие внешние сигналы управляют процессами развития SCs и миелинизации. Неизвестно, имеются ли негативные сигналы на немиелинизированных нервных волокнах, которые препятствуют миелинизации [27]. Еще предстоит выяснить, каково влияние не только аксональных сигналов, но и влияние других типов клеток (эндотелия, фибробластов) на дифференцировку SCs в онтогенезе [27].
Немиелинизирующие шванновские клетки имеют ряд отличительных морфологических особенностей по сравнению с миелинизирующими. Во-первых, они располагаются вдоль аксонов на более близком расстоянии друг от друга, во-вторых, они, как правило, находятся в контакте более чем с одним аксоном [27, 28]. Такие клетки окружают несколько тонких (диаметром менее 1 мкм) аксонов (без формирования миелиновой оболочки), образуя структуру, называемую пучок Ремака (“Remak bundle”). В ПНС имеется несколько классов немиелинизированных нервных волокон: ноцицепторные С-волокна, постганглионарные симпатические и парасимпатические волокна и терминальные окончания двигательных нервов в нервно-мышечных синапсах [27, 29]. Немиелинизирующие шванновские клетки входят в состав телец Пачини и чувствительных телец Мейснера [29]. Немиелинизирующие шванновские клетки, которые связаны с аксонами малого калибра, называют ремаковскими (“Remak SC” [30]). При иннервации кожи, когда ремаковские нервные волокна доходят до эпидермиса, их SCs достигают соотношения 1 шванновская клетка: 1 аксон. В дальнейшем эти волокна теряют контакт со шванновскими клетками, и только аксоны проникают в эпидермис. В отличие от миелинизированных аксонов, эти волокна характеризуются непрерывным ростом, который находится под контролем фактора роста нервов, выделяемого немиелинизирующими шванновскими клетками [30].
Немиелинизирующие шванновские клетки, которые связаны с аксонами в нервно-мышечных контактах, называют терминальными или перисинаптическими шванновскими клетками [31, 32]. Осуществляют ли терминальные шванновские клетки трофическую функцию по отношению к аксонам, как это делают ремаковские SCs, неизвестно. Предположительно они участвуют в процессе синаптогенеза во время развития, а также в реиннервации нервных волокон после травмы [27, 33, 34].
ПРОИСХОЖДЕНИЕ ШВАННОВСКИХ КЛЕТОК В ЭМБРИОГЕНЕЗЕ
Шванновские клетки происходят в эмбриогенезе из нервного гребня, закладки, которая образуется во время замыкания нервной трубки и располагается в виде тяжей с двух сторон от нее. Из мигрирующих мультипотентных клеток нервного гребня, наряду со шванновскими клетками, образуются периферические нейроны, меланоциты, нейроэндокринные клетки и др. [обзоры: 18, 25, 23, 35, 36].
После процесса миграции клетки нервного гребня проходят несколько стадий дифференцировки в направлении шванновских клеток: предшественники (SCPs), незрелые шванновские клетки (iSCs), немиелинизирующие шванновские клетки (pro-mSCs) и, наконец, дифференцированные, среди которых одни миелинизируют аксоны, другие нет (mSCs и nmSCs) [23, 25]. Описание особенностей шванновских клеток и их фенотипа на разных этапах развития обобщены в табл. 1.
Таблица 1.
Характеристика шванновских клеток на разных стадиях дифференцировки
| Стадия дифференцировки | Характеристика | Маркеры | Источ-ник |
|---|---|---|---|
| Предшественник шванновской клетки, Schwann cell precursor (SCP) | Как и клетки нервного гребня, являются мигрирующими и способны к пролиферации. Их жизнеспособность зависит от сигналов, исходящих от растущих аксонов. SCP перемещаются вместе с развивающимися аксонами. Регулятор развития NRG1. Активация NRG1 ErbB2/3 имеет важное значение как для пролиферации SCP, так и для направленной миграции. | Sox10, GAP43, Oct6, Sox2, MPZ | [23, 27, 37] |
| Незрелая шванновская клетка, immature Schwann cell (iSC) | Образуются из SCP и перестают мигрировать. Формируют базальную мембрану. Выживание iSC не зависит от аксональных факторов. В период их дифференцировки в нервах начинают формироваться сосуды и фибробласты, в экстрацеллюлярном матриксе появляется коллаген. Возникает периневральная оболочка. Механизмы, регулирующие этот этап дифференцировки, не вполне изучены, предполагается участие сигнального пути Notch. | Sox10, S100, GAP43, P75NTR, NCAM, Sox2, Oct6, MPZ GFAP, O4 | [23, 27, 37] |
| Стадия промиелинизации, pro-myelin Schwann cell (pro-mSC) | Возникают на стадии, когда достигается соотношение 1 шванновская клетка: 1 аксон. Когда все аксоны большого калибра отделены. Pro-mSC образуют собственную базальную мембрану. Те незрелые SCs, которые охватывают оставшиеся аксоны небольшого калибра, дифференцируются в Remak SCs. | Sox10, S100, Krox20, Oct6 | [27, 37] |
| Немиелинизирующая шванновская клетка, non-myelinating Schwann cell (nmSC) | Немиелинизирующие шванновские клетки окружают малые сенсорные и вегетативные аксоны ПНС, формируя классическое ремаковское волокно. Они сохраняют свои пролиферативные потенции. Терминальные шванновские клетки. Шванновские клетки телец Пачини и Мейснера. | Sox10, S100, GAP43, P75NTR, NCAM, Oct6 Egr-1, GFAP и AN2/ NG2 | [27, 28, 37] |
| Миелинизирующая шванновская клетка, myelinating Schwann cell (mSC) | Шванновские клетки, образующие миелиновые оболочки нервных волокон большинства нервов. | Sox10, S100, Krox20, Oct6, MBP, MPZ P0/Pmp22/MAG/MBR | [18, 37] |
Предшественники шванновских клеток отличаются от клеток нервного гребня тем, что уже находятся в тесной связи с аксонами. Есть данные, что они являются мультипотентными клетками и способны дифференцироваться не только в шванновские клетки, но и в эндоневральные фибробласты и ряд других типов клеток [23, 25]. Описывая эти клетки, авторы [23, 25] проводят параллель с клетками радиальной глии в развивающейся ЦНС, которые, являясь нейральными стволовыми клетками, мультипотентны и дают начало нейронам, астроцитам, эпендимным клеткам и олигодендроцитам. Молекулярный механизм дифференцировки клеток нервного гребня в предшественники шванновских клеток мало изучен. Имеются лишь отдельные данные о том, что в этом процессе участвует сигнальная система Notch [23]. Описана интересная особенность предшественников шванновских клеток при их культивировании: в отсутствие аксонов они погибают.
Фенотипические характеристики шванновских клеток различаются в зависимости от стадии их развития в онтогенезе. Маркеры шванновских клеток на разных этапах развития изучены не только in vivo, но и in vitro. Liu et al. (2015) [37] с помощью иммунофлуоресценции, вестерн-блот анализа и количественной полимеразной цепной реакции в реальном времени изучали специфические маркеры шванновских клеток новорожденных мышей. Исследования проводились на культуре шванновских клеток. Были выявлены десять маркеров, свойственных шванновским клеткам in vivo: S100, p75NTR, Sox10, Sox2, GAP43, NCAM, Krox20, Oct6, MBP и MPZ. На всех стадиях развития были обнаружены только транскрипционные факторы Sox10 и Sox2. Через 8 сут культивирования появлялись все маркеры, кроме GAP43 и Oct6. Было обнаружено, что широко используемые маркеры S100 и P75NTR не были выражены на ранней стадии культивируемых SCs.
Механизмы, контролирующие дифференцировку незрелых шванновских клеток в немиелинизирующие, мало изучены. Есть данные, что в этом процессе участвует белок внеклеточного матрикса – ламинин. Используя линию мутантных мышей, лишенных ламинина, Yu et al. (2009) [27, 28] показали, что необходимым стимулом для дифференцировки шванновских клеток является именно этот белок.
Незрелые шванновские клетки (iSCs) выполняют важные гистогенетические функции. Во-первых, они отделяют аксоны большого калибра, которые впоследствии станут миелинизированными, от немиелинизированных волокон малого калибра. Во-вторых, они вырабатывают трофические факторы, стимулирующие дифференцировку таких структурных элементов нерва, как периневральные клетки, клетки кровеносных сосудов, фибробласты эндоневрия и эпиневрия [27].
ФУНКЦИИ ШВАННОВСКИХ КЛЕТОК И ИХ ПРЕДШЕСТВЕННИКОВ
Миелинизация периферических нервных волокон
В процессе эволюции для увеличения скорости проводимости нервного импульса развивалось два механизма: первый связан с увеличением диаметра аксона, второй – с возникновением миелиновой оболочки [38]. Миелинизация позволила увеличить скорость проводимости аксонов малого калибра. Миелиновые нервные волокна имеются у большинства позвоночных животных. Они появляются в филогенезе у хрящевых рыб. Миелин акул и скатов устроен, как и у других позвоночных: нервные волокна покрыты базальной пластинкой, окружены коллагеном, имеют много насечек Штидта–Лантермана и перехваты Ранвье. Установлено, что как и у других позвоночных, для миелиновых оболочек хрящевых рыб свойственны миелинпротеины P0, MPZ и основной белок миелина (MBP) [39].
Что касается беспозвоночных животных, у представителей различных таксонов описан миелин разного уровня развития. У одних – плотные миелиновые оболочки, у других – “голые” нейриты, обернутые несколькими мембранами глиальных клеток [38, 40]. Так, у отдельных представителей ракообразных (крабы и омары), а также у моллюсков и насекомых миелиновые оболочки не описаны. Изолирующую аксоны функцию здесь выполняют немиелинизирующие глиальные клетки и соединительнотканные элементы. У тех представителей ракообразных, которым свойственны миелиновые оболочки, например, у планктонных рачков Copepoda, миелин имеет сходную структуру c таковой у позвоночных животных [41]. Их миелин характеризуется концентрически расположенными слоями мембраны вокруг аксона. Количество слоев в оболочке изменяется для каждого аксона, варьируя от одного до пятидесяти и более. Высокоорганизованные пластинки плотно обернуты вокруг заполненного микротрубочками аксона. Оболочка состоит из электронноплотных слоев одинаковой толщины, которые чередуются с менее плотными слоями большей толщины [41]. Такое сходство миелина позвоночных и беспозвоночных животных связано с идентичной функцией миелинизирующих клеток.
Вопрос о том, какие именно условия среды привели к появлению миелина у беспозвоночных животных, до сих пор не находит четкого объяснения [38]. Предположительно увеличение скорости проведения нервного импульса актуально для тех животных, которым необходимо, скрываясь от хищников, или, наоборот, догоняя жертву, развивать большую скорость движения [4, 38]. Подтверждением этой гипотезы является тот факт, что ареал обитания копепод, обладающих миелинизированными волокнами, занимает большую территорию, чем ареал обитания копепод, не имеющих миелинизированных волокон. Дискуссионным до сих пор является вопрос о том, где первоначально в филогенезе появился миелин и миелинобразующие клетки: в центральной или периферической нервной системе [42]. Некоторые исследователи считают, что SCs ПНС и олигодендроглия ЦНС имеют в эволюции общего предшественника [2]. Однако между этими типами клеток множество различий. Например, различное эмбриональное происхождение: олигодендроциты в эмбриогенезе происходят из нейроэктодермы, а шванновские клетки – из нервного гребня. Между процессами миелинизации, проходящими по центральному и периферическому типу, также много отличий. Их регулируют различные транскрипционные каскады: Sox10, Olig1/2, MYRF для олигодендроглии и Sox10, Pou3F1, Egr2 для шванновских клеток. Кроме того, как известно, у миелинизирующих клеток ЦНС и ПНС разные механизмы “упаковки” миелина. Предполагается, что появление миелиновых структур в центральной и периферической нервной системе происходило параллельно. Высказывается также мнение, что миелин появлялся в эволюции несколько раз [4]. Имеются палеонтологические данные о том, что первыми позвоночными животными, которые имели миелиновые нервные волокна, были панцирные рыбы [2, 3, 38].
В настоящее время активно изучаются молекулярные механизмы регуляции процесса миелинизации периферических нервных проводников с применением различных моделей исследования. Среди них культивирование нейронов и шванновских клеток in vitro, модели с применением трансгенных животных, модели повреждения нервов и др. [43].
Считается, что толщина миелиновой оболочки нервного волокна зависит от его диаметра [8, 22]. В процессе формирования миелиновой оболочки необходимой толщины ключевую роль играет передача сигналов NRG1 через рецепторы ErbB [43–45]. NRG1-сигнализация необходима шванновским клеткам для экспрессии структурных компонентов цитоплазматической мембраны и осуществления нужного количества обвертываний вокруг аксона. На моделях с применением трансгенных животных показано, что в отсутствие NRG1-III миелинизации не происходит [18]. Доказательством значения NRG1 для осуществления миелинизации служит тот факт, что немиелинизирующиеся в норме отростки симпатических нейронов становятся миелинизированными в условиях in vitro, если такие нейроны обладают сверхэкспрессией NRG1 [24].
Трофическая функция шванновских клеток
Осуществление трофической функции миелинизирующих клеток (олигодендроцитов или SCs) по отношению к нервной клетке и ее аксону ранее отмечалось многими авторами [1, 8, 22, 46], однако в наши дни при использовании современных методов исследования получены дополнительные данные о влиянии глиальных клеток как ЦНС, так и ПНС, на метаболизм аксонов. Так, показано, что олигодендроциты синтезируют лактат для аксонов и тем самым предотвращают их дегенерацию [47]. Установлено, что нарушение функции митохондрий в SCs вызывает прогрессирующую дегенерацию миелинизированных аксонов [48]. Важная роль в метаболизме аксонов отводится и немиелинизирующим шванновским клеткам [27, 48].
Исследования взаимоотношений шванновских клеток и аксонов показали, что между ними может осуществляться обмен органоидами. Имеются данные о том, что рибосомы могут переноситься от SC к аксону при повреждении и в процессе развития [1]. Эксперименты, доказывающие перенос полирибосом из SCs в аксоны, были выполнены с использованием зеленого флуоресцентного белка на моделях in vitro и in vivo. Рибосомы SCs были помечены зеленым флуоресцентным белком. После проникновения в аксон меченые рибосомы можно было наблюдать в течение нескольких недель, где они предположительно участвовали в местном синтезе белка [49]. Высказывается также мнение, что в нервах в области перехватов Ранвье или насечек Шмидта-Лантермана может осуществляться процесс переноса РНК от SCs в аксоны [50].
Для ПНС трофическая функция глиальных клеток имеет особое значение, поскольку периферические нервы достигают значительной длины, а транспорт метаболитов из тела нейрона осуществляется медленно (по сравнению с транспортом везикул), их скорость составляет 300 мкм в час [4].
Обмен генетической информацией с аксоном путем высвобождения экзосом
Экзосомы и микровезикулы представляют собой внеклеточные нанопузырьки, высвобождаемые многими клетками [51]. С их помощью осуществляются межклеточные взаимодействия путем передачи генетической информации, включая передачу как кодирующих, так и некодирующих РНК, в клетки-реципиенты. Экзосомы достигают размеров 10–100 нм. Показано, что экзосомы способны переносить фрагменты матричной РНК (мРНК) и микроРНК (miRNA) из клетки в клетку [15, 51]. Изучая взаимоотношения между шванновской клеткой и аксоном, многие авторы показали, что экзосомы, высвобождаемые SCs, влияют на регенерацию поврежденных аксонов. В обзорах [50] и [52] дана характеристика экзосом и описаны механизмы их образования и значение в аксон-глиальных взаимоотношениях.
В модельных экспериментах, выполненных in vitro, показано, что экзосомы шванновских клеток усваиваются аксонами периферических нервов, и это приводит к стимуляции роста нейритов [52]. Установлено, что этот эффект специфичен для экзосом, полученных именно из шванновских клеток. Доказательством служит тот факт, что экзосомы, синтезируемые не SCs, а фибробластами, не оказывают такого влияния. Стимулирующее влияние экзосом шванновских клеток на рост аксонов подтверждено и в экспериментах in vivo. Показано, что ежедневные инъекции экзосом в дистальный сегмент поврежденного нерва приводят к двукратному увеличению скорости роста аксонов.
Предполагается, что экзосомы могут участвовать в регуляции валлеровской дегенерации [50]. Известно, что экзосомы способны модулировать фенотип клеток путем переноса мРНК, miRNAs и факторов транскрипции белков в различных органах [51]. Это позволяет предполагать, что с их помощью осуществляется переключение фенотипа SCs с миелинизирующего зрелого на немиелинизирующий при дедифференцировке.
Синтез биологически активных веществ
Шванновские клетки оказывают влияние на нервные клетки, вырабатывая нейротрофические факторы, цитокины и белки экстрацеллюлярного матрикса. Установлено, что они оказывают поддерживающее влияние на развивающиеся нейроны, пока их аксоны еще не достигли органов-мишеней [44]. Так, у трансгенных мышей с дефицитом ErbB3 (т.е. в отсутствие предшественников SCs) двигательные нейроны спинного мозга и чувствительные нейроны спинномозговых ганглиев погибают по механизму апоптоза [44].
После травмирования периферического нервного проводника и повреждения аксона SCs оказывают поддерживающее влияние на нейроны, вырабатывая ряд биологически активных веществ: фактор роста нервов (NGF), фактор роста фибро-бластов (FGF), нейротрофический фактор головного мозга (BDNF), инсулиноподобный фактор роста (IGF), глиальный нейротрофический фактор (GDNF), нейротрофин 4/5, нейротрофин 3(NT-3), цилиарный нейротрофический фактор, нейрональный белок клеточной адгезии (NCAM) и др. [15, 53–56]. Доказательства необходимости этих факторов для сохранения жизнеспособности нейронов и их дифференцировки были получены на моделях с использованием трансгенных животных. Нарушение синтеза этих биологически активных веществ шванновскими клетками может приводить к неврологическим заболеваниям и нарушению регенерации нервов.
Известно, что после повреждения нерва наблюдается дедифференцировка шванновских клеток. Дедифференцированные SCs обретают свойство синтезировать ряд белков внеклеточного матрикса (ламинина, фибронектина, тенасцина и др.), которые участвуют в стимуляции регенерации аксонов [15, 27, 55]. Они секретируют также хемокины и цитокины, необходимые для привлечения в нерв моноцитов/макрофагов. Среди них MCP-1 (моноцитарный хемоаттрактантный белок-1), LIF (leukemia inhibitory factor), PAP-III (панкреатит-ассоциированный белок III) и интерлейкины IL-1α и IL-1β [57–59].
Шванновские клетки способны синтезировать вещества, участвующие в регуляции морфогенетических процессов, происходящих в нерве. Во-первых, они вырабатывают белок, который контролирует образование периневрия – dhh (“desert hedgehog”) во время развития нерва [60]. Периневрий – одна из оболочек нервного ствола, которая обеспечивает периневральный барьер, предотвращающий доступ в эндоневрий инфекционных агентов. Во-вторых, предшественники шванновских клеток, ассоциированные с определенными нервами в период эмбриогенеза, способны секретировать фактор роста эндотелия сосудов (VEGF-A), способствуя тем самым процессам васкуло- и ангиогенеза в развивающемся нерве [61].
Таким образом, благодаря способности вырабатывать ряд биологически активных веществ SCs оказывают трофическую поддержку развивающимся нейронам, пока их аксоны еще не достигли мишеней, поддерживают жизнеспособность нервных клеток и целостность нервного ствола после травмы нерва, а также участвуют в морфогенезе.
Участие в фагоцитозе продуктов распада миелина при валлеровской дегенерации
С появлением иммуногистохимических методов идентификации шванновских клеток и макрофагов удалось установить, что в удалении продуктов распада миелина участвуют и одни, и другие клетки [62]. В настоящее время не вызывает сомнения тот факт, что в течение первых суток после травмы нерва функцию уборки продуктов распада миелина в его дистальном конце выполняют шванновские клетки, а для окончательного очищения эндоневрия от миелина необходимо подключение макрофагов [22, 62, 66]. В современных работах механизм устранения продуктов распада миелина шванновскими клетками пересматривается. Высказывается мнение, что этим механизмом не может быть фагоцитоз, поскольку при фагоцитозе поглощаются вещества, находящиеся вне клетки-фагоцита. Миелиновая оболочка же является внутренним компонентом SC, ее частью. В связи с этим предполагается, что механизм поглощения продуктов распада миелина шванновскими клетками – макроавтофагия [67, 68]. Макроавтофагия является системой деградации, при которой клетки разрушают свои собственные органеллы и крупные макромолекулы. Gomez‑Sanchez et al. (2015) [67] показали, что после повреждения нервного ствола в нем наблюдается активация аутофагии SCs, фомируются аутофагосомы, содержащие продукты распада миелина. Авторы, наблюдая аутофагию миелиновой оболочки SC, предложили для этого процесса термин “миелинофагия”. На экспериментальных моделях показано, что генетическое и фармакологическое ингибирование аутофагии приводит к ингибированию разрушения белков и липидов миелина в поврежденном нерве.
ПЛАСТИЧНОСТЬ ШВАННОВСКИХ КЛЕТОК
О проявлении фенотипической пластичности шванновских клеток принято говорить, когда происходит нарушение взаимодействия SCs с аксоном вследствие повреждения. Это нарушение приводит к дедифференцировке как миелинизирующих, так и немиелинизирующих шванновских клеток в незрелые формы.
После травмирования нерва зрелые шванновские клетки получают сигнал от поврежденного аксона через систему NRG/Erg2 и меняют свой фенотип [22]. Показано, что Erg2 активируется в течение нескольких минут после травмы нервного волокна, а в течение последующих двух суток после потери контакта с аксоном шванновские клетки дедифференцируются [22]. Дедифференцированные клетки способны к миграции и пролиферации. Вследствие своего деления они формируют в дистальном сегменте травмированного нерва так называемые “бюнгнеровские ленты” – пути, по которым осуществляется рост регенерирующих аксонов. Кроме того, они начинают синтезировать противовоспалительные цитокины и хемокины, стимулирующие инфильтрацию макрофагов [59, 69]. Когда вследствие регенерации контакт с аксоном восстанавливается, эти клетки вновь становятся миелинирующими или немиелинирующими в зависимости от сигнала, исходящего от регенерирующего аксона [18]. В регуляции процессов дедифференцировки, пролиферации SCs и последующей ремиелинизации регенерирующих аксонов участвуют белки внеклеточного матрикса, нейтрофические факторы и гормоны [55]. Дедифференцированные шванновские клетки (клетки, формирующие “бюнгнеровские ленты” в дистальном конце травмированного нерва) приобретают свойства незрелых SCs [70]. В исследованиях 2017 г. показано, что у них также имеются специфические черты, отличные от других клеток в линии SCs. Gomez-Sanchez с коллегами [71] показали, что повреждение седалищных нервов у мышей приводит к изменению как структуры, так и функции SCs. Эти клетки принимают удлиненную форму и образуют отростки. Показано, что образующие “бюнгнеровские ленты” клетки в 2–3 раза длиннее миелинизирующих и ремаковских шванновских клеток и в 7‒10 раз больше незрелых форм [71]. Примечательно, что когда эти клетки трансформируются обратно в миелинирующие клетки, их размер уменьшается. Еще одной особенностью дедифференцированных шванновских клеток является их способность оказывать стимулирующее влияние на репаративные процессы в разных тканях [72].
Недавно показано, что предшественники шванновских клеток и клетки, формирующие “бюнгнеровские ленты”, проявляют свойство мультипотентности. Так, в исследовании, выполненном на модели восстановления резцов у мышей, установлено, что SCs генерируют клетки, из которых образуются клетки пульпы и одонтобласты [73]. Экспериментально подтверждена возможность дифференцировки предшественников шванновских клеток в меланоциты, клетки парасимпатических ганглиев нервной системы, мезенхимальные стволовые клетки пульпы зуба [74]. Было продемонстрировано, что предшественники шванновских клеток в условиях in vitro в присутствии FGF-2 и эпидермального фактора роста могут быть перепрограммированы в мультипотентные клетки, которые способны генерировать клетки, подобные нейронам, глиоцитам и гладкомышечным клеткам [75]. Uesaka et al. (2015) [76] показали, что вегетативные нейроны энтеральной нервной системы могут формироваться не только из клеток нервного гребня, но и из клеток-предшественников шванновских клеток.
РЕГЕНЕРАЦИЯ НЕРВА, ПАТОЛОГИЧЕСКАЯ ПРОЛИФЕРАЦИЯ ШВАННОВСКИХ КЛЕТОК И ДЕМИЕЛИНИЗИРУЮЩИЕ ПРОЦЕССЫ
Изучение патологии нервных проводников, связанные с участием шванновских клеток (травма нерва, демиелинизирующие расстройства, опухоли и др.), может пролить свет на молекулярные механизмы регуляции дифференцировки SCs и их взаимоотношения с окружающими тканями. После механической травмы нерва, которая может наступать при переломах, ушибах, сдавливании близлежащей опухолью и др., SCs дедифференцируются и участвуют в репаративных процессах и ремиелинизации. Однако часто нарушение последовательности и стройности этих процессов приводит к необратимым изменениям, которые необходимо учитывать при хирургическом лечении [15, 20]. В результате травмы периферического нервного проводника нередко возникает неврома, которая препятствует нормальной репаративной регенерации нерва. Показано, что невромы различных размеров могут возникать на проксимальном конце поврежденного нервного ствола, сбоку от него и внутри ствола [7, 8]. Неврома состоит из большого числа миелинизированных и немиелинизированных нервных волокон, периневральных футляров, эндоневральных фибробластов, шванновских клеток, коллагеновых пучков соединительной ткани, нередко в ней встречаются кровоизлияния и воспалительные инфильтраты [8]. Показано, что в невроме длительное время продолжаются процессы роста аксонов, миелинизиции, ангиогенеза, а также пролиферация шванновских клеток и фибро-бластов, увеличение числа макрофагов и тучных клеток [22]. Надо отметить, что морфофункциональные особенности шванновских клеток невромы сходны с нормальными SCs в регенерирующем нерве. Неврому в эксперименте можно использовать для изучения взаимоотношений клеточных элементов, составляющих нерв.
К демиелинизирующим заболеваниям относятся рассеянный склероз, болезнь Шарко-Мари-Тута и синдром Гийена-Барре [18]. Болезнь Шарко-Мари-Тута является наследственным заболеванием и связана с дефектами ключевых миелинизирующих генов. Синдром Гийена-Барре по своим проявлениям является аутоиммунным расстройством. Демиелинизацию в нервной системе вызывает также Mycobacterium leprae, которые заражают SCs при проказе. Рецептор шванновских клеток альфа-дистрогликан является сайтом связывания для M. leprae. Как только бактерии проникают внутрь клетки, М. leprae включаются в MAPKcascade для демиелинизации нервов и способствуют пролиферации SCs. В результате наблюдается увеличение количества инфицированных клеток [77].
Среди опухолей нервных проводников различают доброкачественные (шваннома, нейрофиброма, периневрома, травматическая неврома) и злокачественные (злокачественная опухоль периферической нервной оболочки (malignant peripheral nerve sheath tumor (MPNST)) [78]. Шванномы возникают из миелинизирующих шванновских клеток и практически полностью состоят из этих клеток. Нейрофибромы содержат все клеточные элементы периферического нерва, включая SCs, фибробласты, периневриальные клетки и аксоны [78]. Различают нейрофиброматоз 1 типа (синдром Реклингхаузена) (NF1) и нейрофиброматоз 2 типа (NF2). Это аутосомно-доминантные наследственные заболевания. Опухоли в NF1 являются нейрофибромами и состоят из смеси фибробластов, шванновских клеток, периневриальных клеток и тучных клеток [18]. Нейрофибромы иногда перерождаются в злокачественные опухоли периферических нервных оболочек (MPNSTs или нейрофибросаркомы) [18].
Исследование патологии нервных стволов, в частности формирующихся в них опухолей, позволяет изучать молекулярные механизмы регуляции тканевого гомеостаза в нерве. Так, было выявлено, что одна из изоформ нейрегулина участвует в развитии нейрофибромы [79]. В отличие от нейрегулина III-1a, который ответственен за формирование миелиновых волокон и за толщину миелиновой оболочки, тип нейрегулина III-3 не влияет на толщину миелиновой оболочки. Используя трансгенных животных, показано, что сверхэкспрессия этого белка у мышей приводит к увеличению размеров ганглиев и нервов. При этом они приобретают признаки нейрофиброматоза I типа, о чем свидетельствует увеличение коллагеновых волокон и количества шванновских клеток. При этом отмечается резкое изменение ремаковских пучков: ремаковские шванновские клетки перестают отделять аксоны малого калибра друг от друга. Вместо этого аксоны плотно упакованы, и весь пучок обернут SCs как единое целое. Гиперпролиферация SCs и нарушение разделения аксонов в цитоплазме ремаковских шванновских клеток также являются ранними признаками NF1 [79]. Полученные данные, по мнению авторов, подтверждают тот факт, что устойчивая активация немиелинизирующих шванновских клеток нейрегулином, вырабатываемым аксоном, может способствовать возникновению опухоли в ремаковских комплексах. Это указывает на то, что ингибирование сигнальной передачи аксонов может служить в качестве предполагаемой терапии для лечения опухолей ПНС [79].
В трех заболеваниях, связанных с пролиферацией SCs: проказа, NF1 и NF2, участвует MAP-киназный каскад. Предполагается, что этот сигнальный путь играет центральную роль в распространении заболевания по организму, поэтому некоторые исследователи считают, что именно в этом направлении следует осуществлять поиск терапии этих заболеваний [18] (наряду с антимикробной терапией, если это касается проказы). Из плексиформной нейрофибромы, реже из шванномы [80], может развиваться MPNST. Клеточные и молекулярные особенности шванном были описаны в 1920 г. шведским невропатологом Nils Ragnar Eugene Antoni [78]. Он описал два типа шванном, отличающихся по своей гистологии. В обзоре Wippold et al. (2007) [78] охарактеризованы оба типа опухолевой ткани, носящие название Antoni A и B. Ткань типа А является многоклеточной и содержит ламинин, ткань типа B состоит из большого числа кистозных образований, кровеносных сосудов, областей некроза. Для шванном типа А характерно высокое содержание белков базальных мембран: ламинина и коллагена IV. Как известно, высокомолекулярный гликопротеин ламинин вырабатывается шванновскими клетками на всех стадиях развития. Именно он является маркером, с помощью которого можно дифференцировать опухоли, полученные из SCs, и отличать их от гистиоцитомы и фибросаркомы [78]. Второй, свойственный SCs маркер, белок S100. Он также применяется для диагностики опухолей. В шванномах он содержится практически во всех клетках, в нейрофибромах – в некоторых, в MPNST – в единичных [78].
Исследование морфофункциональных особенностей SCs при различных заболеваниях позволяет выявлять их гистобластические потенции в условиях измененного микроокружения. Исследование молекулярных механизмов дифференцировки и уникальной пластичности этих клеток в опухолях и при других заболеваниях нерва, а также изучение изменения сигнальных путей, регулирующих эти процессы, имеет как общебиологическую значимость, так и большое практическое значение для разработки подходов к лечению этих заболеваний.
ШВАННОВСКИЕ КЛЕТКИ И СТИМУЛЯЦИЯ РЕГЕНЕРАЦИИ НЕРВОВ
В литературе, посвященной разработке способов улучшения регенерации органов нервной системы, шванновским клеткам уделяется значительное внимание. Это касается экспериментальных работ, целью которых является восстановление спинного мозга или периферического нерва после травмы.
Анализируя различные клеточные технологии, используемые для восстановления поврежденного спинного мозга, Челышев и Викторов [81] обращают внимание на то, что после травмы спинного мозга в области его повреждения появляются SCs. То есть в травмированном спинном мозге в процессе ремиелинизации аксонов принимают участие SCs, а не только олигодендроглия (миелин-образующие клетки ЦНС). Шванновские клетки мигрируют в область травмы спинного мозга из периферических нервных структур при нарушении целостности барьера в результате повреждения. Высказываются также предположения об участии резидентных нейральных клеток-предшественников спинного мозга, дифференцирующихся в SCs, или о возможности олигодендроцитов спинного мозга экспрессировать маркеры SCs при патологии. Главной целью применения клеточной терапии при травме спинного мозга является восстановление или поддержание структуры и функции именно белого вещества [81]. Здесь, в месте, где сосредоточены нервные волокна, использование трансплантации SCs кажется уместным, ведь эти клетки формируют миелин в нервных проводниках. В оригинальных исследованиях, выполненных десять лет назад как in vivo так и in vitro, установлено, что SCs способны миелинизировать аксоны ЦНС и улучшать их регенерацию.
В 90-е годы прошлого века были проведены первые работы по трансплантации экзогенных шванновских клеток в поврежденные нервные стволы с целью улучшения их регенерации [82]. Первоначально в искусственный кондуит, соединяющий концы перерезанного седалищного нерва крыс линии с иммунодефицитом, наполненный матригелем, пересаживали SCs человека. Используя антитела против клеток приматов, было установлено, что половина пересаженных SCs выживает в течение 4 нед. Количество миелинизированных аксонов в кондуите было значительно выше после применения клеточной терапии по сравнению с контролем. Некоторые из трансплантированных человеческих шванновских клеток оказались способными миелинизировать регенерирующие аксоны крысы. В то же время улучшение регенерации нерва было показано после введения SCs в коллагеновый кондуит аллогенного животного [83]. Гистологический анализ показал, что SCs сохраняли свою жизнеспособность длительное время (120 сут) и после трансплантации мигрировали на значительное расстояние от места имплантации.
Позднее кондуиты, соединяющие проксимальный и дистальный сегменты нервов, становились более совершенными [84]. Hadlock et al. [85] вводили SCs в кондуит из биодеградируемого материала (из высокомолекулярного сополимера молочной и гликолевой кислот) с внутренними поверхностями, которые способствовали прилипанию донорских SCs. Присутствие в такой конструкции шванновских клеток оказывало стимулирующее влияние на рост аксонов. В дальнейшем исследования в этом направлении проводились с использованием в качестве доноров животных, экспрессирующих зеленый флуоресцентный белок (GFP), что позволило наблюдать за судьбой пересаженных клеток [86, 87].
Как отмечалось ранее, шванновские клетки являются источником большого числа ростовых и нейротрофических факторов, белков экстрацеллюлярного матрикса, цитокинов. Учитывая эту особенность и необходимость биологически активных веществ, вырабатываемых SCs, для восстановления поврежденных нервных волокон, появились экспериментальные работы, в которых для трансплантации применялись не обычные SCs, а генетически модифицированные по NGF, BDNF, FGF-2, GDNF или NT-3 [88–91]. Генная модификация SCs осуществляется с помощью плазмидного или вирусного векторов [92]. В настоящее время в эксперименте применяется инъекция в поврежденный спинной мозг животного непосредственно плазмиды или аденовируса с генами определенных факторов роста (FRF2, VEGF, NDNF) [93, 94]. По данным некоторых авторов такой способ оказывается более эффективным для сохранения нервных проводников спинного мозга, чем трансплантация генетически модифицированных клеток [93, 94].
После того, как было установлено, что наполнение различного рода кондуитов (синтетических и биологических) шванновскими клетками оказывает стимулирующее влияние на рост аксонов, начались исследования по применению в качестве клеточной терапии различных стволовых клеток, в частности мезенхимных стволовых клеток (MSCs) [обзоры: 9–16]. В течение многих лет обсуждался вопрос о возможности MSCs или других используемых для пересадки в нерв стволовых клеток дифференцироваться в SCs и миелинизировать регенерирующие нервные волокна. С помощью иммуногистохимических маркеров и электронной микроскопии в ряде работ было показано, что это возможно. Проводятся эксперименты по предифференцировке MSCs, полученных из разных источников, в шванновские клетки в условиях in vitro перед тем, как вводить их в кондуит или непосредственно в поврежденный нерв.
Применение генной и клеточной терапии для восстановления нервных проводников в настоящее время продолжает активно разрабатываться. Здесь хочется подчеркнуть, что не менее важным направлением исследований является изучение реакции эндогенных шванновских клеток нервных стволов на повреждение и применение клеточной терапии. Исследования в этом направлении малочисленны. Есть данные о том, что повышение пролиферативной активности SCs после применения экспериментальной клеточной терапии коррелирует с улучшением роста аксонов [95]. Какие именно факторы, вырабатываемые пересаженными нейрогенными предшественниками, являются митогенами для SCs, неясно. Не изучено также, увеличивается ли пролиферация эндоневральных фибробластов при таких воздействиях. Предполагается, что ангиогенные факторы, вырабатываемые MSCs, могут улучшать васкуляризацию нервных стволов [96]. Васкуляризация нерва имеет не только важное трофическое значение для его регенерации, но способствует поступлению цитокинов и гормонов из кровеносного русла, которые оказывают влияние на эндогенные клетки и на репаративные процессы в поврежденном нерве. Высказывается мнение, что такие факторы роста как FGF или NGF, могут стимулировать пролиферацию шванновских клеток. Учитывая роль SCs для регенерации аксонов, стимуляция именно эндогенных шванновских клеток (а также других клеточных элементов нерва), на наш взгляд, может быть новой терапевтической стратегией восстановления поврежденных нервных проводников.
ЗАКЛЮЧЕНИЕ
В настоящем обзоре обобщены имеющиеся в современной литературе данные о происхождении шванновских клеток периферических нервных проводников в фило- и онтогенезе, а также об их уникальной фенотипической пластичности. Описаны функции SCs, проявляющиеся на разных стадиях их развития и после повреждения. Отмечены особенности SCs, выявляющиеся при патологии периферических нервных проводников. В настоящее время на улучшение микроокружения регенерирующих аксонов направлены новые стратегии применения биоинженерных конструкций, соединяющих проксимальный и дистальный сегменты поврежденного нерва. Для этого используется сочетание добавочных компонентов внеклеточного матрикса, нейротрофических факторов и экзогенных стволовых и генетически модифицированных клеток, которые могут способствовать росту и регенерации аксонов. Для применения новых клеточных и генных технологий в качестве терапии поврежденного нерва необходимо более полное понимание молекулярно-клеточных процессов, происходящих в регенерирующем нервном стволе. Малоизученными остаются молекулярные факторы и сигнальные пути, участвующие в регенерации нервных волокон.
Дальнейшие исследования помогут понять, в каком направлении следует совершенствовать клеточные и генные технологии восстановления нервных проводников, а также разобраться в этиологии и патогенезе неврологических расстройств, связанных с дисфункцией шванновских клеток.