Что является конечным продуктом окислительного декарбоксилирования пвк
ОКИСЛИТЕЛЬНОЕ ДЕКАРБОКСИЛИРОВАНИЕ ПВК



В состав пируватдегидрогеназного комплекса входит примерно по три десятка молекул Е1 и Е2 и 10 молекул Е3. Комплекс работает как конвейер: промежуточные продукты не освобождаются в раствор, а передаются от фермента к ферменту.
 а а | 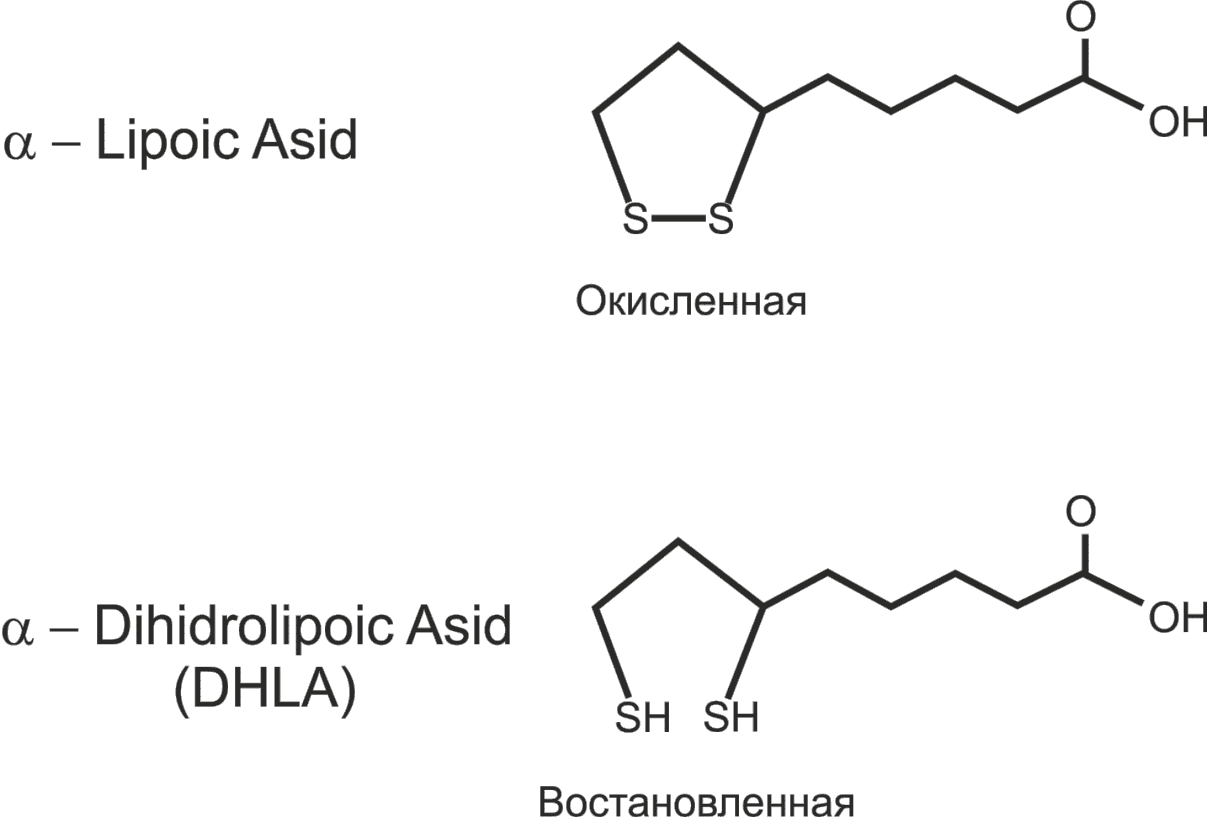 б б |
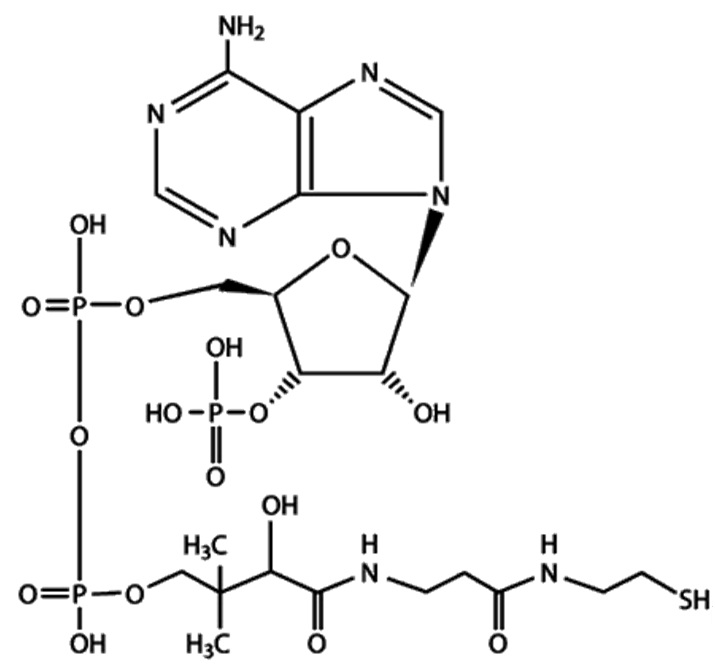
| Рис. 36. Структура кофермента А (а) и липоевой кислоты (б) |
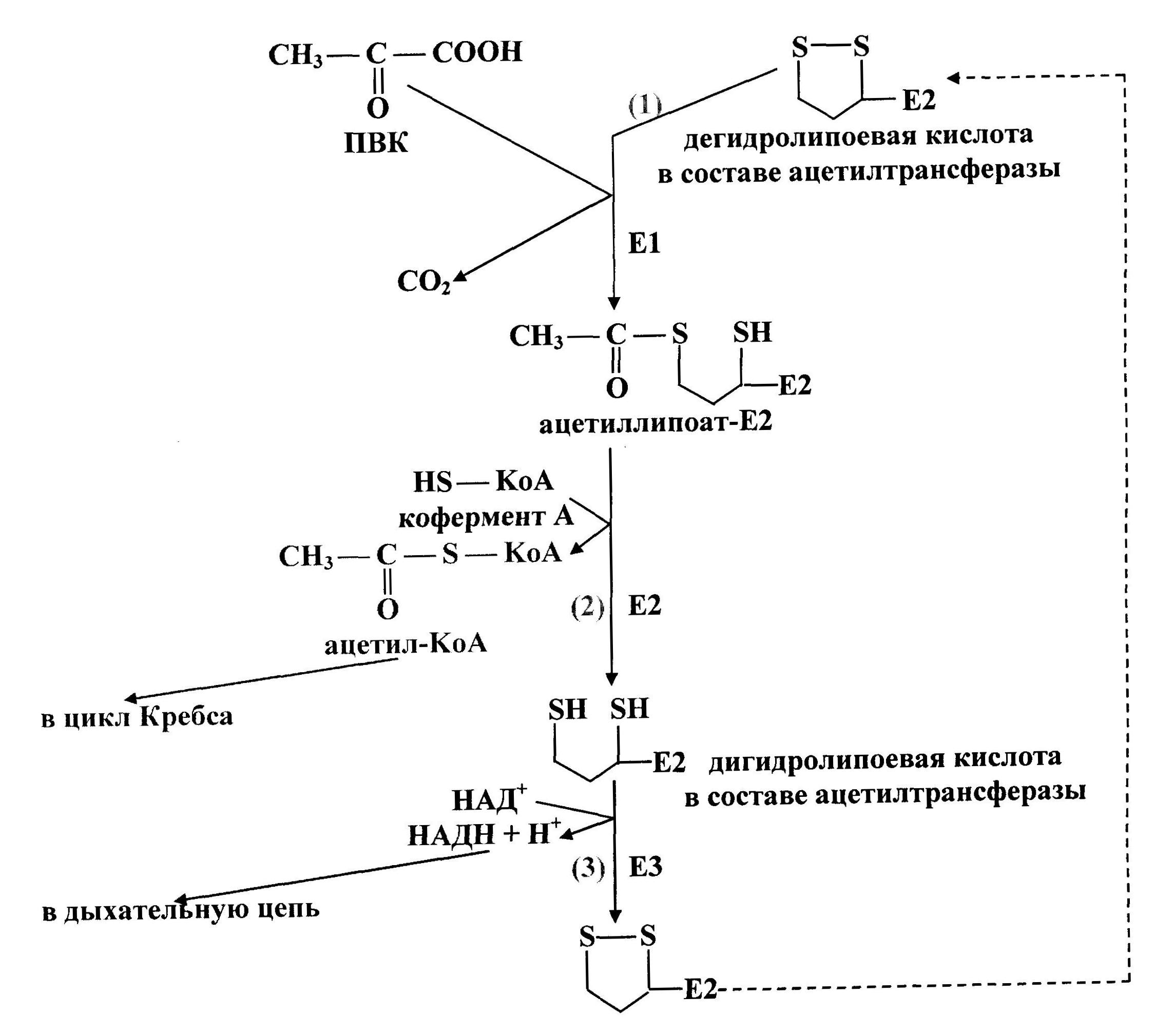
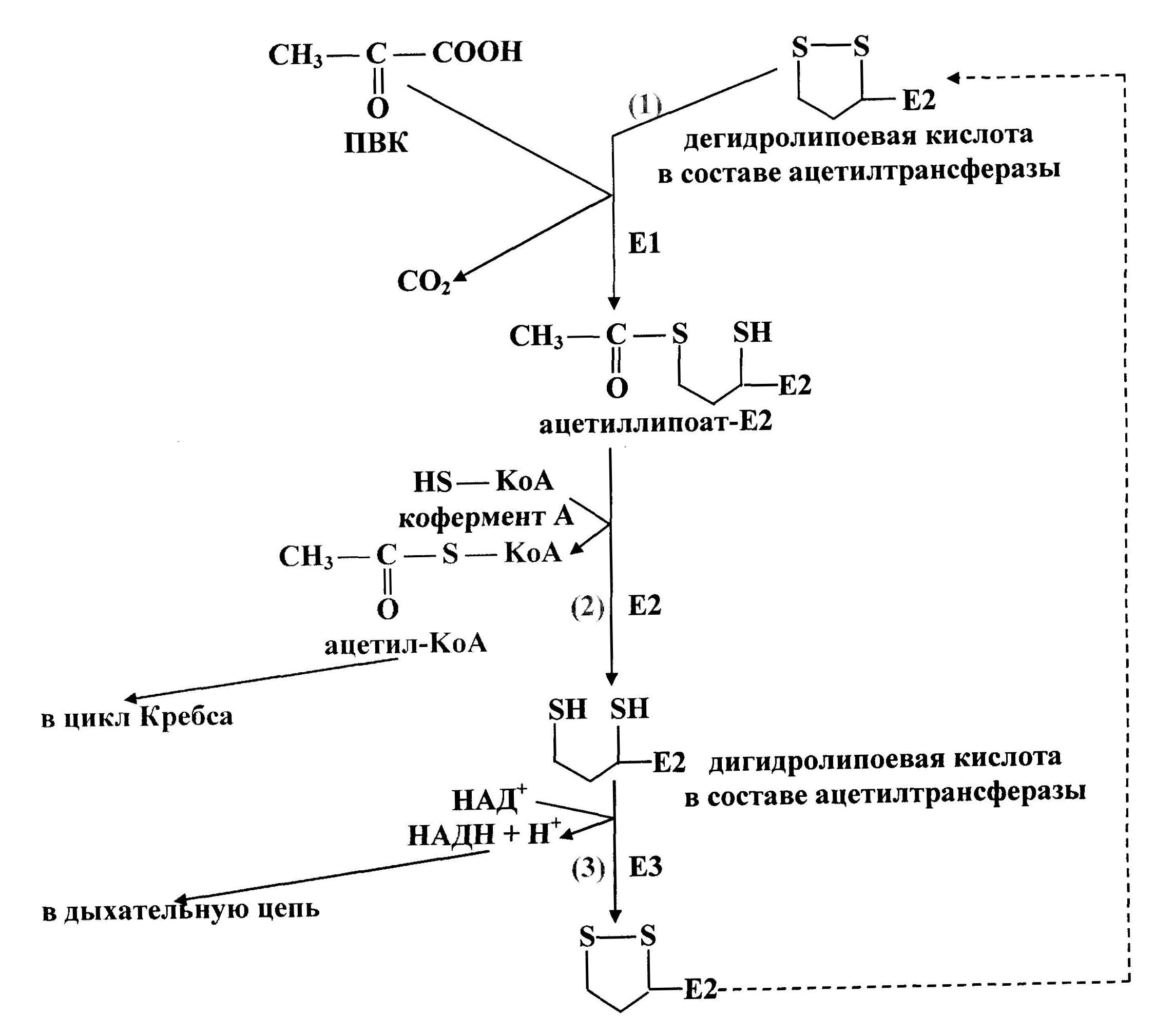
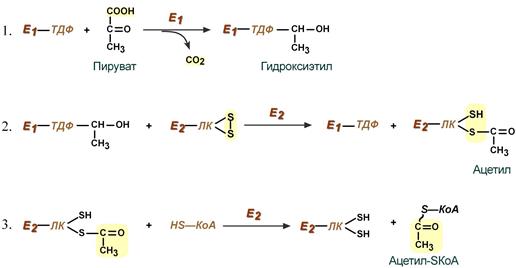
Первую реакцию (рис. 37) катализирует Е1, субстратами являются ПВК и дегидролипоевая кислота, являющаяся простетической группой Е2. От ПВК отщепляется карбоксильная группа и образуется СО2, а ацетильный остаток соединяется с атомом серы липоевой кислоты в составе ацетилтрансферазы. Образуется ацетиллипоат-Е2.
Ацетил-KоА (продукт второй реакции) затем окисляется в цикле Кребса. Водород с НАДН (продукт третьей реакции) поступает в дыхательную цепь, где образуется АТФ.
Энергетический выход окислительного декарбоксилирования пирувата – 3 АТФ.
Суммарное уравнение процесса:
СH3-CО-COOH + HS-KoA + НАД + ® СH3-CО-S-KoA + НАДН + Н + + СО2.
Рис. 37. Схема окислительного декарбоксилирования пирувата
ОКИСЛИТЕЛЬНОЕ ДЕКАРБОКСИЛИРОВАНИЕ ПВК
В состав пируватдегидрогеназного комплекса входит примерно по три десятка молекул Е1 и Е2 и 10 молекул Е3. Комплекс работает как конвейер: промежуточные продукты не освобождаются в раствор, а передаются от фермента к ферменту.
 а а | 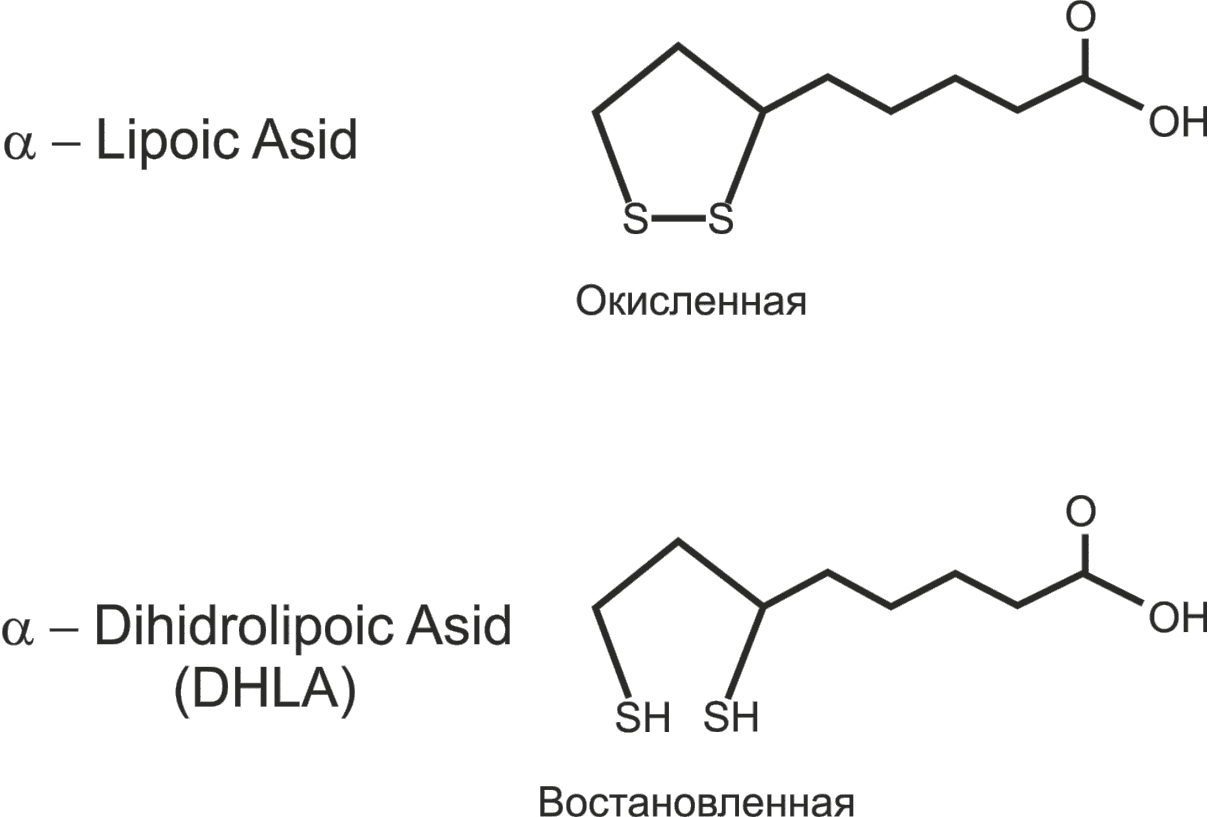 б б |
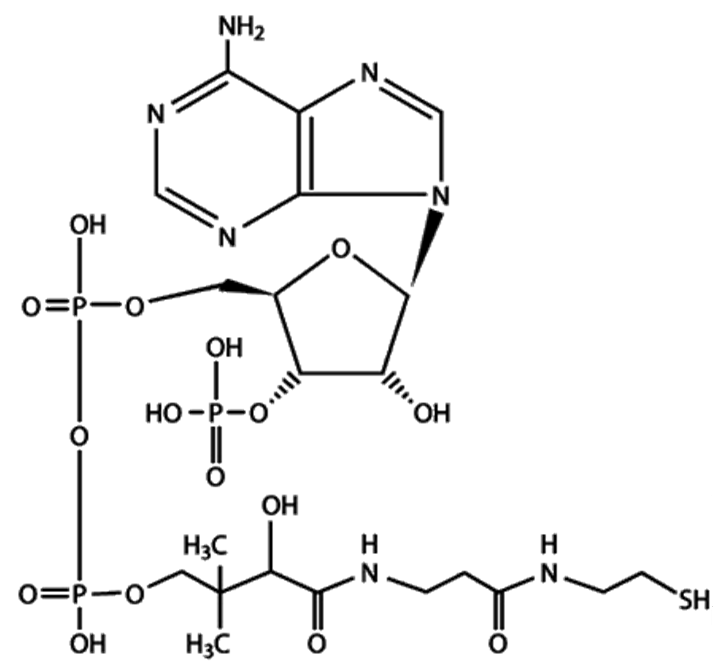
| Рис. 36. Структура кофермента А (а) и липоевой кислоты (б) |
Первую реакцию (рис. 37) катализирует Е1, субстратами являются ПВК и дегидролипоевая кислота, являющаяся простетической группой Е2. От ПВК отщепляется карбоксильная группа и образуется СО2, а ацетильный остаток соединяется с атомом серы липоевой кислоты в составе ацетилтрансферазы. Образуется ацетиллипоат-Е2.
Ацетил-KоА (продукт второй реакции) затем окисляется в цикле Кребса. Водород с НАДН (продукт третьей реакции) поступает в дыхательную цепь, где образуется АТФ.
Энергетический выход окислительного декарбоксилирования пирувата – 3 АТФ.
Суммарное уравнение процесса:
СH3-CО-COOH + HS-KoA + НАД + ® СH3-CО-S-KoA + НАДН + Н + + СО2.
Рис. 37. Схема окислительного декарбоксилирования пирувата
Окислительное декарбоксилирование пировиноградной кислоты
Окисление пирувата до ацетил-КоА происходит при участии ряда ферментов и коферментов, объединенных структурно в мультиферментную систему, получившую название «пируватдегидрогеназный комплекс».
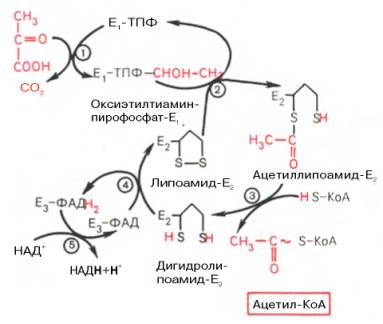
На I стадии этого процесса пируват (рис. 10.8) теряет свою карбоксильную группу в результате взаимодействия с тиаминпирофосфатом (ТПФ) в составе активного центра фермента пируватдегидрогеназы (E1). На II стадии оксиэтильная группа комплекса E1–ТПФ–СНОН–СН3 окисляется с образованием ацетильной группы, которая одновременно переносится на амид липоевой кислоты (кофермент), связанной с ферментом дигидроли-поилацетилтрансферазой (Е2). Этот фермент катализирует III стадию – перенос ацетильной группы на коэнзим КоА (HS-KoA) с образованием конечного продукта ацетил-КоА, который является высокоэнергетическим (макроэргическим) соединением.
Процесс окислительного декарбоксилирования пирувата происходит в матриксе митохондрий. В нем принимают участие (в составе сложного мультиферментного комплекса) 3 фермента (пируватдегидрогеназа, ди-гидролипоилацетилтрансфераза, дигидролипоилдегидрогеназа) и 5 кофер-ментов (ТПФ, амид липоевой кислоты, коэнзим А, ФАД и НАД), из которых три относительно прочно связаны с ферментами (ТПФ-E1, ли-поамид-Е2 и ФАД-Е3), а два – легко диссоциируют (HS-KoA и НАД).
Рис. 10.8. Механизм действия пируватдегидрогеназного комплекса.
Все эти ферменты, имеющие субъединичное строение, и коферменты организованы в единый комплекс. Поэтому промежуточные продукты способны быстро взаимодействовать друг с другом. Показано, что составляющие комплекс полипептидные цепи субъединиц дигидролипоил-ацетилтрансферазы составляют как бы ядро комплекса, вокруг которого расположены пируватдегидрогеназа и дигидролипоилдегидрогеназа. Принято считать, что нативный ферментный комплекс образуется путем самосборки.
Суммарную реакцию, катализируемую пируватдегидрогеназным комплексом, можно представить следующим образом:
Пируват + НАД + + HS-KoA –> Ацетил-КоА + НАДН + Н + + СO2.
Реакция сопровождается значительным уменьшением стандартной свободной энергии и практически необратима.
Образовавшийся в процессе окислительного декарбоксилирования аце-тил-КоА подвергается дальнейшему окислению с образованием СО2 и Н2О. Полное окисление ацетил-КоА происходит в цикле трикарбоновых кислот (цикл Кребса). Этот процесс, так же как окислительное декарбо-ксилирование пирувата, происходит в митохондриях клеток.
Пируват окисляется до уксусной кислоты
Пируватдегидрогеназный мульферментный комплекс
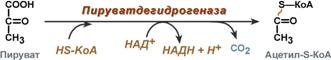
Суммарное уравнение отражает окислительное декарбоксилирование пирувата, восстановление НАД до НАДН и образование ацетил-SKoA.
Суммарное уравнение окисления пировиноградной кислоты
Превращение состоит из пяти последовательных реакций, осуществляется мультиферментным комплексом, прикрепленным к внутренней митохондриальной мембране со стороны матрикса. В составе комплекса насчитывают 3 фермента и 5 коферментов:
Помимо указанных коферментов, которые прочно связаны с соответствующими ферментами, в работе комплекса принимают участие коэнзим А и НАД.
Суть первых трех реакций сводится к декарбоксилированию пирувата (катализируется пируватдегидрогеназой, Е1), окислению полученного гидроксиэтила до ацетила и переносу ацетила на коэнзим А (катализируется дигидролипоат-ацетилтрансферазой, Е2).
Реакции синтеза ацетил-SКоА
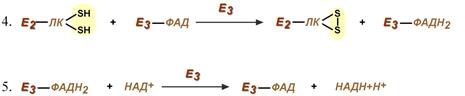
Оставшиеся 2 реакции необходимы для возвращения липоевой кислоты и ФАД в окисленное состояние (катализируются дигидролипоат-дегидрогеназой, Е3). При этом образуется НАДН.
Реакции образования НАДН
Регуляция пируватдегидрогеназного комплекса
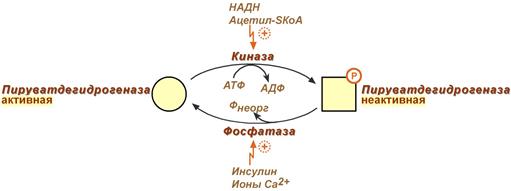
Регулируемым ферментом ПВК-дегидрогеназного комплекса является первый фермент – пируватдегидрогеназа (Е1). Два вспомогательных фермента – киназа и фосфатаза обеспечивают регуляцию активности пируватдегидрогеназы путем ее фосфорилирования и дефосфорилирования.
Регуляция активности пируватдегидрогеназы
Таким образом, работа пируватдегидрогеназы подавляется при избытке в митохондрии (в клетке) ацетил-SКоА и НАДН, что позволяет снизить окисление пирувата и, следовательно, глюкозы в случае когда энергии достаточно.
Если АТФ мало или имеется влияние инсулина, то образуется ацетил-SКоА. Последний в зависимости от условий будет направляться либо в цикл трикарбоновых кислот с образованием энергии АТФ, либо на синтез холестерина и жирных кислот.
Лекционные материалы на тему: «Цикл трикарбоновых кислот»
Онлайн-конференция
«Современная профориентация педагогов
и родителей, перспективы рынка труда
и особенности личности подростка»
Свидетельство и скидка на обучение каждому участнику
ЦЕНТРАЛЬНЫЕ МЕТАБОЛИЧЕСКИЕ ПУТИ:
ОКИСЛИТЕЛЬНОЕ ДЕКАРБОКСИЛИРОВАНИЕ ПИРУВАТА,
ЦИКЛ ТИКАРБОНОВЫХ КИСЛОТ
ЦЕНТРАЛЬНЫЕ МЕТАБОЛИЧЕСКИЕ ПУТИ
Основными поставщиками восстановленных субстратов являются центральные метаболические пути, а именно, окислительное декарбоксилирование пировиноградной кислоты и цикл лимонной кислоты. Они локализованы в матриксе митохондрий, в ходе этих процессов происходят реакции декарбоксилирования (большая часть всей углекислоты, образующейся в клетках, образуется именно здесь). Кроме того, в ходе этих процессов происходят реакции дегидрирования субстратов, образуются восстановленные коферментные формы НАДН·Н + и ФАДН2, водород которых поступает в дыхательную цепь внутренней мембраны митохондрий, где происходит его окисление кислородом до воды и синтез АТФ.
ОКИСЛИТЕЛЬНОЕ ДЕКАРБОКСИЛИРОВАНИЕ ПИРУВАТА
Пировиноградная кислота (ПВК, пируват) является продуктом окисления глюкозы и некоторых аминокислот. Ее судьба различна в зависимости от доступности кислорода в клетке. В анаэробных условиях она восстанавливается до молочной кислоты. В аэробных условиях происходит ее окислительное декарбоксилирование до уксусной кислоты, переносчиком которой служит коэнзим А.
Суммарное уравнение реакции отражает декарбоксилирование пирувата, восстановление НАД до НАДН Н + и образование ацетил-SKoA.
Окислительное декарбоксилирование пирувата состоит из пяти последовательных реакций и осуществляется при участии набора ферментов, объединенных в пируватдегидрогеназный комплекс (ПВДГК). Это мультиферментная система, которая включает 3 фермента и 5 коферментов (все они являются водорастворимыми витаминами).
Е1 — пируватдекарбоксилаза. Коферментом является активная форма витамина В1, тиамина — ТПФ (тиаминпирофосфат).
Е2 — дигидролипоилацетилтрансфераза. Коферментом является витаминоподобное вещество — липоевая кислота (липоил), которая может временно превращаться в дигидролипоил, присоединив 2 атома водорода. Липоил может также переносить ацетильные остатки.
С этим ферментом также работает активная форма пантотеновой кислоты — КоА-SH, которая принимает ацетильный остаток от липоевой кислоты.
Е3 — дигидролипоилдегидрогеназа. Коферментом является ФАД — активная форма витамина В2, рибофлавина. С работой этого фермента связан также кофермент НАД + — активная форма витамина РР, никотиновой кислоты.
Суть первых трех реакций сводится к декарбоксилированию пирувата (катализируется Е1), окислению пирувата до ацетила и переносу ацетила на коэнзим А (катализируется Е2).
Оставшиеся 2 реакции необходимы для возвращения липоевой кислоты и ФАД в окисленное состояние (катализируются Е3). При этом образуется
Таким образом, в результате образуются конечные продукты — СО2, атомы водорода для дыхательной цепи в составе НАДН·Н + и макроэргическое соединение ацетил- S КоА.
Лимитирующей реакцией в этом процессе является пируватдекарбоксилазная реакция. Поскольку фермент
Е1- пируватдекарбоксилаза в качестве кофермента использует ТПФ, при недостатке тиамина в пище нарушается окисление пирувата — процесса, который поставляет клеткам энергию. Возникает энергодефицит, что требует коррекции нарушения метаболизма с помощью тиамина. Схема регуляции работы пиуватдегидогеназного комплекса предствалена на рисунке (слайде).
ЛИМОННОКИСЛЫЙ ЦИКЛ КРЕБСА,
ЦИКЛ ТРИКАРБОНОВЫХ КИСЛОТ (ЦТК)
Цикл лимонной кислоты локализован в матриксе митохондрий. Это циклический процесс из восьми последовательных реакций, в результате которых происходит декарбоксилирование и дегидрирование ацетил-КоА (универсального клеточного топлива).
Цикл начинается с конденсации ацетил-КоА с 4-углеродной кетокислотой — щавелевоуксусной (ЩУК). В результате образуется трикарбоновая кислота – лимонная, или цитрат. Изомеризация цитрата ведет к образованию изоцитрата. В ходе последовательных реакций изоцитрат де-карбоксилируется и одновременно дегидрируется (фермент изоцитратДГ). Образовавшийся альфа-кетоглутарат также декарбоксилируется и дегидрируется. Образовавшийся макроэрг сукцинил-КоА служит источником энергии для синтеза АТФ (субстратное фосфорилирование в цикле Кребса). В результате еще двух дегидрирований (ферменты сукцинатДГ и малатДГ) ЩУК регенерирует и запускает новый оборот цикла Кребса.
Таким образом, наряду с конечным продуктом обмена — СО2, в четырех дегидрогеназных реакциях трижды восстанавливается НАД+ (изоцитратДГ, альфа-кетоглутаратДГ, малатДГ) и один раз восстанавливается ФАД (сукцинатДГ). Чтобы цикл мог функционировать, необходимо окислить эти коферменты, т. е. передать атомы водорода в дыхательную цепь, где происходит их окисление кислородом до воды.
Функции цикла Кребса
1. Интегративная функция. Цикл Кребса является связующим звеном между реакциями катаболизма и анаболизма.
2. Катаболическая функция. В ходе ЦТК окисляются до конечных продуктов обмена ацетильные остатки, образовавшиеся из топливных молекул (глюкоза, жирные кислоты, глицерол, аминокислоты).
3. Анаболическая функция. Субстраты ЦТК являются основой для синтеза многих молекул (кетокислоты — α-кетоглутарат и ЩУК — могут превращаться в аминокислоты глутамин и аспарагин; ЩУК может превращаться в глюкозу, сукцинил-КоА используется на синтез гема).
4. Водороддонорная функция. Цикл Кребса поставляет субстраты для дыхательной цепи (НАД-зависимые субстраты: изоцитрат, альфа-кетоглутарат, малат; ФАД-зависимый субстрат – сукцинат).
5. Энергетическая функция. На уровне сукцинил-КоА происходит субстратное фосфорилирование с образованием 1 молекулы макроэрга. Помимо этого, 4 дегидрогеназные реакции в цикле Кребса создают мощный поток электронов, богатых энергией. Эти электроны поступают в дыхательную цепь внутренней мембраны митохондрий. Конечным акцептором электронов является кислород. При последовательном переносе электронов на кислород выделяется энергия, достаточная для образования 9 молекул АТФ путем окислительного фосфорилирования.
Несмотря на постоянную убыль субстратов в результате анаболической функции, цикл Кребса не прерывается благодаря анаплеротическим реакциям, которые пополняют фонд его субстратов. Важнейшей анаплеротической реакцией является образование ЩУК (молекулы, запускающей цикл) путем карбоксилирования ПВК.
1. Главным и основным регулятором ЦТК является доступность оксалоацетата. Наличие оксалоацетата вовлекает в ЦТК ацетил-SКоА и запускает процесс.
В клетке имеется баланс между образованием ацетил-SКоА (из глюкозы, жирных кислот или аминокислот) и количеством оксалоацетата. Источником оксалоацетата является синтез из пирувата (анаплеротическая или пополняющая реакция), поступление из фруктовых кислот самого ЦТК (яблочной, лимонной), образование из аспарагиновой кислоты.
2. Ферменты ЦТК являются чувствительными к аллостерической регуляции метаболитами.
Например, первый фермент цитратсинтаза ингибируется АТФ, жирными кислотами. Лимитирующим ферментом (катализирует самую медленную реакцию) является изоцитратДГ. Он активируется АДФ, НАД+, ингибируется АТФ, НАДН·Н+. Когда в клетке достаточно АТФ (покой), скорость цикла снижается, при распаде же АТФ образуется АДФ, который активирует самую медленную реакцию и, следовательно, скорость всего цикла в целом.
Если Вы считаете, что материал нарушает авторские права либо по каким-то другим причинам должен быть удален с сайта, Вы можете оставить жалобу на материал.