Что является непосредственным источником энергии в организме адреналин эритроциты миоглобин
Основные закономерности метаболических процессов в организме человека. Часть 2.
Рассматривая обмен веществ в условиях нормального функционирования организма, следует остановиться на безусловно взаимосвязанных, но в то же время достаточно специфичных составляющих метаболизма, а именно на углеводном, белковом, липидном и водно-электролитном обмене.
Очевидно, что основная роль углеводов в метаболизме определяется их энергетической функцией. Именно глюкоза крови вследствие наличия простого и быстрого пути гликолитической диссимиляции и последующего окисления в цикле трикарбоновых кислот, а также возможности максимально быстрого извлечения ее из депо гликогена, обеспечивающей экстренную мобилизацию энергетических ресурсов, является наиболее востребованным источником энергии в организме. Использование циркулирующей в плазме глюкозы разными органами неодинаково: мозг задерживает 12% глюкозы, кишечник— 9%, мышцы — 7%, почки — 5%. При этом уровень глюкозы плазмы крови является одной из важнейших гомеостатических констант организма, составляя 3, 3—5, 5 ммоль/л. Как известно снижение уровня глюкозы ниже допустимого передела имеет своим незамедлительным следствием дискоординацию деятельности ЦНС, проявляющуюся соответствующей клинической симптоматикой: головной мозг содержит небольшие резервы углеводов и нуждается в постоянном поступлении глюкозы, поскольку энергетические расходы мозга покрываются исключительно за счет углеводов. Глюкоза в тканях мозга преимущественно окисляется, а небольшая часть ее превращается в молочную кислоту.
При полном отсутствии углеводов в пище они образуются в организме из продуктов трансформации жиров и белков. В печени возможно новообразование углеводов как из собственных продуктов их распада (пировиноградной или молочной кислоты), так и из продуктов диссимиляции жиров и белков (кетокислот и аминокислот), что обозначается как глюконеогенез. В результате трансформации аминокислот образуется пировиноградная кислота, при окислении жирных кислот — ацетилкоэнзим А, который может превращаться в пировиноградную кислоту — предшественник глюкозы. Это наиболее важный общий путь биосинтеза углеводов. Между двумя основными источниками энергии — углеводами и жирами — существует тесная физиологическая взаимосвязь. Повышение содержания глюкозы в крови увеличивает биосинтез триглицеридов и уменьшает распад жиров в жировой ткани. Поступление в кровь свободных жирных кислот уменьшается. В случае возникновения гипогликемии процесс синтеза триглицеридов тормозится, ускоряется распад жиров и в кровь в большом количестве поступают свободные жирные кислоты. Гликогенез, гликогенолиз и глюконеогенез являются тесно взаимосвязанными процессами, обеспечивающими оптимальный уровень глюкозы крови сообразно степени функционального напряжения организма.
Центральным звеном регуляции углеводного и других видов обмена и местом формирования сигналов, управляющих уровнем глюкозы, является гипоталамус. Отсюда регулирующие влияния реализуются вегетативными нервами и гуморальным путем, включающим эндокринные железы. Единственным гормоном, снижающим уровень гликемии, является инсулин — гормон, вырабатываемый β-клетками островков Ланхгерганса. Снижение гликемии происходит за счет усиления инсулином синтеза гликогена в печени и мышцах и повышения потребления глюкозы тканями организма. Увеличение уровня глюкозы в крови возникает при действии нескольких гормонов. Это глюкагон, продуцируемый α-клетками островков Ланхгерганса, адреналин — гормон мозгового слоя надпочечников, глюкокортикоиды — гормоны коркового слоя надпочечников, соматотропный гормон гипофиза, тироксин и трийодтиронин — гормоны щитовидной железы. Данные гормоны в связи с однонаправленностью их влияния на углеводный обмен и функциональным антагонизмом по отношению к эффектам инсулина часто объединяют понятием «контринсулярные гормоны».
Таким образом биологическая роль углеводов для организма человека определяется прежде всего их энергетической функцией. Обладая энергетической ценностью в 16, 7 кДж (4, 0 ккал) на 1 грамм вещества, углеводы являются основным источником энергии для всех клеток организма, при этом выполняя еще пластическую и опорную функции. Суточная потребность взрослого человека в углеводах составляет около 500 г.
— пластическая (структурная) функция заключается в том, что белки являются главной составной частью всех клеточных и межклеточных структур тканей;
— ферментная (каталитическая, энзимная) функция состоит в обеспечении всех химических реакций, протекающих в ходе обмена веществ в организме (дыхание, пищеварение, выделение), деятельностью ферментов, являющихся по своей структуре белками;
— транспортная функция белков заключается в их способности к соединению с целым рядом метаболитов и переносе последних в связанном состоянии в межтканевой жидкости и плазме крови к области их утилизации;
— защитная функция белков проявляется реализацией иммунного ответа образованием иммуноглобулинов (антител) и системы комплемента при поступлении в организм чужеродного белка, а также способностью к непосредственному связыванию экзогенных токсинов; белки системы гемостаза обеспечивают свертывание крови и остановку кровотечения при повреждении кровеносных сосудов;
— регуляторная функция, направленная на сохранение гомеостаза с поддержанием биологических констатнт организма, реализуется буферными свойствами молекулы протеинов, белковой структурой клеточных рецепторов, активируемых в свою очередь регуляторными полипептидами и гормонами, также имеющими белковую структуру;
— двигательная функция, обеспечивается взаимодействием сократительных белков мышечной ткани актина и миозина;
— энергетическая роль белков состоит в обеспечении организма энергией, образующейся при диссимиляции белковых молекул; при окислении 1 г белка в среднем освобождается энергия, равная 16, 7 кДж (4, 0 ккал).
При катаболизме почти все природные аминокислоты сначала передают аминогруппу на а-кетоглутарат в реакции трансаминирования с образованием глутамата и соответствующей кетокислоты. Затем глутамат подвергается прямому окислительному дезаминированию под действием глутаматдегидрогеназы, в результате чего получаются а-кетоглутарат и аммиак. При необходимости синтеза аминокислот и наличии необходимых а-кетокислот обе стадии непрямого дезаминирования протекают в обратном направлении. В результате восстановительного аминирования а-кетоглутарата образуется глутамат, который вступает в трансаминирование с соответствующей а-кетокислотой, что приводит к синтезу новой аминокислоты. В случае использования белков в качестве источника энергии большинство аминокислот окисляются в конечном счёте через цикл лимонной кислоты до углекислого газа и воды. Прежде, чем эти вещества вовлекаются в заключительный этап катаболизма, их углеродный скелет превращается в двухуглеродный фрагмент в форме ацетил-КоА. Именно в этой форме большая часть молекул аминокислот включается в цикл лимонной кислоты.
Таблица 1. 1. Аминокислоты, входящие в состав белков человека.
1. Незаменимые
2. Частично заменимые
3. Условно заменимые
4. Заменимые
Таблица 1. 2. Классификация липидов организма человека.
1. Гликолипиды.
Содержат углеводный компонент.
2. Жиры.
3. Минорные липиды.
4. Стероиды.
А. Стерины (спирты).
Наиболее важен холестерин.
В. Стериды.
Эфиры стеринов и высших жирных кислот. Наиболее распространены эфиры холестерина.
5. Фосфолипипы.
Одним из продуктов катаболизма жиров, имеющем важное значения для метаболизма в целом являются кетоновые тела. Кетоновые тела — группа органических соединений, являющихся промежуточными продуктами жирового, углеводного и белкового обменов. К кетоновым телам относят β-оксимасляную и ацетоуксусную кислоты и ацетон, имеющие сходное строение и способные к взаимопревращениям. Главным путем синтеза кетоновых тел, происходящего в основном в печени, считается реакция конденсации между двумя молекулами ацетил-КоА, образовавшегося при β-окислении жирных кислот или при окислительном декарбоксилировании пирувата (пировиноградной кислоты) в процессе обмена глюкозы и ряда аминокислот. Данный путь синтеза кетоновых тел более других зависит от характера питания и в большей степени страдает при патологических нарушениях обмена веществ. Из печени кетоновые тела поступают в кровь и с нею во все остальные органы и ткани, где они включаются в универсальный энергообразующий цикл — цикл трикарбоновых кислот, в котором окисляются до углекислоты и воды. Кетоновые тела используются также для синтеза холестерина, высших жирных кислот, фосфолипидов и заменимых аминокислот. При голодании, однообразном безуглеводистом питании и при недостаточной секреции инсулина использование ацетил-КоА в цикле трикарбоновых кислот подавляется, так как все метаболически доступные ресурсы организма превращаются в глюкозу крови. В этих условиях увеличивается синтез кетоновых тел. Следует подчеркнуть важную роль кетоновых тел в поддержании энергетического баланса. Кетоновые тела – поставщики «топлива» для мышц, почек и действуют, возможно, как часть регуляторного механизма с обратной связью, предотвращая чрезвычайную мобилизацию жирных кислот из жировых депо. Печень в этом смысле является исключением, она не использует кетоновые тела в качестве энергетического материала.
Процесс образования, отложения и мобилизации из депо жира регулируется нервной и эндокринной системами, а также тканевыми механизмами и тесно связаны с углеводным обменом. Так, повышение концентрации глюкозы в крови уменьшает распад триглицеридов и активизирует их синтез. Понижение концентрации глюкозы в крови, наоборот, тормозит синтез триглицеридов и усиливает их расщепление. Таким образом, взаимосвязь жирового и углеводного обменов направлена на обеспечение энергетических потребностей организма. При избытке углеводов в пище триглицериды депонируются в жировой ткани, при нехватке углеводов происходит расщепление триглицеридов с образованием неэтерифицнрованных жирных кислот, служащих источником энергии. В обмене жиров одна из важнейших ролей принадлежит печени. Печень — основной орган, в котором происходит образование кетоновых тел (бета-оксимасляная, ацетоуксусная кислоты, ацетон), используемых как альтернативный глюкозе источник энергии.
Как указывалось выше метаболизм жиров контролируется нервной и эндокринной системами. Мобилизация жиров из депо происходит под влиянием гормонов мозгового слоя надпочечников — адреналина и норадреналина. Соматотропный гормон гипофиза также обладает жиромобилизирующим действием. Аналогично действует тироксин — гормон щитовидной железы. Тормозят мобилизацию жира глюкокортикоиды — гормоны коркового слоя надпочечника, вероятно, вследствие того, что они несколько повышают уровень глюкозы в крови. Действие инсулина связано с повышением активности внутриклеточной фосфодиэстеразы, что приводит к снижению концентрации цАМФ и угнетению липолиза. Таким образом, инсулин усиливает синтез жира и уменьшает скорость его мобилизации. Имеются данные, свидетельствующие о возможности прямых нервных влияний на обмен жиров. Симпатические влияния тормозят синтез триглицеридов и усиливают их распад. Парасимпатические влияния, напротив, способствуют отложению жира в депо.
Статья добавлена 31 мая 2016 г.
Что является непосредственным источником энергии в организме адреналин эритроциты миоглобин
Источники энергетического обеспечения эритроцитов
Эритроцит является метаболически активной клеткой и содержит более 40 различных ферментов. Энергетическое обеспечение эритроцита осуществляется за счет утилизации глюкозы в реакциях анаэробного гликолиза. Эффективность гликолиза характеризуется образованием двух молекул АТФ на одну молекулу глюкозы, однако это небольшое количество энергии обеспечивает эритроциту выполнение всех его функций.
Основная доля энергии АТФ расходуется в эритроцитах на транспорт ионов, функционирование АТФ-азных систем и поддержание электролитного баланса клетки. Макроэргические фосфатные связи АТФ необходимы также и для инициации реакций гликолиза и пентозофосфатного цикла.
Наиболее важные реакции гликолиза протекают с участием следующих ферментов: гексокиназы, фосфофруктокиназы и пируваткиназы. Отличительной особенностью гликолиза в эритроцитах по сравнению с другими клетками является выработка значительного количества 2,3-дифосфоглицериновой кислоты, регулирующей кислородосвязывающую функцию гемоглобина.
Кроме гликолиза в эритроцитах происходит прямое окисление глюкозы в пентозофосфатном цикле, на долю которого приходится 10 – 11 % всего энергетического метаболизма клетки. Ключевыми ферментами пентозофосфатного цикла являются глюкозо-6-фосфат-дегидротеназа, 6-фосфоглюконатдегидрогеназа. В процессе пентозофосфатного окисления глюкозы образуется восстановленная форма кофермента НАДФ, использующаяся для восстановления глутатиона – основного компонента антиоксидантной системы эритроцита.
Главной функциональной группой глутатиона является сульфгидрильная группа, водород которой обеспечивает нейтрализацию органических и неорганических окислителей, действующих на мембрану эритроцита, и защищает липиды мембраны от свободнорадикального окисления.
Вышеизложенное делает очевидным большую значимость для поддержания стабильности эритроцитарной мембраны, интенсивности гликолитических реакций, обеспечивающих образование АТФ и соответственно полноценное функционирование АТФ-азных систем и трансмембранный перенос ионов, а также состояние пентозного цикла окисления глюкозы и образование достаточного количества НАДФН2.
В условиях врожденной или приобретенной недостаточности энергообеспечения эритроцитов при нарушении активности гликолитических ферментов, а также ферментов пентозофосфатного окисления глюкозы возникает дестабилизация эритроцитарной мембраны, изменение формы эритроцита и гемолиз.
Как известно, отличительными особенностями структуры и, соответственно, метаболизма эритроцитов являются отсутствие ядра, рибосомального аппарата, в связи с чем эритроциты не обладают белок-синтетической функцией. В эритроцитах отсутствуют митохондрии, система цитохром и соответственно отсутствует цикл трикарбоновых кислот. Эритроцит не воспроизводит De novo нуклеиноыве кислотиы и липиды. Основным источником энергии для эритроцитов является глюкоза, метаболизирующаяся по двум основным путям: путь Эмбдена-Мейергофа и в гексозомонофосфатный путь.
Лишенный глюкозы эритроцит деградирует, переходит в эхиноцит, сфероцит и затем подвергается осмотическому лизису, поскольку теряет способность поддерживать градиент натрия и калия, в то же время накапливает окисленный глутатион и метгемоглобин в условиях окислительного стресса.
Метаболизм глюкозы в пути Эмбдена-Мейергофа заканчивается образованием пирувата или лактата. Проникновение глюзозы в эритроцит происходит довольно быстро с помощью неиндентифицированного переносчика мембраны клеток. Концентрация глюкозы в эритроцитах такая же, как и в плазме крови. Основные стадии пути Эмбдена-Мейергофа включают: фосфорилирование глюкозы при участии АТФ и гексокиназы.
Дефицит гексокиназы может быть одной из причин наследственной гемолитической анемии. Продукт гексокиназной реакции (глюкозо-6-фосфат) трасформирется в глюкозо-1-фосфат при участии фосфоглюкомутазы, а также находится в рановесии с фруктозо-6-фосфат вследствие глюкозофосфатизомеразной реакции (ГФИ), имеющей большое метаболическое значение. Дефицит ГФИ является причиной достаточно часто возникающей наследственной несфероцитарной гемолитической анемии. Третья стадия в пути Эмбдена-Мейергофа включает фосфорилирование фруктозо-6-фосфата до фруктозо-1,6-дифосфата при участии фосфофруктокиназы.
Дефицит фермента ФФК является одной из причин нарушения накопления гликогена и развития наследственной гемолитической анемии.
Далее в эритроците Ф-1,6-ДФ распадается на две триозы – глицеральдегидтрифосфат (ГАФ) и диоксиацетонфосфат (ДАФ).
Глицеральдегидтрифосфат непрерывно превращается в 1,3ДФГ, который затем трансформируется в 2,3ДФГ и 3ФГ. Последний дефосфорилируется в 2ФГ, который находится в равновесии с фосфоенолпируватом (ФЕП). В свою очередь ФЕП служит донором фосфата для АДФ на второй стадии синтеза АТФ в реакциях гликолиза в эритроцитах.
Гексозомонофосфатный путь. Образующийся в гексокиназной реакции глюкозо-6-фосфат далее участвует в 3-х направлениях метаболизма в эритроцитах с участием ферментов фосфоглюкокиназы, глюкозофосфоизомеразы(ГФИ) и глюкозо-6-фосфатдегидрогеназы(Г-6-ФДГ). В глюкозо-6-фосфатдегидрогеназных реакциях НАДФ+ восстанавливается до НАДФ*Н. В 6-фосфоглюконатдегидрогеназной реакции в эритроцитах образуется рибулозо-5-фосфат, который находится в равновесии с рибозо-5-фосфатом и ксилулозо-5-фосфатом.
В физиологических условиях энергетические потребности эритроцитов покрываются в результате утилизации глюкозы в пути Эмбдена-Мейергофа и гексозомонофостном пути. Однако эритроциты обладают способностью метаболизировать фруктозу, лактозу, галактозу, нуклеотиды, в частности инозин.
В эритроцитах происходят реакции восстановления метгемоглобина. Как известно, в процессе диссоциации оксигемоглобина железо гемоглобина приобретает 2-х валентное ферросостояние. В ряде случаев О2 отрывается в виде супероксиданионрадикала, забирает один электрон у железа и превращает гемоглобин в метгемоглобин. В присутствии восстановленного глютатиона и аскорбиновой кислоты метгемоглобин восстанавливается до гемоглобина.
Гемоглобин эритроцитов. Основным белком эритроцитов, на долю которого приходится около 98 % всей массы белков цитоплазмы, является гемоглобин. Последний является гетеродимерным тетрамером, состоящим из четырех полипептидных цепей, соединенных с четырьмя молекулами гема. В свою очередь гем – это молекула протопорфина IX, связанная с анионом железа. Каждый тетрамер гемоглобина может обратимо связывать и транспортировать не более 4-х молекул кислорода. К числу основных гемоглобинов (Hb) взрослого человека относится гемоглобин А (от слова adultus – взрослый), на долю которого приходится 96–98 % и в составе которого имеются две α- и две β-цепи (α2β2).
Главным регулятором сродства Hb к О2 является промежуточный продукт гликолиза – 2-3дифосфоглицериновая кислота (2-3ДФГ). Увеличение образования 2-3ДФГ снижает сродство Hb к О2, что приводит к сдвигу кривой диссоциации оксигемоглобина вправо и к усиленному поступлению О2 в ткани. Сдвиг кривой вправо возникает также при увеличении температуры тела, возрастании уровня СО2 или на фоне развития метаболического ацидоза.
Фетальный гемоглобин слабо связывается с 2-3ДФГ и поэтому характеризуется более высокой кислородсвязывающей способностью по сравнению с HbA.
Гены гемоглобина: 2 гена α–цепей глобина расположены в 16-й паре хромосом, а 11 пара хромосом содержит пару генов γ-цепей и по одной копии δ- и β-цепей. Глобин синтезируется только в эритрокариоцитах и лишь в период созревания ретикулоцита из нормоцитов. На каждой стадии развития гены α-глобина и других глобинов координировано экспрессируются.
Избыточное образование одной цепи гемоглобина, происходящее при талассемии, приводит к преципитации белка в эритроците, повреждению клетки и её преждевременной элиминации клетками моноцитарно-макрофагальной системы.
Что является непосредственным источником энергии в организме адреналин эритроциты миоглобин
4.1. Транспорт кислорода
В сложных механизмах транспорта газов кровью и газообмена в тканях важная роль отводится эритроцитам, ответственным за доставку О2 к различным органам и удаление образующегося в процессе метаболизма СО2.
Эритроцит – безъядерная клетка, лишенная митохондрий, основным источником энергии для эритроцита служит глюкоза, метаболизируемая в гексозомонофосфатном шунте или цикле Эмбдена-Мейергофа. Транспорт О2 обеспечивается в значительной мере гемоглобином, состоящим из белка глобина и гема. Последний представляет собой комплексное соединение железа и порфирина. Глобин представляет собой тетрамер полипептидной цепи. Hb A (HbA) – основной гемоглобин взрослых содержит 2 – альфа и 2 – бета – цепи, Hb A2 – содержит две альфа и две дельта цепи.
Гем состоит из иона железа, встроенного в порфириновое кольцо. Ион железа гема обратимо связывает одну молекулу О2. С одной молекулой Hb максимально связываются 4 молекулы О2 с образованием оксигемоглобина.
Гем может подвергаться не только оксигенации, но и истинному окислению, когда железо становится из двухвалентного трехвалентным. Окисленный гем носит название гематина, а молекула гемоглобина становится метгемоглобином. В крови человека метгемоглобин находится в незначительных количествах, его уровень резко возрастает при отравлениях. Метгемоглобин не способен отдавать кислород тканям.
В норме метгемоглобин составляет менее 3% общего Hb крови. Основная форма транспорта О2 – в виде оксигемоглобина. Кислород транспортируется артериальной кровью не только в связи с гемоглобином, но и в растворенном виде. Принимая во внимание тот факт, что 1 г Hb может связать 1,34 мл О2, кислородная емкость крови в среднем у взрослого человека составляет около 200 мл/л крови. Одним из показателей кислородного транспорта является насыщение артериальной крови О2(Sa O2), равного отношению О2, связанного с Hb, к кислородной емкости крови:
SaO2=O2, связанного с Hb/O2 емкость крови* 100%.
В соответствии с кривой диссоциации оксигемоглобина насыщение артериальной крови кислородом в среднем составляет 97%, в венозной крови – 75%.
PaO2 в артериальной крови около 100 мм. рт. ст., а в венозной – около 40 мм. рт. ст.
Количество растворенного кислорода в крови пропорционально парциальному давлению О2 и коэффициэнту его растворимости.
Последний для О2 составляет 0,0031/100 мл крови/ 1 мм. рт. ст.. Таким образом, 100 мл крови при PaO2, равном 100 мм. рт. ст., содержит менее 0,31 мл O2.
Диссоциация оксигемоглобина в тканях обусловлена главным образом химическими свойствами гемоглобина, а также рядом других факторов – температурой тела, рН среды, р СО2.
При понижении температуры тела наклон кривой диссоциации оксигемоглобина возрастает, а при ее повышении – снижается, и соответственно снижается сродство Hb к О2.
При снижении рН, т.е. при закислении среды, сродство гемоглобина к О2 уменьшается. Увеличение напряжения в крови СО2 также сопровождается снижением сродства Hb к О2 и уплощением кривой диссоциации оксигемоглобина.
Известно, что степень диссоциации оксигемоглобина определяется содержанием в эритроцитах некоторых фосфорорганических соединений, главным из которых является 2,3 – ДФГ (2,3 дифосфоглицерат), а также содержанием в эритроцитах катионов. В случаях развития алкалозов, поглощение О2 в легких увеличивается, но в то же время затрудняется отдача кислорода тканями. При ацидозах наблюдается обратная картина.
4.2.Утилизация кислорода тканями
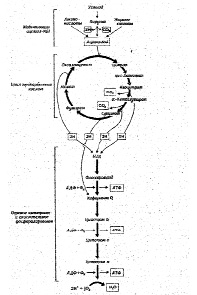
Тканевое или клеточное дыхание включает три стадии. На первой стадии пируват, аминокислоты и жирные кислоты окисляются до двухуглеродных фрагментов ацетильных групп, входящих в состав ацетилкофермента А. Последние на втором этапе окисления включаются в цикл лимонной кислоты, где происходит образование высокоэнергетических атомов водорода и высвобождение СО2 – конечного продукта окисления органических субстратов. На третьей стадии клеточного дыхания атомы водорода делятся на протоны (Н+) и «высокоэнергетические» электроны, передающиеся по дыхательной цепи на молекулярный О2 и восстанавливающие его до НО2. Перенос электронов сопряжен с запасом энергии в форме АТФ, т.е. с окислительным фосфорилированием (рис.6).
Касаясь патогенеза метаболических сдвигов, свойственных гипоксическим состояниям, следует отметить, что в организме человека более 90% всего потребляемого кислорода восстанавливается с участием цитохромоксидазы митохондрий, и лишь около 10% кислорода метаболизируется в тканях с участием оксигеназ: диоксигеназы и монооксигеназы.
Рис.6. Схема тканевого дыхания. Конечные продукты каждой стадии даны в рамке (Ленинджер А., 1999)
Наиболее многочисленны и сложны монооксигеназные реакции, протекающие в эндоплазматическом ретикулуме клеток при участии цитохрома Р-450 и обеспечивающие гидроксилирование субстрата (стероидных гормонов, лекарственных препаратов и различных др. соединений) и, как правило, его инактивацию.
Диоксигеназы катализируют реакции, в которых в молекулу органического субстрата включаются оба атома молекулы кислорода (например, реакция окисления катехола молекулярным кислородом с раскрытием кольца).
В реакциях, связанных с переносом электронов, т.е. в реакциях окисления-восстановления, где, как указывалось выше, используется более 90% потребляемого кислорода, атомы водорода, отщепленные дегидрогеназами от субстратов в цикле лимонной кислоты, передают свои электроны в цепь переноса электронов и превращаются также в Н +. Как известно, помимо 4 пар атомов водорода, поставляемых каждым оборотом цикла лимонной кислоты, образуются и другие атомы водорода, отщепленные дегидрогеназами от пирувата, жирных кислот и аминокислот в процессе их расщепления до Ацетил-СоА и других продуктов.
Таким образом, все атомы водорода, отщепляемые дегидрогеназами от субстратов, передают свои электроны в дыхательную цепь к конечному акцептору электронов – кислороду.
Скорость утилизации О2 в различных тканях различна. В среднем взрослый человек потребляет 250 мл О2 в 1 мин. Максимальное извлечение О2 из притекающей артериальной крови свойственно миокарду.
Кислород используется в клетках, в основном в метаболизме белков, жиров, углеводов, ксенобиотиков, в окислительно-восстановительных реакциях в различных субклеточных фракциях: в митохондриях, в эндоплазматическом ретикулуме, в реакциях липопероксидации, а также в межклеточном матриксе и в биологических жидкостях.
Коэффициент утилизации О2 в тканях равен отношению потребления О2 к интенсивности его доставки, широко варьирует в различных органах и тканях.
В условиях нормы минимальную потребность в О2 проявляют почки и селезенка, а максимальную потребность – кора головного мозга, миокард и скелетные мышцы, где коэффициент утилизации О2 колеблется от 0,4 до 0,6, а в миокарде до 0,7. При крайне интенсивной физической работе коэффициент утилизации О2 мышцами и миокардом может возрастать до 0,9.
Обмен дыхательных газов в тканях происходит в процессе свободной и облегченной диффузии. При этом О2 переносится по градиенту напряжения газа из эритроцитов и плазмы крови в окружающие ткани.
Одновременно происходит диффузия СО2 из тканей в кровь. На выход О2 из крови в ткани влияет диссоциация оксигемоглобина в эритроцитах, что обеспечивает так называемую облегченную диффузию О2. Интенсивность диффузионного потока О2 и СО2 определяется градиентом их напряжения между кровью и тканями, а также площадью газообмена, плотностью капилляров, распределением кровотока в микроциркуляторном русле. Интенсивность окислительных процессов в тканях определяется величиной критического напряжения О2 в митохондриях, которое в условиях нормы должно превосходить 0,1-1 мм рт. ст.
Соответствие доставки О2 к органам и тканям, возросшим потребностям в оксигенации обеспечивается на клеточном, органном уровнях за счет образования метаболитов изнашивания, а также при участии нервных, гормональных и гуморальных влияний.
Основная масса углекислого газа (СО2) образуется в организме как конечный продукт различных метаболических реакций и транспортируется к легким с кровью. Вдыхаемый воздух содержит лишь незначительное количество СО2.
Транспорт СО2 кровью осуществляется в 3-х состояниях: в виде аниона бикарбоната, в растворенной форме и в виде карбаминовых соединений.
СО2 хорошо растворяется в плазме крови и в артериальной крови, около 5% от общей двуокиси углерода содержится в крови в растворенной форме.
Третьей формой транспорта СО2 кровью являются карбаминовые соединения, образованные взаимодействием СО2 с концевыми группами белков крови преимущественно с гемоглобином:
Карбаминовые соединения составляют около 5% от общего количества СО2, транспортируемого кровью.
В оксигенированной артериальной крови напряжение СО2 составляет 40 мм. рт. ст., а в венозной крови Рv СО2 равно 46 мм. рт. ст.
4.4.Связывание гемоглобина с окисью углерода