Что является твердым раствором
Твёрдый раствор
Твёрдые растворы — фазы переменного состава, в которых атомы различных элементов расположены в общей кристаллической решётке.
Могут быть неупорядоченными (с хаотическим расположением атомов), частично или полностью упорядоченными. Экспериментально упорядоченность определяют, главным образом, рентгеновским структурным анализом.
Способность образовывать твёрдые растворы свойственна всем кристаллическим твёрдым телам. В большинстве случаев она ограничена узкими пределами концентраций, но известны системы с непрерывным рядом твёрдых растворов (например, Cu—Au, Ti—Zr, GaAs—GaP). По существу, все кристаллические вещества, считающиеся чистыми, представляют собой твёрдые растворы с очень малым содержанием примесей.
Различают три вида твёрдых растворов:
Согласно полуэмпирическим правилам Юм-Розери, непрерывный ряд твёрдых растворов замещения в металлических системах образуются лишь теми элементами, которые, во-первых, имеют близкие по размерам атомные радиусы (отличающиеся не более чем на 15 %) и, во-вторых, находятся не слишком далеко друг от друга в электрохимическом ряду напряжений. При этом элементы должны иметь один и тот же тип кристаллической решётки. В твёрдых растворах на основе полупроводников и диэлектриков, благодаря более «рыхлым» кристаллическим решёткам образование твёрдых растворов замещения возможно и при большем различии атомных радиусов.
Если атомы компонентов существенно различаются по размерам или электронной структуре, возможно внедрение атомов одного элемента в междоузлия решётки, образованной другим элементом. Подобные твёрдые растворы часто образуются при растворении неметаллов (B, H2, O2, N2, C) в металлах.
Твёрдые растворы вычитания, возникающие за счёт появления в кристаллической решётке вакантных узлов, образуются при растворении одного из компонентов в химическом соединении и характерны для нестехиометрических соединений.
Природные минералы часто представляют собой твёрдые растворы (см. Изоморфизм в кристаллах). Образование твёрдых растворов при легировании элементов и соединений имеет большое значение в производстве сплавов, полупроводников, керамики, ферритов.
Твёрдые растворы — основа всех важнейших конструкционных и нержавеющих сталей, бронз, латуней, алюминиевых и магниевых сплавов высокой прочности. Свойства твёрдых растворов регулируют их составом, термической или термомеханической обработкой. Легированные полупроводники и многие сегнетоэлектрики, являющиеся основой современной твердотельной электроники, также являются твёрдыми растворами.
При распаде твёрдых растворов сплавы приобретают новые свойства. Наиболее ценными качествами обладают сплавы с очень тонкой неоднородностью — так называемые дисперсионно-твердеющие, или стареющие твёрдые растворы. Дисперсионное твердение может наблюдаться и при распаде твёрдых растворов на основе соединений, например, нестехиометрических шпинелей.
ТВЕРДЫЕ РАСТВОРЫ
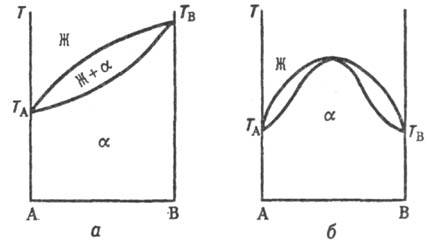
Типы диаграмм состояния. На диаграмме состояния двойных систем в координатах т-ра-состав образованию непрерывных твердых растворов отвечают три типа линий ликвидуса и солидуса (рис. 1, а, б и в), отграничивающих области существования жидкой фазы (расплава) и твердого раствора (Ж и a соотв.) и область сосуществования обеих фаз (Ж + a ). Тип б встречается крайне редко, гл. обр. в случае оптич. изомеров орг. в-в. В системах с непрерывными твердыми растворами, согласно принципу соответствия (см. Физико-химический анализ), должна быть только одна кривая ликвидуса и одна кривая солидуса. Поэтому в точке минимума или максимума происходит плавный переход одной части кривой в другую.
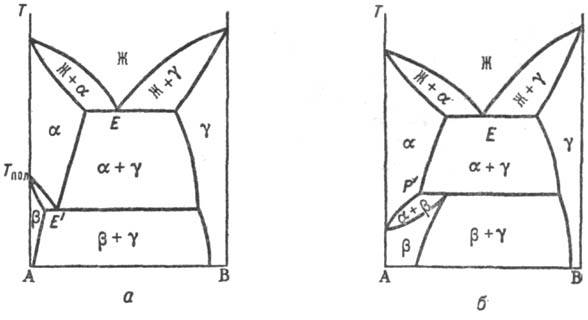
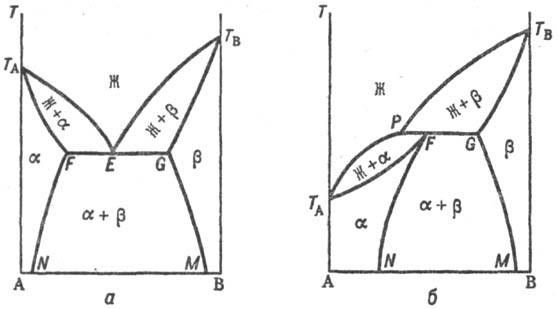
Рис. 2. Диаграммы состояния двойных систем с ограниченными по составу твердыми р-рами a и b : а-система с эвтектич. точкой Е; б-система с пери-тектич. точкой Р. Остальные обозначения те же, что и на рис.’1.
Распад твердых растворов. Предельная концентрация твердого раствора зависит от т-ры и давления. При понижении т-ры взаимная р-римость компонентов, как правило, понижается. Влияние давления неоднозначно, для большинства систем повышение давления приводит к уменьшению взаимной р-римости.
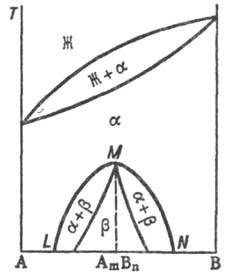
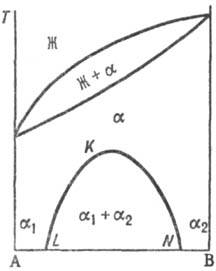
При охлаждении однородного р-ра ниже критич. т-ры р-римости (смешения) (точка К) образуется двухфазная система, состоящая из несмешивающихся твердых растворов a 1 и a 2 (рис. 3), составы к-рых изменяются с т-рой по линиям KL и KN соответственно. Др. тип распада твердого раствора a наблюдается, если компоненты А и В могут образовать хим. соед. А m В n (рис. 4), характеризующееся упорядоченным расположением частиц (атомов или ионов) в кристаллической решетке, в отличие от статистического беспорядка в расположении частиц, характерного для твердых растворов. На основе А m В n образуется твердый раствор b с компонентами А и В. Превращение в упорядоченную фазу (сегрегация) может происходить как фазовый переход II рода. При этом выше температуры перехода вероятности заполнения к.-л. кристаллографич. позиции разл. атомами (ионами) равны, а ниже точки перехода различаются.
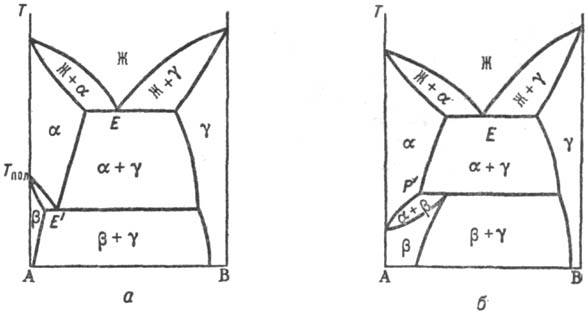
Рис. 5. Диаграммы состояния двойных систем с полиморфным превращением твердого р-ра по эвтектоидному типу (а) и по перитеггоидному типу (б).
Типы твердых растворов. В твердых растворах замещения растворенное в-во замещает исходное-атом на атом, ион на ион или молекула на молекулу. При этом число частиц (атомов, молекул) в элементарной кристаллич. ячейке остается постоянным. Один из важнейших факторов, определяющих возможность образования твердых растворов замещения,-это размеры замещающих друг друга атомов (ионов, молекул). Согласно правилу Гольдшмидта, для образования широких по составу областей гомогенности твердых растворов при т-рах, далеких от т-р плавления компонентов, разница D r в ионных радиусах замещающих друг друга ионов не должна превышать 15%, т.е. отношение D r/r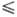
Т вердые растворы как внедрения, так и замещения м.б. неупорядоченными-со статистич. распределением атомов в решетке либо частично или полностью упорядоченными, с определенным расположением атомов разного сорта относительно друг друга. Упорядоченные твердые растворы иногда наз. сверхструктурами. В нек-рых случаях в твердых растворах атомы одного сорта могут образовывать скопления, к-рые, в свою очередь, могут определенным образом упорядочиваться или ориентироваться в данном направлении. Т. обр., твердые растворы, будучи истинно гомогенным в макроскопич. масштабе, т.е. система, находящаяся в термодинамич. равновесии, м.б. неоднородной при рассмотрении на микроуровне. Эксперим. данные об упорядочении твердых растворов получают в осн. при использовании рентгеновского структурного анализа. Упорядоченность твердых растворов и ее изменения в процессах старения важны для материаловедения (см. Сплавы).
числа атомов в элементарной кристаллич. ячейке оптим. размер иона-заместителя не совпадает с размером замещаемого иона. А.Е.Ферсман (1933) полагал, что наиболее благоприятна для образования твердых растворов ситуация, когда ион-заместитель, несущий больший электрический заряд, имеет и больший радиус. Однако часто, напр. при образовании твердых растворов сульфатов двухвалентных металлов в сульфатах Na или К, наблюдается обратная зависимость. Вообще размерный фактор иногда очень сильно, а иногда относительно слабо влияет на ширину областей гомогенности таких твердых растворов, в зависимости от природы соединения-основы.
Нек-рые гетеровалентные твердые растворы (напр., КС1О 4 в BaSO 4 или KBF 4 в SrSO 4 ) относятся к числу т. наз. аномальных твердых растворов, в к-рых наблюдается ниж. температурный предел смешения или при понижении концентрации коэф. сокрис-таллизации стремится к 0 (см. Соосаждение). Это объясняется замещением отдельных блоков элементарных ячеек, так что образуется не истинный, а микродисперсный («коллоидный») твердый раствор.
Выяснение механизма образования твердых растворов требует применения физ. методов исследования, в частности рентгеновского структурного анализа. К числу наиб. часто применяемых методов исследования твердых растворов относится рентгенография порошков. Параметры кристаллич. решетки твердого раствора линейно зависят от состава (Л. Вегард, 1921); реально наблюдаются отклонения от этого правила. Широко используют также измерения плотности; согласно правилу Ретгерса (1889), плотность, а также молярный объем аддитивно зависят от концентрации. Измерение т-р фазовых переходов (см. Термография) позволяет строить диаграммы р-римости с их последующим физико-химическим анализом.
Для твердых растворов, как и для жидких растворов, применяют термодинамические модели и рассматривают идеальные твердые растворы, в к-рых энтальпия смешения равна нулю, регулярные, субрегулярные твердые растворы (см. Растворы неэлектролитов).
Природные кристаллич. в-ва (минералы) и синтетич. кристаллы представляют собой многокомпонентные твердые растворы; даже в-ва высокой чистоты с очень малым содержанием примесей являются твердыми растворами. Как было показано Н. С. Курна-ковым и С.Ф.Жемчужным (1906), св-ва твердых растворов отличаются (иногда очень сильно) от св-в чистых компонентов. В частности, при образовании твердых растворов на основе металла возрастает твердость и уменьшается электропроводность в-ва. Изменение состава твердых растворов позволяет изменять в широких пределах св-ва сплавов, полупроводниковых материалов, ионных проводников, ферритов, лазерных материалов и т. п. и получать материалы с нужными св-вами (см. Легирование). Св-ва
Т вердые растворы могут изменяться в результате термич. обработки, к-рая позволяет получать твердые растворы либо в неравновесном состоянии (закалка), либо в состоянии, в той или иной степени приближенном к равновесному (отжиг, отпуск). Термин «твердые растворы» предложен Я. Вант-Гоффом в 1890.
Лит.: Макаров Е. С., Изоморфизм атомов в кристаллах, М., 1973; Хачатурян А. Г., Теория фазовых превращений и структура твердых растворов, М., 1974; Урусов В. С., Теория изоморфной смесимости, М., 1977; его же, Теоретическая кристаллохимия, М., 1987; Федоров П. П., Соболев Б. П., Федоров П. И., «Кристаллография», 1981, т. 26, № 3, с. 512-20; Китайгородский А. И., Смешанные кристаллы, М., 1983. П.И. Федоров,
твердые растворы
ТВЕРДЫЕ РАСТВОРЫ
однородные (гомогенные) крис-таллич. фазы переменного состава; образуются в двойных или многокомпонентных системах. Если компоненты системы неограниченно растворимы друг в друге, они образуют непрерывный ряд Т. р. Чаще, однако, концентрация растворенного вещества не может превышать некоторое предельное значение и существование Т. р. ограничено некоторыми областями составов (области гомогенности). Т. р. являются мн. метал-лич. сплавы и неметаллич. системы — минералы, стекла, полупроводники, ферриты.
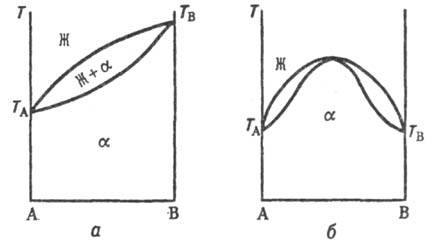
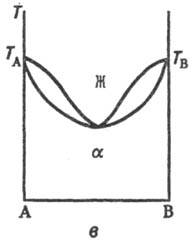
Типы диаграмм состояния. На диаграмме состояния двойных систем в координатах температура-состав образованию непрерывных Т. р. отвечают три типа линий ликвидуса и солидуса (рис. 1, а, б и в), отграничивающих области существования жидкой фазы (расплава) и Т. р. (Ж и α соотв.) и область сосуществования обеих фаз (Ж + α). Тип б встречается крайне редко, гл. обр. в случае оптич. изомеров орг. веществ. В системах с непрерывными Т. р., согласно принципу соответствия ( см. физико-химический анализ), должна быть только одна кривая ликвидуса и одна кривая солидуса. Поэтому в точке минимума или максимума происходит плавный переход одной части кривой в другую.
Рис. 1. Диаграммы состояний двойных систем в координатах температура Т-состав А-В: Ж-жидкая фаза (расплав), α-непрерывный твердый раствор, ТА и TB-температуры плавления чистых компонентов.
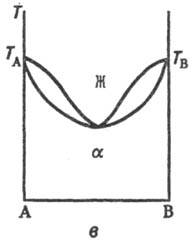
Если компоненты образуют только ограниченные Т. р., возможны два типа диаграмм состояния (рис. 2), на которых Т. р. компонента А в В, обозначаемые как α-p-p, образуются лишь до определенной концентрации В, а Т. р. В в А (раствор-р)-до определенной концентрации А. В первом случае Т.р. образуют эвтектику, т. е. существует точка E нонва-риантного равновесия трех фаз: жидкого расплава, состав которого отвечает точке E, твердого α-раствора, концентрация которого соответствует точке F, и твердого β-p-pa, концентрация которого отвечает точке G, причем точка E лежит между точками состава этих Т. р. Ниже температуры ТЕ остаются в равновесии два Т. р. α и β, составы которых по мере снижения температуры изменяются в соответствии с ходом линий GM и FN (рис. 2, а). Образование подобных Т. р. наблюдается, напр., в системах Cu-Ag, Pb-Sn. Во втором случае Т. р. Образуют перитектику-нонвариантную точку также трехфазного равновесия, но расположенную по одну сторону от точек состава Т. р. (точка Р, рис. 2,б). Примером системы пе-ритектич. типа может служить Cd-Hg.
Рис. 2. Диаграммы состояния двойных систем с ограниченными по составу твердыми растворами α и β: а — система с эвтектич. точкой Е; б-система с пери-тектич. точкой Р. Остальные обозначения те же, что и на рис.’1.
На линиях ликвидуса ограниченных Т. р. иногда встречаются экстремальные точки-минимум или (чаще) максимум. Последнее характерно для солевых и оксидных систем только в случае гетеровалентных Т. р. (см. ниже) с переменным числом ионов в элементарной ячейке, напр. Т. р. Y2O3 в ZrO2. Повышение температуры плавления при образовании такого Т. р., напр. DyF3 в PbF2, м. б. настолько сильным, что температура плавления эвтектич. смеси (957 °C) становится выше температуры плавления компонента (для PbF2 824 °C).
Распад Т. р. Предельная концентрация Т. р. зависит от температуры и давления. При понижении температуры взаимная растворимость компонентов, как правило, понижается. Влияние давления неоднозначно, для большинства систем повышение давления приводит к уменьшению взаимной растворимости.
Рис. 3. Распад непрерывного твердого раствора с образованием двухфазной системы. Жирная линия — бинодаль, отделяющая область существования твердого раствора от области сущестзования двухфазной системы.
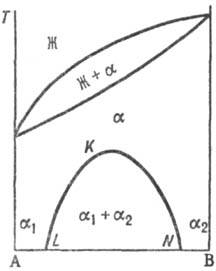
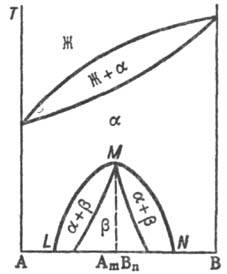
При охлаждении однородного раствора ниже критич. температуры растворимости (смешения) (точка К) образуется двухфазная система, состоящая из несмешивающихся Т. p. α1 и α2 (рис. 3), составы которых изменяются с температурой по линиям KL и KN соответственно. Др. тип распада Т. р. α наблюдается, если компоненты А и В могут образовать хим. соед. АmВn (рис. 4), характеризующееся упорядоченным расположением частиц (атомов или ионов) в кристаллической решетке, в отличие от статистического беспорядка в расположении частиц, характерного для Т. р. На основе АmВn образуется Т. р. β с компонентами А и В. Превращение в упорядоченную фазу (сегрегация) может происходить как фазовый переход II рода. При этом выше температуры перехода вероятности заполнения к.-л. кристаллографич. позиции разл. атомами (ионами) равны, а ниже точки перехода различаются.
Рис. 4. Распад непрерывного твердого раствора с образованием хим. соед. АmВn. Жирная линия — температура начала кристаллизации твердого раствора β на основе АmВn.
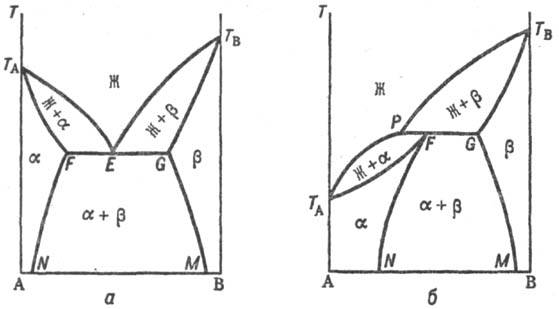
Полиморфизм. С полиморфным превращением вещества, на основе которого образуется Т. р;, всегда связано и превращение Т. р. На рис. 5 приведены диаграммы состояния систем с наиб. часто встречающимися вариантами полиморфного превращения. При эвтектоидном превращении (рис. 5, а) т-pa трехфазного равновесия (точка E’) T. р. α и β, образующихся на основе двух модификаций компонента А, с Т. р. γ на основе компонента В расположена ниже температуры Тн полиморфного превращения, а область гомогенности Т. р. на основе низкотемпературной модификации (β) уже, чем на основе высокотемпературной (α); при перитектоидном (рис. 5, б)-наоборот.
Рис. 5. Диаграммы состояния двойных систем с полиморфным превращением твердого раствора по эвтектоидному типу (а) и по перитеггоидному типу (б).
Типы Т.р. В Т.р. замещения растворенное вещество замещает исходное-атом на атом, ион на ион или молекула на молекулу. При этом число частиц (атомов, молекул) в элементарной кристаллич. ячейке остается постоянным. Один из важнейших факторов, определяющих возможность образования Т. р. замещения,-это размеры замещающих друг друга атомов (ионов, молекул). Согласно правилу Гольдшмидта, для образования широких по составу областей гомогенности Т. р. при температурах, далеких от температур плавления компонентов, разница Δr в ионных радиусах замещающих друг друга ионов не должна превышать 15%, т. е. отношение Δr/r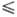
Размерный фактор не всегда является решающим. Например, NaCl и PbS не образуют Т. р., хотя их размерные факторы (радиусы ионов, межатомные расстояния и др.) близки. Второй необходимый фактор-хим. подобие компонентов, в частности близость типа хим. связи. В качестве параметра, определяющего возможность образования Т. р. замещения, используют различие в степени ионности связи, иногда — разность электроотрицательностей атомов замещающих друг друга элементов. Предложено использовать в качестве характеристик хим. подобия температуры плавления хим. соед. или энергии 17 кристаллич. решеток. Для образования непрерывных Т. р. замещения требуется, чтобы ΔTпл/Tпл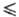
В Т.р. внедрения атомы (молекулы) растворенного вещества располагаются в междоузлиях кристаллич. решетки, образованной веществом-основой Т. р., или в стехиометрич. вакансиях. В результате число атомов (молекул) в элементарной ячейке кристалла увеличивается. Классич. пример Т. р. внедрения-растворы неметаллов H, N, С, О в металлах. В Т. р. на основе In2Те3, обладающего дефектной структурой типа сфалерита, примесные атомы Sb, Bi, In и др. располагаются в стехиометрич. вакансиях. Т. р. внедрения являются растворы воды в цеолитах-молекулы воды располагаются в полостях структуры осн. вещества. При образовании Т. р. внедрения не требуется близости типа хим. связи, а размерный фактор может играть роль, противоположную Т. р. замещения, а именно: макс. взаимной растворимости компонентов благоприятствует наиб. разница их атомных радиусов.
В Т.р. вычитания число атомов в элементарной ячейке кристалла уменьшается по сравнению с чистым компонентом. Такие Т. р. часто образуются на основе нестехиомет-рич. соединении. Так, в сульфиде железа Fe1-xS, который можно рассматривать как Т. p. S в FeS, в действительности имеются своб. октаэдрич. пустоты — катионные вакансии-вследствие того, что часть атомов железа имеет степень окисления III. Т. р. калия в KCl-также Т. р. вычитания. В его решетке существуют анионные вакансии, в которых локализуются электроны, что обеспечивает электрич. нейтральность кристаллич. решетки. В пределах области гомогенности одной и той же фазы могут наблюдаться как Т. р. внедрения, так и Т. р. вычитания, поэтому иногда эти типы Т. р. объединяют под назв. «Т. р. с переменным числом атомов в элементарной ячейке».
Т. р. как внедрения, так и замещения м. б. неупорядоченными-со статистич. распределением атомов в решетке либо частично или полностью упорядоченными, с определенным расположением атомов разного сорта относительно друг друга. Упорядоченные Т.р. иногда наз. сверхструктурами. В некоторых случаях в Т. р. атомы одного сорта могут образовывать скопления, которые, в свою очередь, могут определенным образом упорядочиваться или ориентироваться в данном направлении. Таким образом, Т. р., будучи истинно гомогенным в макроскопич. масштабе, т. е. система, находящаяся в термодинамич. равновесии, м. б. неоднородной при рассмотрении на микроуровне. Эксперим. данные об упорядочении Т. р. получают в осн. при использовании рентгеновского структурного анализа. Упорядоченность Т. р. и ее изменения в процессах старения важны для материаловедения ( см. сплавы).
Некоторые гетеровалентные Т. р. ( напр., KClO4 в BaSO4 или KBF4 в SrSO4) относятся к числу т. наз. аномальных Т. р., в которых наблюдается ниж. температурный предел смешения или при понижении концентрации коэф. сокрис-таллизации стремится к 0 ( см. соосаждение). Это объясняется замещением отдельных блоков элементарных ячеек, так что образуется не истинный, а микродисперсный («коллоидный») Т. р.
Выяснение механизма образования Т. р. требует применения физ. методов исследования, в частности рентгеновского структурного анализа. К числу наиб. часто применяемых методов исследования Т. р. относится рентгенография порошков. Параметры кристаллич. решетки Т. р. линейно зависят от состава (Л. Вегард, 1921); реально наблюдаются отклонения от этого правила. Широко используют также измерения плотности; согласно правилу Ретгерса (1889), плотность, а также молярный объем аддитивно зависят от концентрации. Измерение температур фазовых переходов ( см. термография) позволяет строить диаграммы растворимости с их последующим физико-химическим анализом.
Для Т. р., как и для жидких растворов, применяют термодинамические модели и рассматривают идеальные Т. р., в которых энтальпия смешения равна нулю, регулярные, субрегулярные Т. р. ( см. растворы неэлектролитов).
Природные кристаллич. вещества (минералы) и синтетич. кристаллы представляют собой многокомпонентные Т. р.; даже вещества высокой чистоты с очень малым содержанием примесей являются Т. р. Как было показано Н. С. Курна-ковым и С.Ф.Жемчужным (1906), свойства Т.р. отличаются (иногда очень сильно) от свойств чистых компонентов. В частности, при образовании Т. р. на основе металла возрастает твердость и уменьшается электропроводность вещества. Изменение состава Т. р. позволяет изменять в широких пределах свойства сплавов, полупроводниковых материалов, ионных проводников, ферритов, лазерных материалов и т. п. и получать материалы с нужными свойствами ( см. легирование). Свойства
Т. р. могут изменяться в результате термич. обработки, которая позволяет получать Т. р. либо в неравновесном состоянии (закалка), либо в состоянии, в той или иной степени приближенном к равновесному (отжиг, отпуск). Термин «Т. р.» предложен Я. Вант-Гоффом в 1890.
Лит.: Макаров Е. С., Изоморфизм атомов в кристаллах, М., 1973; Хачатурян А. Г., Теория фазовых превращений и структура твердых растворов, М., 1974; Урусов В. С., Теория изоморфной смесимости, М., 1977; его же, Теоретическая кристаллохимия, М., 1987; Федоров П. П., Соболев Б. П., Федоров П. И., «Кристаллография», 1981, т. 26, № 3, с. 512–20; Китайгородский А. И., Смешанные кристаллы, М., 1983.