десквамация децидуальной оболочки что это
Десквамация децидуальной оболочки что это
Децидуальная оболочка представляет собой трансформированный в связи с беременностью функциональный слой эндометрия. К моменту имплантации эндометрий находится в секреторной фазе. Он состоит из двух слоев: компактного и спонгиозного. Компактный слой, обращенный в полость матки, содержит выводные протоки маточных желез и клетки стромы эндометрия, превратившиеся во время беременности в децидуальный спонгиозный слой в основном состоит из желез.
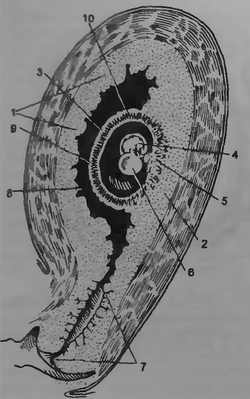
В соответствии с локализацией плодного яйца в децидуальной оболочке можно различить три части:
• выстилающая полость матки (decidua parietalis);
• покрывающая плодное яйцо со стороны полости матки (decidua capsularis);
• расположенная между плодным яйцом и стенкой матки (decidua basalis). Указанные взаимоотношения различных частей децидуальной оболочки представлены на рис. 3.7.
В процессе роста плодного яйца decidua parietalis и decidua capsularis растягиваются, истончаются и приближаются друг к другу. На 4—5-м месяце беременности плодное яйцо занимает уже всю полость матки, и decidua parietalis сливается с decidua capsularis. Наоборот, decidua basalis значительно гипертрофируется и превращается в материнскую часть плаценты. В этой части плаценты находятся многочисленные ворсины хориона, вокруг которых формируется межворсинчатое пространство.
Децидуальная оболочка является для плода питательным и защитным слоем: трофическая функция ее в основном осуществляется на ранних этапах внутриутробного развития, защитная роль наиболее полно проявляется высокой фагоцитарной активностью. Децидуальная ткань лизирует микроорганизмы и инактивирует их токсины, принимает также участие в синтезе углеводов, липидов и белков В ней происходит синтез пролактина и простагландинов. Таким образом, децидуальной оболочке принадлежит очень важная роль в имплантации и дальнейшем развитии эмбриона и плода.
Десквамация децидуальной оболочки что это
Проделав путь по маточной трубе в течение 4 сут, плодное яйцо на стадии морулы попадает в матку, где превращается в бластоцисту (рис. 3.4). Стадия бластоцисты характеризуется тем, что блас-томеры подвергаются определенным изменениям. Часть бластомеров, более крупных по своим размерам, образует так называемый эмбриобласт, из которого в дальнейшем развивается эмбрион. Другая часть клеток, более мелких и располагающихся по периферии плодного яйца, образует питательную оболочку — трофобласт. В дальнейшем наиболее развитая часть трофобласта превращается в плаценту. В полости матки бластоциста приближается к месту имплантации (нидации) (рис. 3.5, а,б). Локализация имплантации имеет свои закономерности и, по-видимому, в значительной степени определяется местными особенностями эндометрия. Обычно бластоциста имплантируется в области передней или задней стенки матки.
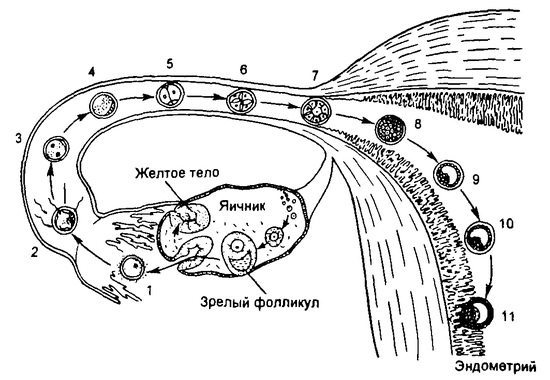
Затем начинается погружение бластоцисты в эндометрий, который к этому времени превращается в децидуальную оболочку (рис. 3.5, в,г).
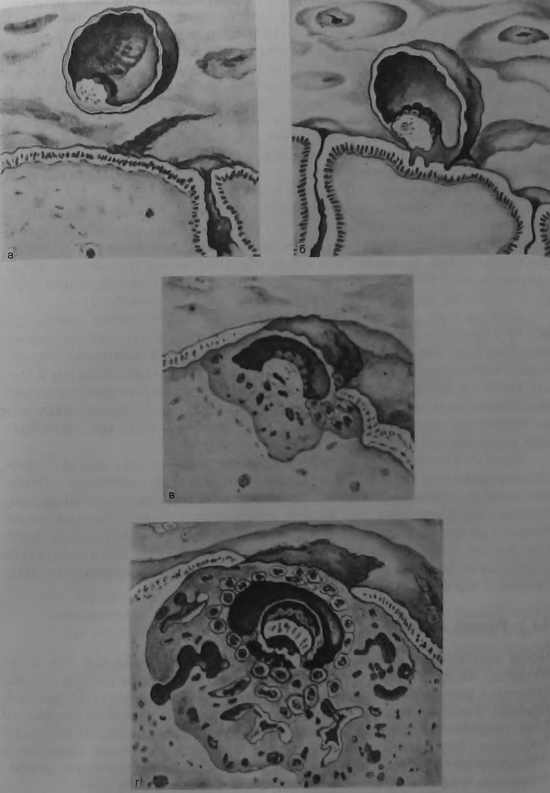
Децидуальная оболочка представляет собой видоизмененный функциональный слой эндометрия. К моменту имплантации оплодотворенной яйцеклетки слизистая оболочка матки находится в секреторной фазе, железы пилообразно изменены и заполнены секретом, клетки стромы имеют округ-тын вид и содержат большое количество гликогена, липидов, нейтральных мукополисахаридов, солей и микроэлементов, ферментов и их ингибиторов, иммуноглобулинов и многие другие биологически активные соединения, необходимые для жизнедеятельности зародыша.
Процесс имплантации в первую очередь связан с гормональными факторами. Ведущая роль принадлежит половым (стероидным) гормонам. Во время беременности происходит развитие и активное функционирование желтого тела яичника, возникшего на месте лопнувшего фолликула. Желтое тело секретирует большое количество прогестерона и несколько меньшее — эстрогенов. Эти половые гормоны через специфические стероидные рецепторы, находящиеся в эндометрии, оказывают выраженное воздействие на секреторные преобразования слизистой оболочки матки и процессы ее де-цидуализации. Кроме стероидных, определенную роль в имплантации играют и некоторые другие гормоны (пролактин, глюкокортикоиды).
Децидуальная ткань как своеобразный эндокринный орган имеет прямое отношение к имплантации и дальнейшим стадиям постимплантацион-ного развития зародыша. Установлено, что эндометрий женщины вырабатывает иммунореактивный пролактин. Он начинает секретироваться с 9-го дня после овуляции, при этом во время беременности продукция тканевого пролактина значительно повышается, поэтому в настоящее время некоторые исследователи склонны рассматривать децидуальную ткань как своеобразный эндокринный орган.
Процесс имплантации, который в среднем продолжается около 2 дней, сопровождается не только значительными изменениями клеточных элементов желез и стромы эндометрия, но и выраженными гемодинамическими сдвигами местного характера. Вблизи места имплантации бластоцисты отмечается расширение кровеносных сосудов и образование синусоидов, пред-ставляющих собой расширенные капилляры и венулы. Этим процессам принадлежит большая роль в процессах обмена между материнским организмом и зародышем.
ДЕЦИДУАЛЬНАЯ ОБОЛОЧКА
ДЕЦИДУАЛЬНАЯ ОБОЛОЧКА [membrana decidua (LNH), s. caduca, s. decidua, s. decidua graviditatis; син. отпадающая оболочка] — слизистая оболочка матки, подвергающаяся определенным преобразованиям при беременности и отпадающая после родов (выделяется из полости матки вместе с лохиями). В Д. о. различают три отдела: 1) базальная Д. о. [decidua basalis (LNH), s. decidua serotina]— часть слизистой оболочки, расположенная между плодным пузырем и мышечной оболочкой матки; 2) капсульная Д. о. [decidua Capsularis (LNH), s. reflexa] — часть слизистой оболочки, отделяющая плодный пузырь от полости матки; 3) париетальная Д. о. [decidua parietalis (LNH), s. decidua vera] — вся остальная часть слизистой оболочки матки (см.).
В начале беременности Д. о. представляет собой утолщенную (до 1 см) слизистую оболочку с сильно разросшимися железами и крупными содержащими гликоген децидуальными клетками (cellulae deciduales). Ряд авторов считает, что питательные вещества (гликоген), содержащиеся в децидуальных клетках, служат для питания яйца на ранней стадии его развития в матке.
Париетальная децидуальная оболочка начиная с VI мес. беременности сдавливается растущим плодом и подвергается обратному развитию, эпителий на ее поверхности и в железах исчезает (кроме самых глубоких их отделов). Ампулообразные концы желез, сдавливаясь, образуют щели.
Капсульная децидуальная оболочка, растянутая плодным пузырем, начинает атрофироваться с конца II мес. беременности, в последующие месяцы беременности прижимается растущим плодом к париетальной Д. о. и атрофируется.
Базальная децидуальная оболочка участвует в образовании материнской, или маточной, части плаценты (см.). Слои базальной Д. о., обращенные к плоду (компактный и губчатый), подвергаются разрушению ворсинами хориона, и на их месте образуются лакуны, заполненные кровью. Глубокие ее слои образуют базальную пластинку, от к-рой отходят к хориону перегородки, делящие заполненные кровью пространства на отдельные камеры. Краевая зона базальной Д. о. образует замыкающую пластинку плаценты. С V мес. беременности в ней появляются гигантские много-ядерные клетки трофобластического происхождения, специфические для плаценты. Децидуальные клетки в слизистой оболочке матки появляются также в конце второй половины менструального цикла — так наз. менструальная Д. о. (decidua menstrualis), отпадающая в период менструации. Децидуальные клетки развиваются не только при маточной беременности, но и при ряде патол, состояний женского полового аппарата, а также внематочной беременности, что может быть одним из ее диагностических признаков (см. Внематочная беременность).
Медикаментозное прерывание малых сроков беременности
Одной из наиболее важных проблем современного здравоохранения является сохранение репродуктивного здоровья женщин. Столь пристальное внимание к этой проблеме связано, в первую очередь, с демографической ситуацией, сложившейся в России. Предпринимаемые ме
Одной из наиболее важных проблем современного здравоохранения является сохранение репродуктивного здоровья женщин. Столь пристальное внимание к этой проблеме связано, в первую очередь, с демографической ситуацией, сложившейся в России. Предпринимаемые меры, к сожалению, не повышают рождаемость в нашей стране на должный уровень. Основным путем решения проблемы сохранения детородной функции женщин являются уменьшение числа медицинских и криминальных абортов, профилактика нежелательной беременности.
В Российской Федерации аборт продолжает оставаться распространенным методом регулирования рождаемости и планирования семьи (В. И. Кулаков, 1993). По данным медицинской статистики, ежегодно около 15—20 тыс. женщин прерывают беременность. До последнего десятилетия применялись хирургические методы прерывания беременности, такие, как вакуум-кюретаж, вакуум-аспирация («мини-аборт») и традиционный кюретаж.
Вакуум-кюретаж — наиболее распространенный метод искусственного прерывания беременности во многих странах мира, в том числе и в России. Преимуществами этой процедуры являются простота и непродолжительность процедуры полной эвакуации содержимого полости матки через небольшое расширение шейки матки. Операция легко выполнима под местной анестезией в амбулаторных условиях.
При применении указанного метода прерывания беременности возможны аллергические реакции на используемые лекарственные препараты, перфорация или атония матки, судороги или остановка сердца и т. д.
Искусственное прерывание беременности методом вакуум-аспирации в целях регулирования рождаемости приобрело большое распространение во многих странах мира. Широкое применение этого метода обусловлено тем, что проведение операции возможно в амбулаторных условиях при помощи относительно простой медицинской техники, при соблюдении правил асептики и антисептики, без применения местной анестезии. После операции пациенты возвращаются к обычной жизнедеятельности через 1 ч. Несмотря на преимущество данного метода, некоторую сложность представляют диагностирование начальных сроков беременности и исключение внематочной беременности.
Традиционный кюретаж представляет собой операцию искусственного прерывания беременности, которая в настоящее время используется все реже. Медицинский аборт часто приводит к серьезным осложнениям в раннем послеоперационном периоде (кровотечение, инфекция, остатки плодного яйца и т. д.). В более поздние сроки развиваются воспалительные заболевания женских половых органов, невынашивание беременности, бесплодие, внематочная беременность. Осложненное течение последующей беременности, родов и послеродового периода (В. И. Кулаков и соавт., 1991; Т. Н. Мельник и соавт., 2001) неблагоприятно влияет на состояние плода и новорожденного (Т. С. Чередниченко, 2001).
Среди современных щадящих способов прерывания незапланированной беременности можно упомянуть медикаментозный метод. Его разработка началась еще в 70-е гг. ХХ столетия. В этот период во Франции была реализована программа создания стероидов с антигормональным действием. В 1980 г. появился мифепристон, представляющий собой синтетический стероидный препарат для перорального применения и являющийся антагонистом прогестерона и глюкокортикоидов.
Медикаментозный метод прерывания незапланированной беременности с помощью препарата мифепристон (мифегин, пенкрофтон) применяется за рубежом с 1980 г., а в России — с 1998 г. (Е. Н. Караева и соавт., 1999).
Мифепристон (мифегин, пенкрофтон, мифепрекс) — синтетическое стероидное антипрогестогенное средство (блокирует действие прогестерона на уровне рецепторов). Механизм действия препарата основан на взаимодействии с гормонсвязывающим доменом рецептора клеток-мишеней, что вызывает «неэффективную» конформацию и блокаду эффектов природного стероида.
Мифепристон повышает сократительную способность миометрия, стимулируя высвобождение интерлей- кина-8 в хориодецидуальных клетках, повышая чувствительность миометрия к простагландинам (для усиления эффекта применяется в сочетании с синтетическими аналогами простагландинов (Е. Н. Караева и соавт., 1999)). В результате действия препарата происходят десквамация децидуальной оболочки и выведение плодного яйца.
После однократного приема внутрь 600 мг мифепристона максимальная концентрация достигается через 1,5 ч. Абсолютная биодоступность препарата составляет 69%. В плазме крови мифепристон на 98% связывается с белками: альбумином и кислым альфа-1-гликопротеином. После фазы распределения выведение сначала происходит медленно, концентрация уменьшается в 2 раза между 12—72 ч, затем процесс выведения ускоряется. Период полувыведения составляет 18 ч.
При патоморфологическом исследовании материала выкидышей (Т. Н. Мельник и соавт., 2001) после применения мифепристона обнаружили, что линия отторжения формирующейся плаценты проходила по терминальным окончаниям якорных ворсин и остаточным фрагментам базальной оболочки, состоящей из пластов цитотрофобласта и децидуальных клеток. В полости эмбрионального мешка обнаруживались сохраненные фрагменты эмбриона, амниотической оболочки и желточного мешка. Отмечалось полное соответствие строения ворсин, а также стенки эмбрионального мешка, что объяснялось небольшим сроком от момента приема препарата до отторжения эмбрионального мешка. Непосредственный механизм отторжения заключался в формировании гематомы в толще базальной пластинки с переходом ее в близлежащее межворсинчатое пространство. Местный характер геморрагических нарушений (на границе эндо- и миометрия), их острое возникновение и кратковременность процесса не создавали предпосылок для выброса тромбопластических масс и, следовательно, для изменения гемостазиологических параметров крови, что подтверждалось исследованием свертывающей системы крови.
Показанием к применению мифепристона (мифегина, пенкрофтона) в настоящее время является прерывание маточной беременности на ранних сроках (42 дня аменореи). Однако имеются исследования (Р. А. Хетчер, 1993; Р. А. Манушарова, Э. И. Черкезова, 2002), в ходе которых эти препараты применяли до 9-недельного срока беременности. Кроме того, данные литературы свидетельствуют об эффективности использования мифепристона для подготовки и индукции родов при доношенной беременности. В настоящее время мифепристон применяется во Франции, США, Швеции, Китае, России, Великобритании, Индии и других странах.
Противопоказаниями к назначению препарата являются: наличие в анамнезе повышенной чувствительности к мифепристону, надпочечниковая недостаточность и длительная глюкокортикостероидная терапия, острая или хроническая почечная и/или печеночная недостаточность, порфирия, миома матки, наличие рубца на матке, анемия, нарушения гемостаза (в том числе в результате предшествующего лечения антикоагулянтами), воспалительные заболевания женских половых органов, наличие тяжелой экстрагенитальной патологии. Нельзя применять мифепристон у курящих женщин старше 35 лет без предварительной консультации терапевта. Кроме того, противопоказаниями к применению препарата с целью прерывания беременности являются подозрение на внематочную беременность; беременность, не подтвержденная клиническими исследованиями; превышающая по сроку 42 дня после прекращения менструации; возникшая на фоне применения внутриматочной контрацепции или после отмены гормональной контрацепции.
С осторожностью следует назначать препарат при хронических обструктивных заболеваниях легких (в том числе при бронхиальной астме), тяжелой артериальной гипертензии, нарушениях ритма сердца и сердечной недостаточности. Пациенткам с искусственными сердечными клапанами или инфекционным эндокардитом при применении мифепристона следует проводить профилактическое лечение антибиотиками.
Грудное вскармливание после приема мифепристона следует прекратить на 14 дней. Применение этого препарата требует проведения всех подготовительных мероприятий, связанных с абортом.
Среди побочных действий, связанных с процедурой прерывания, следует отметить: кровянистые выделения из половых путей, боли в низу живота, обострение воспалительных процессов матки и придатков.
Побочные действия, связанные с приемом мифепристона, — чувство дискомфорта в низу живота, слабость, головная боль, тошнота и рвота, головокружение, гипертермия. Прием мифепристона в дозе до 2 г не вызывает нежелательных реакций. В случаях передозировки препарата может наблюдаться надпочечниковая недостаточность.
При проведении медикаментозного аборта с помощью препарата мифепристон следует избегать назначения нестероидных противовоспалительных средств, так как они ослабляют его эффективность. Если на 10–14-й день эффект от применения препарата отсутствует, беременность обязательно следует прервать иным способом, поскольку возможно формирование врожденных пороков развития у плода.
Исследования, проводившиеся еще в 80-х гг., показали, что эффективность изолированного применения мифепристона составляет 85%. Поэтому впоследствии было предложено мифепристон сочетать с простагландинами. По данным литературы, эффективность указанной комбинации достигает 96—98% (Р. А. Манушарова, Э. И. Черкезова, 2002). Также было показано, что эффективность комбинированного применения мифепристона (в дозе 400 мг) и сайтотека (800 мкг) равна 96%.
Под нашим наблюдением находились 200 женщин в возрасте от 18 до 41 года (36,7+2,3 года). У 37 из них беременность была первой; 28 прерывали вторую беременность (первая закончилась искусственным абортом), остальные имели в анамнезе роды (37) или роды и аборты (98). По данным гинекологического осмотра и УЗИ, гестационный срок в среднем составил 5,2±0,2 недели при среднем диаметре плодного яйца 10,5+0,5 мм.
Гинекологические заболевания имелись у 42,1% пациенток (бессимптомная миома матки небольших размеров — 4,1%; эрозия шейки матки — 20,9%; хронические аднекситы — 15%; параовариальная киста — 4%; дисфункции яичников — 5%; генитальный эндометриоз — 3,1%).
Мифегин назначали однократно в виде таблеток в дозе 600 мг (3 табл. по 200 мг), а через 36—48 ч пациентки принимали простагландин — мизопростол (сайтотек) в дозе 400 мкг (2 табл. по 200 мкг) и спустя 3 ч — еще 400 мкг (2 табл.). Препараты принимались в присутствии врача после получения согласия пациентки. Наблюдение осуществлялось в течение 2-3 ч, после чего женщины могли покинуть лечебное учреждение, получив необходимые рекомендации. Трудоспособность при этом сохранялась полностью.
Эффективность метода оценивалась на основании констатации положительного исхода, подтвержденного данными объективного исследования, бимануального исследования, УЗИ (отсутствие плодного яйца, а также его элементов в полости матки на 10—14-й день).
Экспульсия плодного яйца у 180 из 200 женщин произошла после комбинированного применения мифегина и сайтотека, у 11 пациенток — без дополнительного приема сайтотека. У 9 пациенток со сроком беременности 8,5-9 нед. через 12—24 ч после приема мифегина наблюдалось кровотечение из половых путей, по поводу чего они были госпитализированы и было произведено выскабливание слизистой полости матки. Экспульсия плодного яйца произошла в первые сутки после приема сайтотека — у 95,3%, на вторые сутки — у 4,7% женщин. Клинически это проявлялось кровянистыми выделениями из половых путей (скудных или умеренной интенсивности) в первые сутки после приема мифегина — у 38% женщин; у 62% пациенток в первые сутки после приема мифегина не отмечено появления кровянистых выделений из половых путей. Спустя 40–55 мин после приема сайтотека кровянистые выделения из половых путей усиливались у подавляющего большинства женщин и в 60% случаев сопровождались схваткообразными болями в низу живота и экспульсией плодного яйца.
Продолжительность кровянистых выделений составляла в большинстве случаев от 7 до 14 дней. У 4 пациенток наблюдались скудные кровянистые выделения до 15—17 дней. Кровотечения, потребовавшие проведения консервативной терапии в течение 1-2 дней (дицинон, аскорутин, викасол), были отмечены у 3 пациенток. Хирургического вмешательства с целью гемостаза не потребовалось ни в одном наблюдении. Следует отметить, что выраженные схваткообразные боли в низу живота наблюдались у нерожавших женщин, а у рожавших пациенток они были выражены слабо или отсутствовали. Купировали схваткообразные боли в низу живота пероральным приемом или парентеральным введением спазмолитических (но-шпа) или анальгетических (анальгин, баралгин) средств.
Положительного результата приема после мифегина нам не удалось добиться в 3 случаях. По данным УЗИ, было зафиксировано наличие остатков плодного яйца в полости матки, по поводу чего пациенткам было проведено диагностическое выскабливание. Следует отметить, что у этих женщин в анамнезе имелся эндометрит. По-видимому, отсутствие достаточного эффекта в данных случаях обусловлено нарушением сократительной способности матки.
Переносимость мифегина была хорошей. При приеме сайтотека у 8 женщин отмечены побочные эффекты(в виде тошноты, рвоты, головокружения, головной боли), которые продолжались в течение 30—45 мин от начала приема препарата и проходили самостоятельно.
Контрольные УЗИ, выполненные на 10—14-е сутки после экспульсии плодного яйца, показали нормальное состояние эндометрия у 187 женщин. У 3 пациенток отмечалось расширение М-ЭХО при наличии гипоэхогенного содержимого. В одном наблюдении выявлены неоднородность М-ЭХО и эхонегативные включения. Этим женщинам дополнительно назначался дюфастон в дозе 10 мг 2 раза в сутки в течение 10 дней и после очередной менструации проводилось дополнительное УЗИ. Во всех случаях было установлено нормальное состояние М-ЭХО при контрольном УЗИ.
Таким образом, результаты проведенного исследования свидетельствуют о том, что комбинированное применение препаратов мифегин (мифепристон) и сайтотек является высокоэффективным средством для прерывания нежелательной беременности. При строгом соблюдении всех необходимых требований этот способ хорошо переносится женщинами, не имеет существенных побочных эффектов и может применяться для прерывания беременности на малых сроках (до 7 нед.). Применение мифегина не вызывает нарушения менструального цикла, вероятность влияния на репродуктивную функцию практически равна нулю.
Медикаментозное прерывание беременности почти полностью исключает риск возникновения восходящей инфекции и связанных с ней осложнений. Кроме того, при данном методе прерывания беременности отсутствует психогенная травма, чаще всего сопровождающая традиционный артифициальный аборт, что повышает качество жизни женщины.
По вопросам литературы обращайтесь в редакцию.
Р. А. Манушарова, доктор медицинских наук, профессор
Э. И. Черкезова
РМАПО, Клиника андрологии, Москва
Децидуальный полип
Децидуальный полип – это новообразование в виде небольшого выроста, выступающее в просвет канала шейки матки или за его пределы. В период беременности гормональный фон женщины подвергается мощным изменением, в результате чего слизистая канала начинает разрастаться, то есть происходит ее децидуализация. Избыточное разрастание децидуальной (хориальной) ткани в результате приводит к ее проникновению в цервикальный канал в виде небольших наростов (полипов).
По данным научных исследований, практически 22% беременных женщин сталкиваются с доброкачественными патологическими процессами шейки матки, в частности, с полиповидными образованиями эндоцервикса (слизистой оболочки, выстилающей шейку матки изнутри).
Различают два вида полиповидных образований шейки матки:
Образование таких полипов сложно назвать заболеванием, поскольку в большинстве случаев они проходят самостоятельно после рождения ребенка и стабилизации гормонального фона. Однако такие образования способны вызвать беспокойство женщины, поскольку характеризуются наличием большого количества сосудов и начинают кровоточить при малейшем механическом воздействии, например, во время половой близости или медицинского обследования.
Травмированный полип представляет собой серьезную опасность, поскольку может быть инфицирован, а это способно вызвать серьезные воспалительные процессы в организме женщины. Необходимо срочно обратиться к специалисту, если обнаружили у себя любой из симптомов, указывающий на наличие полипа.
Симптомы и причины возникновения
Как уже было отмечено, поскольку тело децидуального полипа пронизано большим количеством кровеносных сосудов, он может начать кровить даже при малейшем повреждении. То есть кровянистые выделения из влагалища могут возникнуть в результате активных физических нагрузок или в процессе планового обследования в кабинете врача.
На что следует обращать внимание, если специалисты диагностировали наличие полипа:
Любой из данных симптомов может свидетельствовать об инфицировании полипа и возникновении воспалительного процесса. Если новообразование постоянно кровоточит, следует пройти полное обследование, на основании которого специалист назначит адекватное лечение.
Этиология полипов до конца не изучена, но современная медицина выделяет несколько основных причин развития таких новообразований:
Особенно важно отслеживать децидуальный полип при беременности, и поскольку основными показателями состояния образования являются выделения, о любом изменении их состава необходимо сообщать гинекологу.
Децидуальный полип при беременности: диагностика и лечение
Децидуальные новообразования образуются из ткани плаценты или хориона и располагаются в шейке матки. Диагностика таких полипов не представляет особой сложности, поскольку они обнаруживаются при обычном исследовании шейки матки и цервикального канала – кольпоскопии. Процедура занимает всего несколько минут и является безболезненной. Обязательными являются общеклинические и бактериологические лабораторные исследования.
Обнаружив полип, врач проводит дифференциальную диагностику с паппиломой шейки матки, пролабирующими железами и травмированными кусочками ткани шейки матки, которые могут быть приняты за полип. С помощью мазка на онкоцитологию и в редких случаях биопсии определяется состояние полипа. Также выполняется УЗИ органов малого таза с допплеометрическим картированием сосудов и эхоскопией полиповидного образования. После проведения полной диагностики и постановки точного диагноза назначается эффективное лечение.
В большинстве случаев децидуальные образования не нуждаются в каком-либо лечении и самостоятельно проходят после нормализации гормонального фона. Естественному ходу родов такие полипы также не мешают, поэтому чаще всего после постановки диагноза специалисты просто наблюдают за развитием образования, контролируют внутреннюю флору влагалища и при необходимости могут назначить противовоспалительное лечение.
Однако децидуальный полип при беременности подлежит немедленному удалению, если наблюдаются такие симптомы:
Удаляют полип методом откручивания с применением лазера, эндоскопа, с последующей термо- и криокоагуляцией образования. Данный способ оперативного вмешательства является малоинвазивным и не требует выскабливания цервикального канала, поэтому может использоваться при беременности.
Диагностика и лечение децидуального полипа в ОН КЛИНИК
Большинство женщин обращаются к гинекологу лишь при возникновении болезненных или дискомфортных ощущений. Но, чтобы сохранить собственное здоровье и выявить заболевание на самой ранней стадии развития, следует проводить регулярные гинекологические осмотры. Если у Вас возникли любые сомнения по поводу здоровья или появились тревожные симптомы, свидетельствующие о каких-либо нарушениях, рекомендуем незамедлительно обратиться к специалистам нашей клиники.
Медицинский центр ОН КЛИНИК – это команда профессионалов с огромным практическим опытом и прогрессивной диагностической базой. В своей работе наши гинекологи используют уникальные методы диагностики и лечения любых женских заболеваний, что позволит в короткий срок справиться с патологией и полностью устранить все проявления болезни на самом раннем этапе развития.
Ультразвуковая диагностика с объемным сканированием позволяет точно определить наличие и локализацию образований, а современные безоперационные методы позволяют проводить малоинвазивные вмешательства без риска возникновения каких-либо осложнений.
ОН КЛИНИК: тысячи женщин вернулись к здоровой жизни благодаря профессиональной работе наших врачей. Присоединяйтесь!