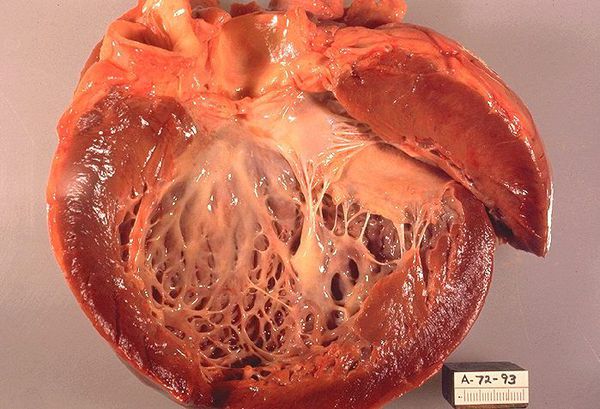
дилатационная кардиомиопатия что это такое простыми словами и как лечить
Что такое кардиомиопатия? Причины возникновения, диагностику и методы лечения разберем в статье доктора Кузнецова Т. Н., кардиолога со стажем в 26 лет.
Определение болезни. Причины заболевания
Пусковым механизмом возникновения кардиомиопатии поначалу считали процесс воспаления в сердце, который мог быть спровоцирован вирусными, бактериальными и аутоиммунными повреждениями клеток. Исходя из этой теории, назначение антибиотиков, противовирусных и противовоспалительных препаратов должно было привести к регрессии повреждения и восстановлению функции сердца. Однако практика это не подтвердила.
Риск развития кардиомиопатий повышен у лиц с отягощённой наследственностью, а также после перенесённых острых инфекционных заболеваний. Для появления вторичных кардиомиопатий важно наличие системных аутоиммунных заболеваний, эндокринной патологии (сахарный диабет, тиреотоксикоз) и токсических факторов.
Первичные кардиомиопатии чаще выявляют в детском и молодом возрасте, вторичные же возможны в любом возрасте.
Симптомы кардиомиопатии
Специфических, характерных только для кардиомиопатии симптомов не существует. Именно эта особенность и затрудняет раннюю диагностику заболевания. Кардиомиопатия длительно протекает бессимптомно или малосимптомно, в развёрнутой стадии похожа по клинике на проявления ишемической болезни сердца, различных пороков сердца.
Первыми жалобами, с которыми пациенты обращаются к врачу, являются:
Патогенез кардиомиопатии
За последние годы благодаря возможностям генетики было установлено, что причиной многих кардиомиопатий являются генетические мутации, которые приводят к выработке дефектных белков кардиомиоцита. От того, какой белок рабочей клетки миокарда (кардиомиоцита) изменился, зависит развитие определённого вида кардиомиопатии.
Подобные изменения бывают также при наследственных нарушениях обмена веществ и лизосомальных болезнях накопления (редких заболеваниях, при которых нарушается функция внутриклеточных органелл лизосом). Из-за врождённой нехватки ферментов, перерабатывающих углеводсодержащие продукты, в организме накапливаются крупные молекулы гликогена, гликопротеина и др., которые повреждают организм. Таких заболеваний известно более сотни, но их распространённость невелика. Как правило, проявляются они в детском и молодом возрасте и помимо поражения сердца затрагивают практически весь организм: кости, мышцы, нервную систему, зрение и слух. Самыми изученными болезнями накопления являются гемохроматоз, болезнь Пике и болезнь Фабри.
Классификация и стадии развития кардиомиопатии
По мере накопления информации были выявлены самые распространённые типы кардиомиопатии и их семейные формы:
К редким формам кардиомиопатии относят также системные заболевания и патологические состояния, при которых возникают так называемые вторичные кардиомиопатии: диабетическая, тиреотоксическая, алкогольная, аутоиммунная и другие.
Исходя из причины развития болезни, становится ясным, что кардиомиопатии могут быть как изолированными – первичными, так и являться частью системного заболевания, т. е. быть вторичными.
В России традиционно применяется клинико-морфологическая классификация первичных кардиомиопатий, где кардиомиопатии разделяются на:
Анатомическая классификация гипертрофической кардиомиопатии в зависимости от локализации:
I. Гипертрофия левого желудочка:
В зависимости от наличия обструкции выносного тракта левого желудочка (область между межжелудочковой перегородкой и передней створкой митрального клапана) в покое и при нагрузке выделяют два типа гипертрофической кардиомиопатии :
К тяжело выявляемым видам относится аритмогенная дисплазия правого желудочка, при которой происходят структурные изменения в строении стенки правого желудочка — замещение кардиомиоцитов фиброзно-жировой тканью и развитие аритмии.
Неклассифицируемые кардиомиопатии: некомпактный миокард, стресс-индуцированная кардиомиопатия.
Вторичные (специфические) кардиомиопатии: при имеющемся известном заболевании тяжесть поражения сердца более выражена и не соответствует причине:
Осложнения кардиомиопатии
Особенности течения кардиомиопатии представляют угрозу для жизни. Болезнь может дебютировать сразу внезапной смертью или жизнеугрожающими аритмиями : фибрилляцей желудочков, желудочковой тахикардией. Высокий риск внезапной сердечной смерти связан с такими факторами риска, как:
С утяжелением недостаточности все симптомы становятся более выраженными. Выделяют пять стадий сердечной недостаточности:
Диагностика кардиомиопатии
Особых признаков, характерных для этого заболевания, при сборе жалоб и осмотре пациента выявить не удаётся.
При клиническом осмотре обращают на себя внимание признаки сердечной недостаточности различной степени выраженности, аритмии, возможны тромбоэмболические осложнения.
В основном кардиомиопатии выявляются при проведении эхокардиографии (ЭХОКГ) и электрокардиографии (ЭКГ). Дополнительно применяются рентгеноконтрастная вентрикулография и магнитно-резонансная томография (МРТ) с контрастированием гадолинием.
В современной кардиологии всё больше распространяются новые методы визуализации сердца и сосудов — например, магнитно-резонансная томография (МРТ). Но её недостатком является дороговизна оборудования и малая доступность методики из-за отсутствия качественного оборудовании и специалистов.
На стандартной ЭКГ также могут быть зарегистрированы изменения в виде признаков гипертрофии миокарда левого желудочка, а также признаки его перегрузки и различные нарушения ритма сердца.
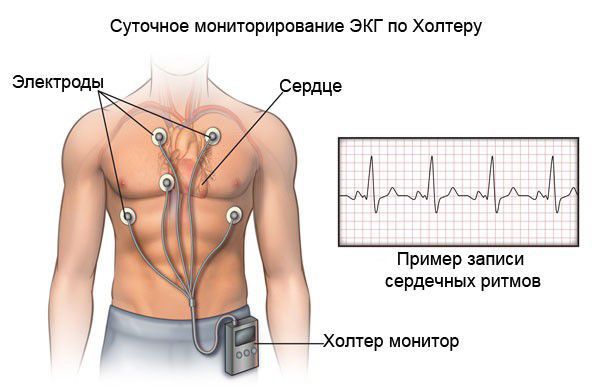
При холтеровском мониторировании ЭКГ также фиксируются нарушения ритма и проводимости практически в 100 % случаях. Выявление таких нарушении ритма сказывается на подборе базисной терапии кардиомиопатии.
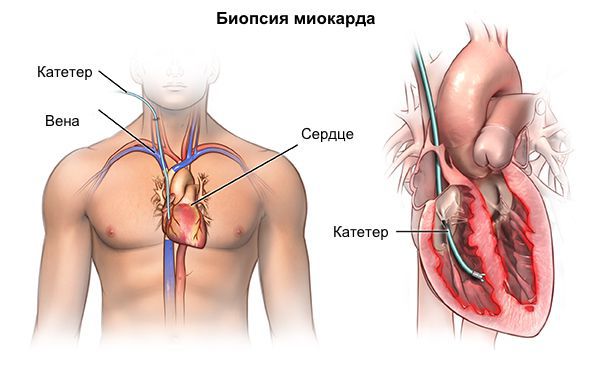
В особых случаях для уточнения диагноза редких форм кардиомиопатии (например, при амилоидозе) возможна прижизненная биопсия миокарда. Методика инвазивная, потенциально опасная для пациента, требует использования уникального комплекса аппаратуры и высочайшей квалификации специалистов, что возможно только в нескольких научных кардиологических центрах РФ.
Из лабораторных методов диагностики помимо стандартных анализов крови (клинического и биохимического), необходимо отметить ДНК-диагностику. Она является «золотым стандартом» при подозрении на кардиомиопатию согласно мировым (европейским и американским) руководствам. Этот подход на данный момент является практически единственным, который применим для раннего выявления и прогнозирования риска развития семейных форм кардиомиопатии. В России такой уровень диагностики возможен в единичных лабораториях и является дорогостоящей процедурой из-за своей уникальности.
Лечение кардиомиопатии
По современным представлениям стратегия лечения пациента определяется в процессе разделения больных на категории в зависимости от типа кардиомиопатии.
Все больные с выявленной кардиомиопатией, независимо от течения заболевания (в том числе и бессимптомные), нуждаются в динамическом наблюдении. Кратность наблюдения и объём обследований определяются индивидуально. В обязательный перечень входят стандартные анализы (клинический и биохимический анализ крови), ЭКГ, ЭХОКГ и холтеровское мониторирование ЭКГ.
Лечебная тактика зависит от множества факторов и подбирается индивидуально. При этом учитываются анатомические особенности — обструкция выносного тракта левого желудочка, растяжение полостей сердца, наличие клапанной патологи, стадия сердечной недостаточности и также сопутствующие заболевания. Необходимо выявлять факторы, повышающие риск внезапной смерти и жизнеугрожающих аритмий [15]
При дилатационной кардиомиопатии необходимо лечить причину развития растяжения полостей сердца, если это возможно. В медикаментозной терапии сердечной недостаточности применяют все стандартные группы лекарств:
Помимо лекарств в ряде случаев прибегают к хирургическим методам лечения кардиомиопатии.
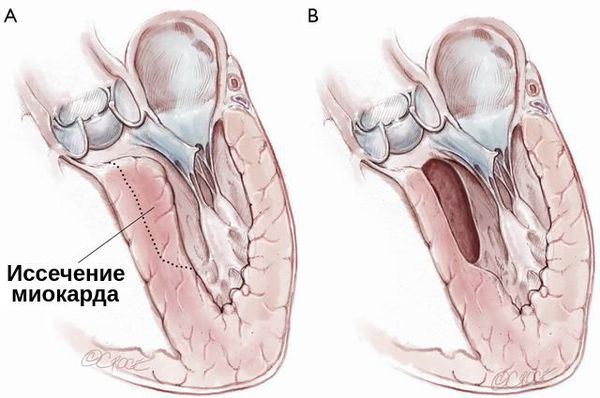
При гипертрофической кардиомиопатии применяется септальная миэктомия — иссечение миокарда, расположенного в основании межжелудочковой перегородки. Она может быть дополнена и вмешательством на изменённом митральном клапане: вальвулопластикой, протезированием митрального клапана и коррекцией кольца митрального клапана.
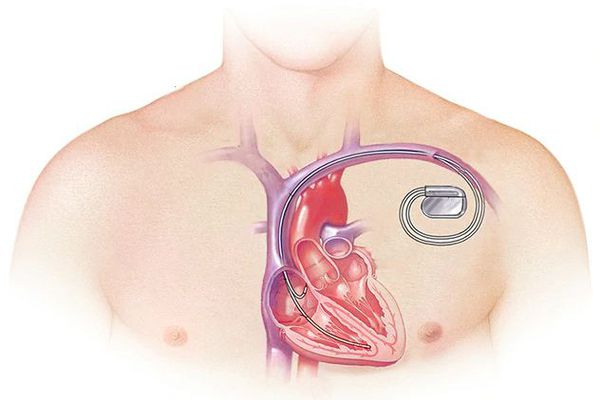
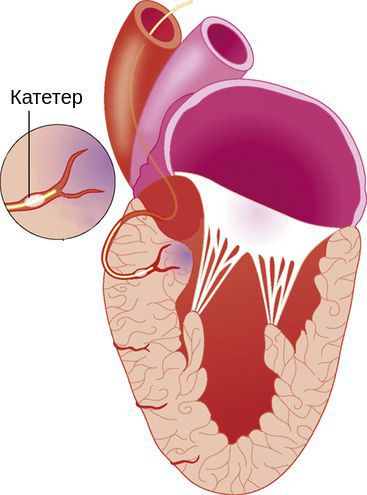
При тяжёлой обструктивной гипертрофической кардиомиопатии рассматривается проведение операции — иссечения части сердечной мышцы или более щадящая методика — чрескожная транслюминальная алкогольная абляция. При ней через катетер вводится до 3 мл 96 % спирта в зону максимальной гипертрофии миокарда и вызывается его инфаркт. Из-за этого мышца уменьшается в размере, исчезает препятствие (обструкция) току крови через митральное кольцо. Далее проводится установка кардиостимулятора для синхронизации работы всех отделов сердца. Эта процедура проводится кардиохирургами в специализированных отделениях.
Прогноз. Профилактика
Прогноз при гипертрофической кардиомиопатии также неблагоприятный, но смертность не такая высокая — в первый год умирают 1 % заболевших, чаще от внезапной смерти, обусловленной факторами риска (наследственностью, тахикардией, предшествующим обмороками, понижением давления).
При рестриктивной кардиомиопатии прогноз неблагоприятный, так как заболевание часто находят уже на поздней стадии развития. Лечение только симптоматическое и поддерживающее.
Для человека с выявленной кардиомиопатии частота посещений и обследований устанавливается индивидуально.
Дилатационная кардиомиопатия
Содержание
Что такое дилатационная кардиомиопатия?
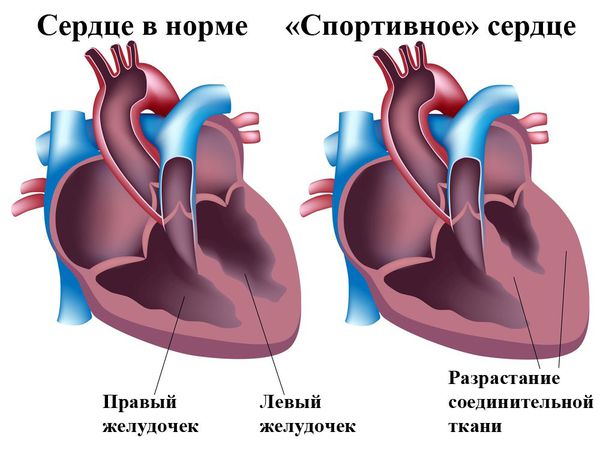
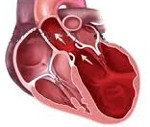
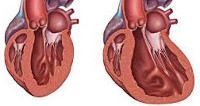
Дилатационная кардиомиопатия (ДКМП) представляет собой состояние, при котором способность сердца качать кровь снижается из-за увеличения и ослабления левого желудочка, главной насосной камеры сердца. Зачастую это не позволяет сердцу наполниться кровью, как следует. Со временем это может повлиять также на другие камеры сердца.
Симптомы дилатационной кардиомиопатии
Многие люди с ДКМП не имеют либо никаких признаков болезни, либо только незначительные симптомы, и живут абсолютно нормальной жизнью. У других же пациентов симптомы могут прогрессировать и обостряться, ухудшая тем самым работу сердца.
Симптомы дилатационной кардиомиопатии могут возникнуть в любом возрасте и включают в себя:
Причины дилатационной кардиомиопатии
Дилатационная кардиомиопатия может быть унаследована (семейная ДКМП), но в первую очередь эта болезнь сердца может быть вызвана рядом других факторов, в их числе:
Диагностика дилатационной кардиомиопатии
ДКМП диагностируется как при исследовании вашей истории болезни (симптомы и семейная история), так и на основе медицинского осмотра и клинических анализов, таких, например, как анализы крови, ЭКГ, рентген грудной клетки, эхокардиография (УЗИ сердца), стресс-тест, катетеризация сердца, КТ и МРТ.
Другие анализы, чтобы выявить причину возникновения ДКМП, делают редко, т.к. при проведении биопсии миокарда, необходимо исследовать под микроскопом, образец ткани, взятый из сердца, чтобы определить причину этих симптомов.
Родственники больных дилатационной кардиомиопатией должны регулярно проходить обследование на ДКМП. Также не лишним будет генетическое тестирование, для выявления ненормальных генов.
Лечение дилатационной кардиомиопатии
Какие препараты используются для лечения ДКМП?
Для улучшения работы сердца, большинство людей, принимают такие лекарства, как бета-блокаторы, ингибиторы АПФ и/или различные мочегонные средства. Если у вас аритмия, врач может дать вам лекарство для контроля сердечного ритма. Растворители крови могут быть использованы, чтобы предотвратить образование кровяных сгустков. Обсудите с вашим врачом, какое лечение вам больше подходит.
Что используют в хирургии для лечения ДКМП?
Людям с тяжелой формой дилатационной кардиомиопатии, возможно, потребуется одна из следующих операций:
Дилатационная кардиомиопатия
Дилатационная кардиомиопатия – это миокардиальное поражение, характеризующееся расширением полости левого или обоих желудочков и нарушением сократительной функции сердца. Дилатационная кардиомиопатия проявляется признаками застойной сердечной недостаточности, тромбоэмболическим синдромом, нарушениями ритма. Диагностика дилатационной кардиомиопатии основывается на данных клинической картины, объективного обследования, ЭКГ, фонокардиографии, ЭхоКГ, рентгенографии, сцинтиграфии, МРТ, биопсии миокарда. Лечение дилатационной кардиомиопатии проводится ингибиторами АПФ, β-адреноблокаторами, диуретиками, нитратами, антикоагулянтами и антиагрегантами.
МКБ-10
Общие сведения
Дилатационная кардиомиопатия (застойная, конгестивная кардиомиопатия) – клиническая форма кардиомиопатии, в основе которой лежит растяжение полостей сердца и систолическая дисфункцией желудочков (преимущественно левого). В современной кардиологии на долю дилатационной кардиомиопатии приходится около 60% всех кардиомиопатий. Дилатационная кардиомиопатия чаще манифестирует в возрасте 20-50 лет, однако встречается у детей и пожилых людей. Среди заболевших преобладают лица мужского пола (62-88%).
Причины
В настоящее время существует несколько теорий, объясняющих развитие дилатационной кардиомиопатии: наследственная, токсическая, метаболическая, аутоиммунная, вирусная. В 20–30 % случаев дилатационная кардиомиопатия является семейным заболеванием, чаще с аутосомно-доминантным, реже – с аутосомно-рецессивным или Х-сцепленным (синдром Барта) типом наследования. Синдром Барта, кроме дилатационной кардиомиопатии, характеризуется множественными миопатиями, сердечной недостаточностью, фиброэластозом эндокарда, нейтропенией, задержкой роста, пиодермиями. Семейные формы дилатационной кардиомиопатии и имеют наиболее неблагоприятное течение.
В анамнезе у 30% пациентов с дилатационной кардиомиопатией отмечается злоупотребление алкоголем. Токсическое воздействие этанола и его метаболитов на миокард выражается в повреждении митохондрий, уменьшении синтеза сократительных белков, образовании свободных радикалов и нарушении метаболизма в кардиомиоцитах. Среди других токсических факторов выделяют профессиональный контакт со смазочными материалами, аэрозолями, промышленной пылью, металлами и пр.
В этиологии дилатационной кардиомиопатии прослеживается влияние алиментарных факторов: недостаточного питания, дефицита белка, гиповитаминоза В1, нехватки селена, дефицита карнитина. На базе этих наблюдений основывается метаболическая теория развития дилатационной кардиомиопатии. Аутоиммунные нарушения при дилатационной кардиомиопатии проявляются наличием органоспецифических кардиальных аутоантител: антиактина, антиламинина, антимиозина тяжелых цепей, антител к митохондриальной мембране кардиомиоцитов и др. Однако аутоиммунные механизмы являются лишь следствием фактора, который пока не установлен.
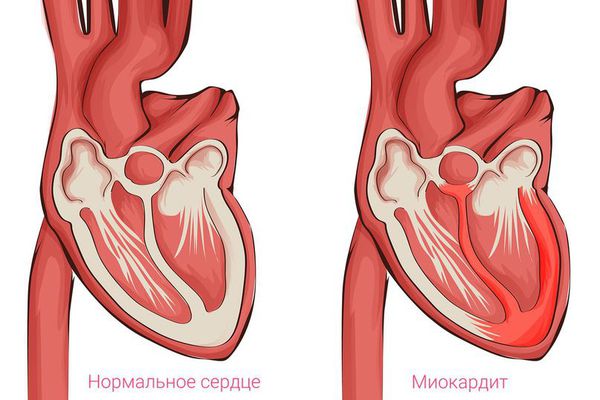
С помощью молекулярно-биологических технологий (в т. ч. ПЦР) в этиопатогенезе дилатационной кардиомиопатии доказана роль вирусов (энтеровируса, аденовируса, вируса герпеса, цитомегаловируса). Часто дилатационная кардиомиопатия служит исходом вирусного миокардита.
Факторами риска послеродовой дилатационной кардиомиопатии, развивающейся у ранее здоровых женщин в последнем триместре беременности или вскоре после родов, считаются возраст старше 30 лет, негроидная раса, многоплодная беременность, наличие в анамнезе более 3-х родов, поздний токсикоз беременности.
В некоторых случаях этиология дилатационной кардиомиопатии остается неизвестной (идиопатическая дилатационная кардиомиопатия). Вероятно, дилатация миокарда возникает при воздействии ряда эндогенных и экзогенных факторов, преимущественно у лиц с генетической предрасположенностью.
Патогенез
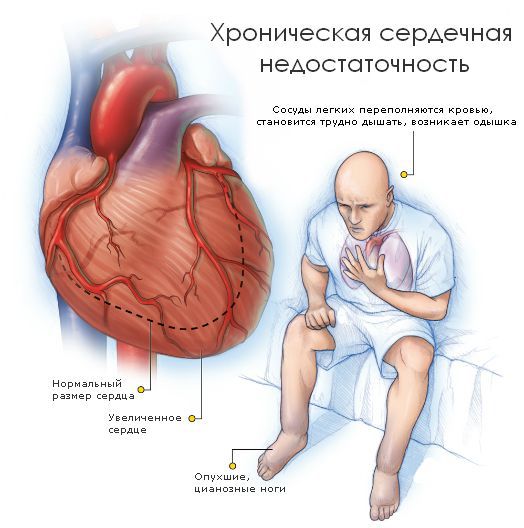
Под действием причинных факторов уменьшается количество функционально полноценно кардиомиоцитов, что сопровождается расширением камер сердца и снижением насосной функции миокарда. Дилатация сердца приводит к диастолической и систолической дисфункции желудочков и обусловливает развитие застойной сердечной недостаточности в малом, а затем и в большом круге кровообращения.
На начальных стадиях дилатационной кардиомиопатии компенсация достигается благодаря действию закона Франка–Старлинга, увеличению ЧСС и уменьшению периферического сопротивления. По мере истощения резервов сердца прогрессирует ригидность миокарда, нарастает систолическая дисфункция, уменьшается минутный и ударный объем, нарастает конечное диастолическое давление в левом желудочке, что приводит к еще большему его расширению.
В результате растяжения полостей желудочков и клапанных колец развивается относительная митральная и трикуспидальная недостаточность. Гипертрофия миоцитов и формирование заместительного фиброза приводят к компенсаторной гипертрофии миокарда. При уменьшении коронарной перфузии развивается субэндокардиальная ишемия.
Вследствие снижения сердечного выброса и уменьшения почечной перфузии активизируются симпатическая нервная и ренин-ангиотензиновая системы. Выброс катехоламинов сопровождается тахикардией, возникновением аритмий. Развивающиеся периферическая вазоконстрикция и вторичный гиперальдостеронизм приводят к задержке ионов натрия, увеличению ОЦК и развитию отеков.
У 60 % пациентов с дилатационной кардиомиопатией в полостях сердца формируются пристеночные тромбы, вызывающие в дальнейшем развитие тромбоэмболического синдрома.
Симптомы дилатационной кардиомиопатии
Дилатационная кардиомиопатия развивается постепенно; длительное время жалобы могут отсутствовать. Реже она манифестирует подостро, после ОРВИ или пневмонии. Патогномоничными синдромами дилатационной кардиомиопатии являются сердечная недостаточность, нарушения ритма и проводимости, тромбоэмболии.
При нарушениях ритма и проводимости возникают пароксизмы сердцебиения и перебоев в работе сердца, головокружение, синкопальные состояния. В некоторых случаях дилатационная кардиомиопатия впервые заявляет о себе тромбоэмболией артерий большого и малого кругов кровообращения (ишемический инсульт, ТЭЛА), что может послужить причиной внезапной смерти больных. Риск эмболии увеличивается при мерцательной аритмии, которая сопутствует дилатационной кардиомиопатии в 10—30% случаев.
Течение дилатационной кардиомиопатии может быть быстро прогрессирующим, медленно прогрессирующим и рецидивирующим (с чередованием обострений и ремиссий заболевания). При быстро прогрессирующем варианте дилатационной кардиомиопатии терминальная стадия сердечной недостаточности наступает в течение 1,5 лет от появления первых признаков заболевания. Чаще всего встречается медленно прогрессирующее течение дилатационной кардиомиопатии.
Диагностика
Диагностика дилатационной кардиомиопатии представляет существенные трудности ввиду отсутствия специфических критериев. Диагноз устанавливается путем исключения других заболеваний, сопровождающихся дилатацией полостей сердца и развитием недостаточности кровообращения, а также с помощью генетического анализа.
Объективными клиническими признаками дилатационной кардиомиопатии служат кардиомегалия, тахикардия, ритм галопа, шумы относительной недостаточности митрального и трикуспидального клапанов, увеличение ЧД, застойные хрипы в нижних отделах легких, набухание вен шеи, увеличение печени и др. Аускультативные данные подтверждаются с помощью фонокардиографии. Инструментальная диагностика:
Лечение дилатационной кардиомиопатии
Лечебная тактика при дилатационной кардиомиопатии заключается в коррекции проявлений сердечной недостаточности, нарушений ритма, гиперкоагуляции. Больным рекомендуется постельный режим, ограничение потребления жидкости и соли.
Профилактика тромбоэмболических осложнений при дилатационной кардиомиопатии проводится антикоагулянтами (гепарин подкожно) и антиагрегантами (ацетилсалициловая кислота, пентоксифиллин, дипиридамол). Радикальное лечение дилатационой кардиомиопатии подразумевает проведение трансплантации сердца. Выживаемость свыше 1 года после пересадки сердца достигает 75–85 %.
Прогноз и профилактика
В целом течение дилатационной кардиомиопатии неблагоприятное: 10-летняя выживаемость составляет от 15 до 30%. Средняя продолжительность жизни после появления симптомов сердечной недостаточности составляет 4–7 лет. Гибель пациентов в большинстве случаев наступает от фибрилляции желудочков, хронической недостаточности кровообращения, массивной легочной тромбоэмболии.
Рекомендации кардиологов по профилактике дилатационной кардиомиопатии включают медико-генетическое консультирование при семейных формах заболевания, активное лечение респираторных инфекций, исключение употребления алкоголя, сбалансированное питание, обеспечивающее достаточное поступление витаминов и минералов.
Дилатационная кардиомиопатия
Термин “кардиомиопатии” (КМП) предложен W. Brigden в 1957 г. для обозначения первичных поражений миокарда неизвестной этиологии, вызывающих нарушение функции сердца и не являющихся следствием заболеваний коронарных артерий, клапанного аппарата, перикарда, системной или легочной гипертензии, поражения проводящей системы сердца. Основным критерием отграничения КМП от других поражений миокарда считался признак “неизвестности” происхождения этих заболеваний.
Больные с ДКМП составляют от 26 до 60% всех больных с кардиомиопатиями. Несмотря на то, что ДКМП считается «диагнозом исключения», имеются сообщения о связи ДКМП с гипертензией, приемом агонистов b-адренергических рецепторов или умеренным потреблением алкоголя. Поскольку дилатация и дисфункция желудочков могут возникать вследствие множества приобретенных или наследственных нарушений, большое прогностическое значение имеет дифференциация идиопатической формы заболевания от вторичных и потенциально обратимых форм поражения миокарда.
Что провоцирует / Причины Дилатационной кардиомиопатии:
В последнее десятилетие в большинстве случаев этиологию ДКМП установить не удается (идиопатическая форма ДКМП). Примерно у 20% больных заболевание ассоциируется с перенесенным ранее инфекционным миокардитом. Считают, что воздействие на миофибриллы персистирующих в организме инфекционных агентов (в первую очередь энтеровирусов), в том числе включение вирусной РНК в генетический аппарат кардиомиоцитов или влияние “запущенного” вирусами аутоиммунного процесса, ведет к повреждению митохондрий и нарушению энергетического метаболизма клеток. При использовании полимеразной цепной реакции (ПЦР) у части больных удается выявить присутствие вирусов Коксаки В, вируса гепатита С, герпеса, цитомегаловируса. У части обнаруживаются высокие титры кардиоспецифических аутоантител к миозину тяжелых цепей, актину, тропомиозину, митохондриальной мембране кардиомиоцитов, увеличение цитокинов в крови. Это подчеркивает роль аутоиммунных нарушений. Больные с аутоиммунным дефицитом в большей степени подвержены повреждающему воздействию вирусов и развитию ДКМП.
В происхождении ДКМП большое значение имеет также генетическая предрасположенность к возникновению заболевания. Семейные ДКМП встречаются примерно в случаев заболевания. Для них характерно аутосомно-доминантное наследование. У части больных ДКМП обнаруживаются также гаплотипы НLА В27 и НLА DR4. Имеются данные о неблагоприятном воздействии алкоголя на миокард: нарушение синтеза сократительных белков кардиомиоцитов, повреждение митохондрий, нарушение энергетического метаболизма клеток, критическое снижение сократительной способности миокарда, расширению полостей сердца и формированию ДКМП.
В генезе ДКМП имеет значение взаимодействие нескольких факторов: генетической предрасположенности к возникновению заболевания; воздействия экзогенных факторов (вирусная инфекция, алкоголь) и аутоиммунных нарушений. Если на начальных стадиях развития ДКМП в ряде случаев удается подтвердить вторичную природу поражения сердца (наличие вирусной инфекции), то на поздних стадиях клиническая картина уже мало зависит от возможных пусковых механизмов болезни. На практике в большинстве случаев конкретные причины остаются невыясненными и ДКМП трактуется как идиопатическая форма заболевания, удовлетворяющая традиционным критериям КМП по J. Goodwin.
Патогенез (что происходит?) во время Дилатационной кардиомиопатии:
В результате воздействия перечисленных выше и некоторых других снижение энергетического метаболизма клеток и уменьшение количества нормально функционирующих миофибрилл. Это ведет к прогрессирующему уменьшению сократительной способности миокарда и насосной функции сердца. В результате снижения инотропной функции миокарда происходит дилатация полостей сердца, которая, согласно механизму Старлинга, в течение некоторого времени поддерживает УО и ФВ на достаточном уровне. Одновременно развивающаяся тахикардия (активация САС) также способствует сохранению сердечного выброса (МО, СИ). Однако такая компенсация весьма невыгодна с энергетической точки зрения, поскольку согласно закону Лапласа, для создания адекватного давления в полости желудочка дилатированная стенка ЛЖ должна развивать значительно большее внутримиокардиальное напряжение.
Следствиями такого прогрессирующего увеличения постнагрузки являются: развитие компенсаторной гипертрофии миокарда желудочков, которая способствует некоторому снижению внутримиокардиального напряжения; увеличение потребности миокарда в кислороде, которое со временем ведет к развитию относительной коронарной недостаточности и ишемии миокарда; дальнейшее повреждение кардиомиоцитов и еще большее снижение сократимости; развитие диффузного и очагового кардиофиброза.
В результате происходит снижение насосной функции сердца, повышается КДД в желудочках и развивается выраженная миогенная дилатация полостей сердца. Эти явления усугубляются развитием относительной недостаточности митрального и трехстворчатого клапанов, что способствует еще большей дилатации предсердий и желудочков. Формируется и быстро прогрессирует ХСН с преимущественным нарушением систолической функции желудочков, застоем крови в малом и большом кругах кровообращения, падением сердечного выброса и нарушением перфузии периферических органов и тканей.
Значительное увеличение массы сердца за счет гипертрофии миокарда обычно не сопровождается заметным утолщением стенки желудочков, поскольку при ДКМП всегда преобладает выраженная дилатация камер сердца, которая как бы нивелирует увеличение мышечной массы. Важное значение в ремоделировании сердечной мышцы и развитии сердечной декомпенсации имеет чрезмерная активация нейрогормональных систем организма, в том числе САС, РААС, АДГ, тканевых РАС и эндотелиальных факторов.
В результате активации этих систем происходит задержка Nа+ и воды в организме, что усугубляет застойные явления в малом и большом кругах кровообращения. Повышенное содержание катехоламинов, ангиотензина II, цитокинов, фактора роста опухолей, тромбоксана приводит к еще большему повреждению миокарда, периферической вазоконстрикции, а также к значительным нарушениям свертывающей и фибринолитической систем крови.
Симптомы Дилатационной кардиомиопатии:
КЛАССИФИКАЦИЯ
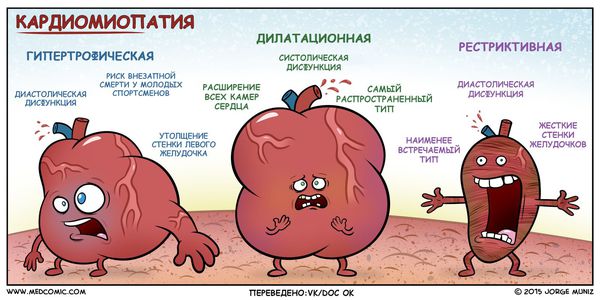
По классификации J. Goodwin (1989) различают 3 группы КПМ: 1. Дилатационная КМП (ДКМП) характеризуется значительной дилатацией камер сердца, систоло-диастолической дисфункцией миокарда и отсутствием выраженной гипертрофии сердечной мышцы. 2. Гипертрофическая КМП (ГКМП) отличается значительной, чаще асимметричной, гипертрофией миокарда левого и/или правого желудочков, отчетливым преобладанием диастолической дисфункции миокарда и отсутствием дилатации полостей сердца. 3. Рестриктивная КМП (РКМП) характеризуется нарушением диастолического наполнения ЛЖ и/или ПЖ, уменьшением их объема, нормальной или почти нормальной систолической функцией.
В 1995 г. экспертами ВОЗ и Международного общества кардиологов рекомендовано использовать термин “кардиомиопатия” для всех случаев поражения миокарда, ассоциированных с нарушением его функции. Согласно этой классификации ВОЗ выделяют 6 групп КМП: ДКМП; ГКМП; РКМП; аритмогенная дисплазия ПЖ; специфические КМП; неклассифицируемые КМП (таблица 37).
Таблица 37. Классификация кардиомиопатий (ВОЗ, 1995)
Приведенная классификация несовершенна. Во-первых, термин “кардиомиопатия” предлагается использовать для обозначения неограниченного количества заболеваний сердца известной и неизвестной этиологии, для которых характерно поражение миокарда, ассоциированное с нарушением его функции. Это приводит к неоправданно широкому употреблению понятия “кардиомиопатия” и полной утрате его нозологической самостоятельности. Во-вторых, вызывает большие сомнения правомочность включения в группу “специфических КМП” так называемых “ишемической”, “гипертензивной”, “клапанной” кардиомиопатий, которые на самом деле представляют собой лишь последствия известных заболеваний сердечно-сосудистой системы (ИБС, АГ, пороков сердца), осложненных сердечной недостаточностью и/или дисфункцией желудочков.
В рекомендациях ВОЗ упоминается, что к этим вариантам специфических КМП отнесены те случаи заболевания, при которых выраженность нарушений функции сердца не соответствует степени нарушений коронарного кровотока, клапанных поражений, уровню АД. На практике решить вопрос о таком соответствии или несоответствии в большинстве случаев довольно сложно.
Делатационная кардиомиопатия манифестирует чаще в возрасте 20-50 лет, однако встречается у детей и пожилых людей. Наиболее частым клиническим проявлением является СН (75-85%). При этом в момент установления диагноза у 90% пациентов определяется уже III–IV ФК ХСН по NYHA. Доминирует симптоматика левожелудочковой СН – снижение переносимости физической нагрузки, прогрессирующая одышка, вплоть до ортопноэ и сердечной астмы. Основные жалобы пациентов обычно на одышку при нагрузке (86%), сердцебиение (30%), периферические отеки (29%). Бессимптомная кардиомегалия выявляется у 4–13% больных. С прогрессированием заболевания симптоматика СН появляется у 95% больных.
Современная клиническая картина ДКМП проявляется тремя основными синдромами: 1. Систолической ХСН (левожелудочковой или бивентрикулярной) с признаками застоя крови в малом и большом кругах кровообращения. 2. Частым возникновением нарушений ритма и проводимости (желудочковые аритмии, фибрилляция предсердий, АВ-блокады и блокады ножек пучка Гиса). 3. Тромбоэмболическими осложнениями (ТЭЛА и эмболия в артерии большого круга кровообращения). Клинические проявления ДКМП и результаты инструментально-лабораторных исследований неспецифичны, что затрудняет дифференциальный диагноз. Поэтому диагноз ДКМП ставится методом исключения других заболеваний сердца с систолической дисфункцией желудочков (ИБС, АГ, миокардит, легочное сердце.
Жалобы
Заболевание длительное время может протекать бессимптомно, несмотря на наличие объективных (эхокардиографических) признаков дилатации желудочков и нарушения их функции. Обычно первые клинические проявления болезни связаны с сердечной декомпенсацией, застоем крови в малом, а затем и в большом кругах кровообращения и снижением сердечного выброса. Больные жалуются на одышку при физической нагрузке и в покое, усиливающуюся в горизонтальном положении больного (ортопноэ). В далеко зашедших случаях возникают приступы удушья, чаще развивающегося по ночам (сердечная астма и отек легких).
Характерна быстрая утомляемость, мышечная слабость, тяжесть в ногах при выполнении физических нагрузок. Признаки правожелудочковой недостаточности (отеки ног, тяжесть в правом подреберье, увеличение живота в объеме, диспептические явления) появляются позже. Примерно у половины больных развиваются разнообразные нарушения ритма и проводимости, часть которых вызывает у больных ДКМП неприятные ощущения (сердцебиения, перебои в работе сердца, приступы пароксизмальной тахикардии и мерцательной аритмии). Наиболее тяжелыми осложнениями являются тромбозы и тромбоэмболии, развивающиеся у 20% больных ДКМП. Наиболее часто эти осложнения возникают у больных с фибрилляцией предсердий. Иногда больные ДКМП отмечают боли в области сердца, которые в большинстве случаев отличаются от типичных приступов стенокардии. Боли часто имеют атипичную локализацию и не связаны с физической нагрузкой.
Физикальное исследование
Физикальные данные, получаемые при обследовании больных ДКМП, неспецифичны. При общем осмотре выявляются признаки СН: акроцианоз, отеки ног, положение ортопноэ, увеличение живота в объеме, набухание шейных вен, иногда положительный венный пульс. При исследовании легких в нижних отделах могут выслушиваться влажные мелкопузырчатые хрипы. Отмечается увеличение печени, появляются признаки сердечной кахексии.
Осмотр, пальпация, перкуссия сердца
Аускультация сердца
Превый тон на верхушке ослаблен. При развитии легочной гипертензии определяется акцент и расщепление II тона. Нередко на верхушке выслушивается протодиастолический ритм галопа (за счет появления III патологического тона), что связано с выраженной объемной перегрузкой желудочков. Характерны систолические шумы на верхушке и в точке выслушивания трехстворчатого клапана, которые указывают на формирование относительной недостаточности митрального и трикуспидального клапанов. При возникновении фибрилляции предсердий или экстрасистолии тоны сердца аритмичные. Специфических изменений артериального пульса нет.
Таблица 38. Предикторы смертности у больных ДКМП
Пятилетняя выживаемость больных ДКМП составляет 60-76%. Более благоприятный прогноз у женщин с ДКМП и I-III ФК СН, а также у пациентов относительно молодого возраста. В последние годы продолжительность жизни этих пациентов значительно увеличилась. С помощью комплексной терапии ингибиторами АПФ, блокаторами b-адренергических рецепторов, диуретиками удается продлить жизнь некоторых больных ДКМП до 8-10 лет. Трансплантация сердца существенно улучшает прогноз. После операции десятилетняя выживаемость достигает 70-80%.
Диагностика Дилатационной кардиомиопатии:
ИНСТРУМЕНТАЛЬНАЯ ДИАГНОСТИКА
Электрокардиография
Электрокардиографическое исследование не позволяет выявить специфические особенности электрического поля сердца, характерные для ДКМП. На ЭКГ обычно определяются: признаки гипертрофии ЛЖ и ЛП, иногда в сочетании с гипертрофией ПЖ. Особенно характерна депрессия сегмента RS–Т в левых грудных отведениях (V5 и V6) и отведениях I и аVL; признаки блокады левой ножки пучка Гиса (частая находка); фибрилляция предсердий и/или другие нарушения ритма сердца; удлинение интервала Q–Т. В ряде случаев на ЭКГ можно выявить признаки крупноочагового или трансмурального рубца миокарда в виде патологических зубцов Q и комплекса QS. Эти изменения отражают характерное для ДКМП развитие очагового фиброза миокарда ЛЖ.
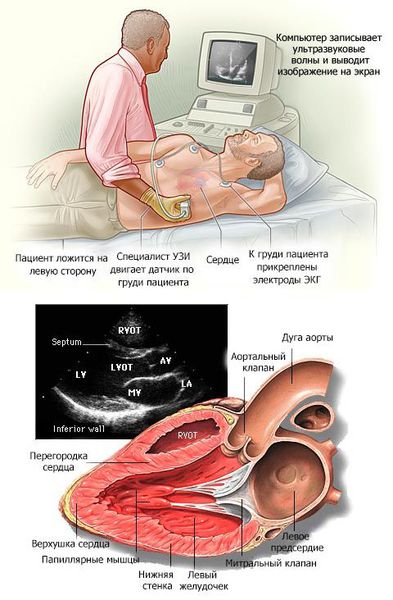
Эхокардиография
ЭхоКГ является наиболее информативным неинвазивным методом исследования больных ДКМП. Во многих случаях эхокардиографическое исследование позволяет впервые выдвинуть диагностическую концепцию ДКМП, оценить степень нарушений систолической и диастолической функций желудочков, а также доказать отсутствие клапанных поражений, заболеваний перикарда. Наиболее характерными эхокардиографическими признаками ДКМП являются значительная дилатация ЛЖ при нормальной или уменьшенной толщине его стенок и снижение ФВ (ниже 30-20%). Часто отмечается расширение других камер сердца (ПЖ, ЛП).
Развиваются тотальная гипокинезия стенок ЛЖ, значительное снижение скорости кровотока в восходящем отделе аорты и выносящем тракте ЛЖ и в легочной артерии (допплеровский режим). Нередко визуализируются внутрисердечные пристеночные тромбы. В некоторых случаях при ДКМП можно обнаружить региональные нарушения сократимости ЛЖ, аневризму верхушки ЛЖ. Это затрудняет дифференциальную диагностику этого заболевания с ИБС. Исследование в двухмерном и допплеровском режимах позволяет выявить признаки относительной недостаточности митрального и трехстворчатого клапанов без деформации их створок.
Рентгенография
Рентгенологическое исследование позволяет визуализировать следующие изменения: признаки кардиомегалии; сглаженность контуров левых отделов сердца; шаровидную форму сердца за счет дилатации всех полостей (в тяжелых случаях); признаки венозной и артериальной легочной гипертензии и расширение корней легких.
Коронароангиография и вентрикулография
Эти инвазивные методы исследования используются в тех случаях, когда возникает необходимость проведения дифференциальной диагностики ДКМП и ИБС при решении вопроса о хирургическом лечении. У больных ДКМП отсутствует гемодинамически значимое сужение КА, определяются повышение показателей КДО и резкое снижение ФВ. Иногда можно выявить нарушения локальной сократимости миокарда ЛЖ.
Эндомиокардиальная биопсия
Проводится в специализированных медицинских центрах. Метод позволяет оценить степень разрушения мышечных филаментов в биоптате, что имеет прогностическое значение.
ДИФФЕРЕНЦИАЛЬНАЯ ДИАГНОСТИКА
Диагностика ДКМП начинается после выявления дилатации ЛЖ сердца с низкой систолической функцией у пациента, который обращается с жалобами на одышку, отеки и слабость. Данные анамнеза, аускультативная картина, рентгенологическое исследование и эхокардиограмма (ЭхоКГ) чаще всего сразу позволяют исключить определенный круг причин дилатации и СН (аневризму ЛЖ сердца, АГ, злоупотребление алкоголем, приобретенные и врожденные пороки сердца). Сбор семейного анамнеза помогает в диагностике наследственных кардиомиопатий, однако при бессимптомных нарушениях выявить больных родственников возможно только с помощью ЭхоКГ.
Электрокардиограмма может оставаться нормальной или отражать лишь неспецифические нарушения реполяризации. Нарушения проводимости встречаются почти у 80% больных и включают атрио-вентрикулярную блокаду I степени, блокаду левой ножки пучка Гиса, блокаду передней левой ветви и неспецифические нарушения внутрижелудочковой проводимости. Блокада правой ножки пучка Гиса встречается реже.
Нарушения проводимости чаще наблюдаются у больных с длительно текущим заболеванием и свидетельствуют о нарастании интерстициального фиброза и гипертрофии кардиомиоцитов. Часто встречаются также признаки гипертрофии ЛЖ, комплексы типа QS в отведениях, отражающих потенциал передней стенки, и отсутствие нарастания амплитуды зубца R в грудных отведениях. Мерцание предсердий, плохо переносимое больными, развивается почти у 20% пациентов, однако это не является свидетельством плохого прогноза. Наиболее широко используемой неинвазивной методикой является ЭхоКГ. Она позволяет выявить дилатацию ЛЖ, оценить толщину его стенок и их сократимость.
Нарушение сократимости является обязательным симптомом ДКМП, обычно диагноз устанавливается при снижении ФИ ниже 45%. Хотя обычным при ДКМП является глобальное нарушение сократимости, почти у 60% больных выявляются сегментарные дисфункции ЛЖ. Более благоприятный прогноз имеется у больных с более выраженным сегментарным, чем тотальным поражением. Дилатация предсердий также встречается часто, однако имеет меньшее значение, чем дилатация желудочков. Внутриполостные тромбы чаще всего выявляются в верхушке ЛЖ. Хотя ДКМП в основном является диффузным процессом, некоторые авторы наблюдали 10-15% больных с изолированной дисфункцией ЛЖ без вовлечения правого. В такой ситуации необходимо в первую очередь исключить коронарный генез дилатации. Допплеровское исследование позволяет выявить умеренную митральную или трикуспидальную регургитации, не слышные при аускультации.
Сцинтиграфия миокарда с 99mТс позволяет количественно оценить систолическую и диастолическую функции ЛЖ и используется в ситуациях, когда проведение ЭхоКГ невозможно (плохое ультразвуковое окно). Нет необходимости проводить катетеризацию полостей сердца всем пациентам, тем более нет необходимости в проведении нескольких последовательных исследований. Катетеризация правых отделов используется для подбора терапии у больных с тяжелым течением заболевания, но исходная оценка гемодинамики перед началом лечения показана редко.
Низкая диагностическая ценность эндомиокардиальной биопсии делает необходимым переосмысление значения этой процедуры. Проведение эндомиокардиальной биопсии необходимо при наличии дисфункции миокарда и системного заболевания, поражающего миокард и поддающегося специфическому лечению (саркоидоз, эозинофилия). Ценность этого метода может возрасти, когда будут внедрены новые технологии диагностики ДКМП на субклеточном и молекулярном уровнях.
Чаще всего сложности возникают при исключении ИБС и миокардита, как причин дилатации ЛЖ. Данные анамнеза и клиническая картина дилатационной кардиомиопатии зачастую имеют сходство со стенокардией, ЭКГ изменения (наличие патологических зубцов Q) не позволяют исключить постинфарктные изменения. Поэтому в сомнительных случаях больным с СН и дилатацией ЛЖ сердца показана коронарография, поскольку реваскуляризация при наличии стенозов коронарных артерий может привести к восстановлению систолической функции.
Недавно перенесенное вирусное заболевание, особенно сопровождавшееся миалгиями или перикардитом, позволяет предположить главенствующую роль миокардита. Однако дифференциальный диагноз дилатационной кардиомиопатии и хронического рецидивирующего миокардита (воспалительной кардиомиопатии) не всегда прост. Более редкой причиной дилатации ЛЖ и снижения его систолической функции является длительно существующая аритмия с частым ритмом сокращения желудочков (кардиомиопатия, индуцированная тахикардией). Дифференциально-диагностическим критерием является восстановление систолической функции ЛЖ и полная обратимость его дилатации после восстановления синусового ритма или контроля ЧСС.
Лечение Дилатационной кардиомиопатии:
Лечение больных ДКМП является в настоящее время трудной задачей. Поскольку причину заболевания установить не удается, патогенетическая терапия больных должна быть направлена на коррекцию ХСН; лечение и профилактику аритмий; лечение и профилактику тромбоэмболических осложнений. Больные ДКМП рефрактерны к лечению инотропными средствами, которые не приводят к уменьшению клинических проявлений ХСН, способствуют возникновению сердечных аритмий.
Консервативное лечение
Лечение ХСН у больных ДКМП основано на определенных принципах. Ограничение физических нагрузок, потребления поваренной соли, особенно при наличии отечного синдрома. Ингибиторы АПФ являются средством первого выбора в лечении больных ДКМП. Назначение этих препаратов (при отсутствии противопоказаний) целесообразно на всех стадиях развития болезни, даже при отсутствии выраженных клинических проявлений ХСН. Ингибиторы АПФ способны предупреждать некроз кардиомиоцитов, развитие кардиофиброза; способствуют обратному развитию гипертрофии, снижают величину постнагрузки (внутримиокардиальное напряжение), уменьшают степень митральной регургитации, давление в ЛП и секрецию ПНУФ.
В-адреноблокаторы целесообразно комбинировать с ингибиторами АПФ. Особенно показаны b-адреноблокаторы у больных со стойкой синусовой тахикардией, а также у пациентов с мерцательной аритмией. У больных ДКМП b-адреноблокаторы используются не только как средство профилактики и лечения нарушений сердечного ритма и контроля ЧСС, но и как препараты, оказывающие влияние на гиперактивированные САС и РААС. Их действие на эти системы сопровождается улучшением гемодинамики, уменьшением ишемии миокарда и повреждения кардиомиоцитов. В-адреноблокаторы улучшают качество жизни, прогноз и выживаемость больных ДКМП. Используют любые b-адреноблокаторы (метопролол, бисопролол, атенолол, карведилол).
Лечение начинают с малых доз препаратов, постепенно увеличивая их до максимально переносимых. У части больных в первые 2–3 недели лечения b-адреноблокаторами могут наблюдаться уменьшение ФВ, УО и некоторое ухудшение состояния, что связано преимущественно с отрицательным инотропным действием этих препаратов. Однако у большинства таких больных со временем начинают преобладать положительные эффекты b-адреноблокаторов, обусловленные стабилизацией нейрогормональной регуляции кровообращения, восстановлением плотности b-адренорецепторов на клеточных мембранах кардиомиоцитов и уменьшением кардиотоксического действия катехоламинов. Постепенно возрастает ФВ и уменьшаются клинические проявления ХСН.Применение b-адреноблокаторов при ДКМП требует осторожности, особенно у больных ХСН III–IV ФК по NYHА, хотя принципиально они не противопоказаны и при тяжелой декомпенсации.
Сердечные гликозиды показаны больным с постоянной формой мерцательной аритмии. В этих случаях положительные эффекты сердечных гликозидов (уменьшение ЧСС) объясняются не положительным инотропным действием этих препаратов, а их ваготропным действием, проявляющимся увеличением рефрактерных периодов АВ-узла и замедлением проведения электрического импульса по АВ-соединению. В результате тахисистолическую форму мерцательной аритмии удается перевести в нормосистолическую, что улучшает процессы диастолического наполнения ЛЖ, снижает давление в ЛП и венах малого круга кровообращения и способствует уменьшению одышки и других проявлений застоя крови в легких.
Дискуссионным остается вопрос о целесообразности применения сердечных гликозидов у больных ДКМП с синусовым ритмом и выраженной систолической дисфункцией ЛЖ (ФВ = 25-30%). Монотерапия сердечными гликозидами бывает неэффективной, поскольку в большистве случаев отсутствует морфологический субстрат для действия этих инотропных лекарственных средств, а именно: имеется значительное и распространенное повреждение кардиомиоцитов, уменьшение количества миофибрилл, нарушения клеточного метаболизма и выраженный кардиофиброз.
Применение сердечных гликозидов у тяжелых больных с выраженной систолической дисфункцией ЛЖ и синусовым ритмом, возможно только в комбинации с ингибиторами АПФ, диуретиками под контролем содержания электролитов и мониторинга ЭКГ. Длительное применение негликозидных инотропных средств у больных ДКМП и ХСН не рекомендуется, так как достоверно увеличивает смертность этих больных. Кратковременное применение негликозидных инотропных лекарственных средств (леводопа, добутамин, милринон, амринон) оправдано при подготовке больных к трансплантации сердца.
Назначение антиагрегантов показано всем больным ДКМП, поскольку в 30% случаев течение заболевания осложняется внутрисердечным тромбозом и развитием тромбоэмболий. С этой целью используется постоянный прием ацетилсалициловой кислоты в дозе 0,25–0,3 г в сутки, применение других антиагрегантов по схемам (трентал, дипиридамол, вазобрал, тонакан). У больных с мерцательной аритмией показано назначение непрямых антикоагулянтов (варфарин) под контролем показателей коагулограммы. Дозы препарата подбираются так, чтобы величина МНО составляла 2-3 ед. Многие специалисты считают показанием для назначения непрямых антикоагулянтов выявление у больных ДКМП внутрисердечных тромбов.
Хирургическое лечение
Серьезной проблемой, ограничивающей широкое распространение этого метода лечения, является высокая стоимость оперативного вмешательства и организационные проблемы. В последние годы в экономически развитых странах длина листа ожидания трансплантации сердца значительно выросла. Тщательный отбор пациентов основан на определении предоперационных характеристик, являющихся лучшими предикторами хорошего исхода.
Двухкамерная электростимуляция сердца с помощью имплантируемого электрокардиостимулятора типа DDD в некоторых случаях позволяет добиться улучшения внутрисердечной гемодинамики, повышая систолическую функцию желудочков, предупредить развитие тяжелых осложнений.
Динамическая кардиомиопластика играет важную роль в лечении больных ДКМП. Используется мышечный лоскут из левой широчайшей мышцы спины, который оборачивается вокруг сердца. Сокращения синхронизируются с помощью электрокардиостимулятора. Эта процедура позволяет улучшить функциональный статус больных, качество жизни, повысить переносимость физической нагрузки. Снижается потребность в госпитализации, медикаментах. Однако не очень оптимистично выглядит показатель выживаемости (70%) при исключении смертности в раннем периоперационном периоде. Кардиомиопластика наиболее эффективна у больных с III ФК ХСН. При более выраженной симптоматике эффект медикаментозной терапии равен или более выражен, чем эффект от операции.
В последнее десятилетие контингент больных ДКМП существенно изменился. Возросло число больных с доклиническими и субклиническими проявлениями болезни. Это связано с широким внедрением в клиническую практику эхокардиографии, позволяющей проводить раннюю диагностику заболевания. Тем не менее, остается много нерешенных проблем в отношении причин, механизмов развития, ранней диагностики и специфического лечения ДКМП.