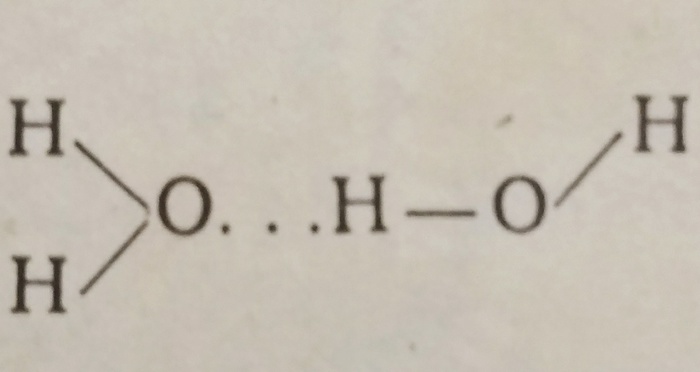диоксид водорода что это
Дигидроген моноксид
Ложную тревогу подняли Эриком Лехнер, Ларс Норпченер и Мэтью Кауфман в 1989 году, распространив в кампусе Калифорнийского университета в Санта-Крусе листовки, предупреждавшие о заражении дигидрогена монооксидом [2] Мысль возникла у Мэтью по аналогии с предупреждением о «гидроксиде водорода», опубликованном в мичиганской газете «Дюранд Экспресс», после чего трое приятелей решили придумать термин, который «звучал бы еще опаснее». Эрик напечатал предупреждение на компьютере, после чего листовка была размножена на копировальном аппарате.
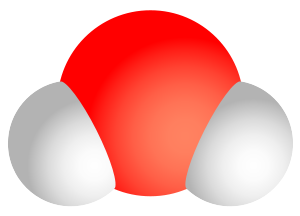
Монооксид дигидрогена — одно из научных англоязычных названий воды, как известно, имеющей формулу Н2О, где H2 «дигидроген» — двойного гидрогена (анг. hydrogen водород), а O — «монооксид» (кислород).
Содержание
Предупреждение на веб-сайте
Недавно исследователи открыли факт заражения наших водопроводных систем опасным химикатом. Этот химикат бесцветный, безвкусный и не имеет запаха. Правительство не предприняло никаких попыток регулирования этого опасного заражения. Данный химикат называется дигидрогена монооксид (Dihydrogen monoxide).
Химикат используется для следующих целей:
Несмотря на эти опасности, химикат активно и безнаказанно используется в индустрии. Многие корпорации ежедневно получают тонны химиката через специально проложенные подземные трубопроводы. Люди, работающие с химикатом, как правило, не получают спецодежды и инструктажа. Отработанный химикат тоннами выливается в реки и моря.
Мы призываем население проявить сознательность и протестовать против дальнейшего использования этого опасного химиката.
История
Будьте осторожны: дигидрогена монооксид
Если вы не знали об этом, то мы с улыбкой сообщаем вам об этом! Называется этот химикат дигидрогена монооксидом. А почему сообщаем с радостью? Да потому что речь идёт об обычной воде.
Не правда ли, неплохое название для воды – «дигидрогена монооксид»? Однако мало кто знает, оно обозначает именно воду. По причине неосведомлённости людей по этому поводу мистификация с дигидрогена монооксидом вызвала в своё время немало шума и послужила причиной массовой паники.
Но давайте обо всём по порядку.
Что за дигидрогена монооксид?
По сути, дигидрогена монноксид – это название воды, согласно системе наименований химических соединений «ИЮПАК». Все мы знаем, что вода имеет формулу «Н2О», в которой «Н2» является дигидрогеном, ведь присутствуют два атома водорода, а «O» является монооксидом, т.к. имеется всего один атом кислорода.
Здесь можно упомянуть о том, что в 2005 году номенклатура «ИЮПАК» была пересмотрена, но для неорганической химии всё еще нет каких-либо единых названий для химических соединений. Главной функцией химической номенклатуры является обеспечение отсутствия двусмысленности касаемо химических соединений, т.е. одним названием должно быть обозначено одно вещество. Обеспечение единого названия для химических веществ является второстепенным, несмотря даже на то, что количество допустимых имён является ограниченным. И название «дигидрогена монооксид» для воды вполне приемлемо.
В нашем случае, дигидрогена монооксид является научной шуткой и мистификацией, созданной с целью иллюстрации того, как может простое отсутствие научных знаний и умелое оперирование фактами стать причиной паники среди людей.
По общепринятым данным, впервые информация о химикате была распространена в 1989 году студентами Мэтью Кауфманом, Ларсом Норпченером и Эриком Лехнером среди других студентов Калифорнийского университета в Санта-Крусе. Они распространили в кампусе учебного заведения листовки, которые предупреждали о заражении веществом под названием «дигидрогена монооксид».
Такая идея возникла у Мэтью Кауфмана. Связана она была с предупреждением о «Гидроксиде водорода», которое было опубликовано в одной из газет Мичигана. В итоге, трое друзей приняли решение выдумать такой термин, который казался бы намного опаснее предыдущего. Эрик Лехнер набрал текст предупреждения на компьютере, а затем листовку размножили при помощи копировального аппарата. Данная листовка вызвала панику среди студентов, которая продолжалась до выяснения сущности указанного в сообщении химиката.
Предупреждение в Интернете
Впервые упоминание о дигидрогена монооксиде в Интернете было сделано, согласно газете «Pittsburgh Post-Gazette», «Объединением по запрещению дигидрогена монооксида» – несуществующей организацией, которая была придумана Крейгом Джексоном.
Смысл информации из предупреждения сводился примерно к следующему:
Не так давно учёные обнаружили факт заражения общедоступных водопроводных систем опаснейшим химическим веществом. Данное вещество не имеет цвета, вкуса и запаха. Правительством не было предпринято каких-либо мер по устранению этого представляющего опасность заражения. Представленное химическое вещество носит название «дигидрогена монооксид», а используется оно со следующими целями:
Невзирая на все эти опасности, химическое вещество активнейшим образом и абсолютно безнаказанно применяется в индустрии. Множество корпораций каждый день получают огромные количества этого химического вещества по специально проложенным для этого трубопроводам. Взаимодействующие с химическим веществом люди не снабжаются никакой спецодеждой; с людьми также не проводится соответствующего инструктажа. Отработанное химическое вещество в огромных объёмах сливается в водоёмы. Мы призываем всех граждан быть сознательными и выразить свой протест против последующего применения этого опасного для жизни химического вещества.
Развитие событий
В итоге, все события, связанные с дигидрогеном монооксида, развивались следующим образом:
В 1989 году Мэтью Кауфман, Ларс Норпченер и Эрик Лечнер сделали копии листовок и оповестили о дигидрогена монооксиде студентов, вызвав панику.
В 1994 году Крейгом Джексоном была создана интернет-страница для «Объединения за запрещения дигидрогена монооксида», что тоже вызвало панику.
В 1997 году четырнадцатилетний ученик школы из городка Айдахо-Фоллз (США) по имени Натан Зонер сумел собрать 43 голоса за запрещение химического вещества, произведя опрос 50 одноклассников. И за свой эксперимент, который он назвал «Насколько мы легковерны?», мальчик получил на научной ярмарке своего города первую премию. В качестве признания его исследования журналист Джеймс К. Глассман даже ввёл термин «зонеризм», который означает «применение факта, приводящего к ложным выводам публику, которая не обладает познаниями в науке и математике».
В 1998 году, первого апреля одним из членов австралийского парламента было объявлено о начале кампании, направленной на запрет дигидрогена монооксида на международном уровне, что вызвало немалую шумиху.
В 2007 году Джаки Дин (член парламента Новой Зеландии), не сумевшая распознать подвох, направила министру здравоохранения сообщение, в котором спрашивала о том, что планирует делать правительство, чтобы запретить крайне опасное представленное вещество. Месяц спустя, Джаки Дин оправдывалась в одном из интервью, говоря, что люди, которые прислали ей информацию о дигидрогена монооксиде, из «левого крыла», и вообще, она поступила правильно.
Итоги
Исходя из всего изложенного выше, можно заключить, что вся эта история с дигидрогена монооксидом является наглядной демонстрацией того, что множество людей по всему миру по причине своего незнания слепо доверяет научной терминологии и умело обыгранной информации. Поэтому, каждый из нас должен прилагать усилия к саморазвитию и самообразованию, дабы не стать жертвой чьего-то обмана или шутки.
А вот ещё несколько примеров распространения информации о вреде дигидрогена монооксида:
Ну что, кто готов подписать петицию за запрещение дигидрогена монооксида?
Диоксид водорода
Правда ли, что серебряная ложка обеззараживает стакан воды?
Издревле серебру приписывали очищающие и обеззараживающие способности. Во многом поэтому посуду для знати и для религиозных ритуалов часто делали именно из этого благородного металла. Мы решили проверить, обладает ли он реальными обеззараживающими свойствами.
Контекст. Истории и даже инструкции по использованию серебряной посуды в дезинфицирующих целях можно встретить не только в блогах и социальных сетях, но и в СМИ. Сайты, посвящённые здоровому образу жизни, советуют применять серебряную воду как профилактическое средство, а также для лечения многих заболеваний: простуды, бронхита, гайморита, гастрита.
О серебре. Самые древние изделия из серебра были обнаружены на территории Древнего Египта и относились ещё к додинастическому периоду (5000–3400 годы до н. э.). До середины II тысячелетия до н. э. серебро ценилось даже дороже золота. Историк Геродот отмечал, что в V веке до н. э. предводитель персов Кир II брал с собой в походы питьевую воду в серебряных кувшинах. Средневековые алхимики относили серебро к одному из благородных металлов и искали способ получения его из других веществ (платину к благородным металлам стали относить только в Новом времени, большое спасибо внимательным пикабушникам @megavoltage и @muravlyansky, которые заметили (1, 2) неточность в формулировке). Знать и особы королевской крови предпочитали использовать серебряную посуду, она же была популярна в христианских обрядах, во многом благодаря приписываемым ей бактерицидным свойствам. В Европе Нового времени коллоидные растворы серебра и его соли прописывали пациентам с различными заболеваниями: простудой, трофическими язвами, эпилепсией и гонореей.
Серебро — ковкий, довольно тяжёлый (тяжелее меди) металл серебристо-белого цвета, имеющий самую высокую электропроводность при комнатной температуре. Как представитель благородных металлов, серебро не растворяется в соляной и разбавленной серной кислоте, однако легко растворяется в ртути, образуя амальгаму. Атом серебра состоит из положительно заряженного ядра, внутри которого находятся 47 протонов и 61 нейтрон, а вокруг по пяти орбитам движутся электроны. При отрыве электрона атом становится электрически заряженной частицей — ионом.
Серебро может быть представлено в виде чистого металла, различных соединений (в основном солей) и коллоидного раствора, насыщенного именно положительно заряженными ионами. Точнее будет даже сказать, что коллоидное серебро со временем становится источником ионов серебра.
Использование в медицине. Современная медицина использует лишь несколько препаратов, в состав которых входят соли серебра. Например, «Протаргол» — противомикробный и противовоспалительный препарат местного действия, применяемый в основном в ЛОР-практике, «Колларгол» — раствор с вяжущим, антисептическим и противовоспалительным свойством, «Аргосульфан» — крем для лечения ожоговых, трофических, гнойных ран, а также пролежней. Важно отметить, что все они относятся к препаратам наружного применения.
Коллоидное серебро представляет собой наночастицы серебра, плавающие в воде или другой жидкости. Существуют и истинные растворы серебра (например, его нитрата), которые представляют собой ионы металла и кислотного остатка. При этом как само коллоидное серебро, так и его ионы действительно обладают антимикробным эффектом — они проникают в микробную клетку и разрушают её. По данным ВОЗ, необходимая концентрация для гарантированного антибактериального эффекта — 0,15 мг/л. В питьевой воде по СанПиН 2.1.4.1074-01 «Питьевая вода» максимально допустимое количество этого металла составляет лишь 0,05 мг/л, что в три раза меньше необходимого для обеззараживающего действия.
Важно отметить, что при хроническом превышении максимально допустимых уровней потребления серебра у человека развивается аргироз — кожные покровы приобретают серебристый или серо-синий оттенок. Причём изменения цвета кожи необратимо, даже лазерная терапия не оказывает существенного влияния. Одним из самых известных пациентов с этим состоянием был житель Калифорнии Пол Карасон. На протяжении многих лет он пил коллоидный раствор серебра, приготовленный в домашних условиях. Помимо аргироза, чрезмерное употребление серебра может привести к проблемам с почками и ЖКТ, судорогам и головным болям. В некоторых странах даже законодательно запрещено рекламировать коллоидное серебро как имеющее лечебный эффект, так как доказанной эффективности оно не имеет, при этом ионы серебра по токсичности превосходят тяжёлые металлы.
Правда, в случае использования серебряной посуды последствий для здоровья опасаться не стоит. Коллоидный раствор можно получить только с помощью специального инструмента — ионизатора, пропускающего через воду электрический ток, способствующий отцеплению электронов. Слабый коллоидный раствор будет содержать от 1 мг серебра на литр, более концентрированный — до 35. Ложка, просто опущенная в стакан с водой, не насытит воду ни опасной для организма (выше 0,05 мг/л), ни уж тем более необходимой для бактерицидного действия (0,15 мг/л) концентрацией.
Таким образом, просто опущенная в стакан серебряная ложка не создаст необходимую для антимикробного действия концентрацию. Однако при условии, что через воду будет пропускаться электрический ток, она фактически сможет обеззаразить стакан воды. Правда, пить очищенную таким способом воду будет опасно для человека по другой причине.
Ещё нас можно читать в Телеграме, в Фейсбуке и в Вконтакте. Традиционно уточняю, что в сообществах отсутствуют спам, реклама и пропаганда чего-либо (за исключением здравого смысла), а в день публикуем не больше двух постов.
Вода. Казалось бы, чего уж проще?
Такие связи гораздо менее прочны, чем ковалентные связи 0-Н внутри молекул, и всё же именно благодаря им взаимодействие молекул в воде гораздо сильнее, чем во многих других жидкостях (например, в жидких H²S, H²Se, H²Te).
В процессе теплового движения молекул водородные связи рвутся, но взамен тут же возникают новые.
Таким образом, в жидкой воде существует
динамическая система межмолекулярных водородных связей.
Иначе говоря, молекулы воды ассоциированы.
Именно повышенная прочность связей между молекулами H²О служит причиной аномально высокой температуры кипения воды.
Сильное межмолекулярное взаимодействие затрудняет переход молекул из жидкости в пар.
В кристаллах льда тоже существуют водородные связи, но здесь система таких связей статична, а следовательно, ещё более прочна, чем в жидкой воде.
Именно в этом причина аномально высокой температуры и теплоты плавления льда.
Рассмотрим теперь структуру льда более
внимательно.
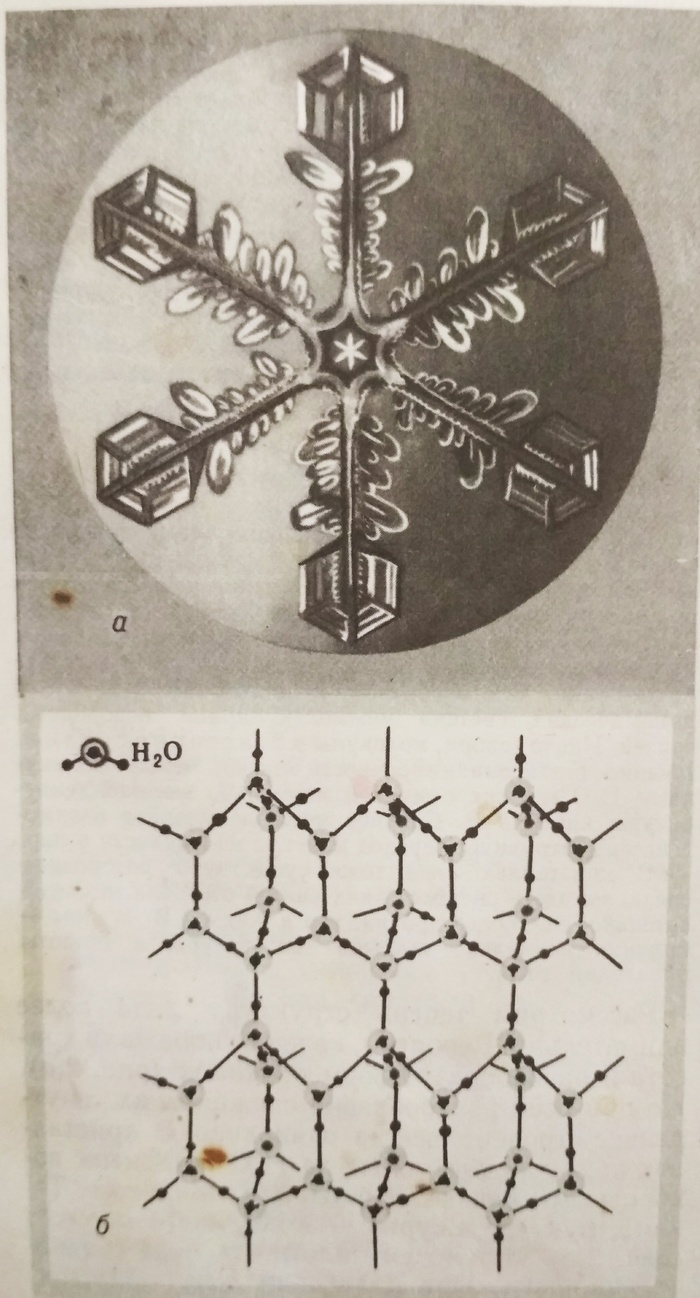
Вероятно, каждого поражали красота и разнообразие форм снежинок.
Но при всём разнообразии снежинок их внутреннее строение ВСЕГДА ОДИНАКОВО.
В кристаллах льда каждая молекула Н²0 соединена водородными связями с четырьмя соседними.
Такая структура ажурна, в ней много «пустот».
Вот почему плотность льда сравнительно низка.
При плавлении льда часть «пустот» заполняется «одиночными», и «сдвоенными» молекулами H²О, уже освободившимися из кристаллической решётки.
Поэтому плотность воды выше, чем у льда.
Такое увеличение плотности продолжается и при нагревании от 0 до
+4 °C.
Но при более высоких температурах начинает преобладать тепловое движение молекул, расстояния между отдельными молекулами H²0 увеличиваются, и изменение плотности становится «нормальным».
Поскольку тепловая энергия при нагревании воды расходуется не только на ускорение движения молекул Н²0, но и на разрыв водородных связей между ними, то и теплоёмкость воды оказывается столь большой.
Кстати, даже в парах воды, при
100 °C эти связи разорваны
ещё не полностью, так что из каждых 200 молекул Н²О примерно 7 попарно связаны между собой.
ХИМИЧЕСКИЕ СВОЙСТВА.
Молекула Н²О настолько прочна, что разрушить её можно лишь очень энергичным внешним воздействием.
Разложение воды по обратимой реакции:
2H²О=2Н²+О²
становится заметным лишь при нагревании до 2000 °С (термическая диссоциация).
Оно происходит и под действием ультрафиолетовых лучей (фотохимическая диссоциация).
Радиоактивное излучение разлагает воду с образованием водорода, кислорода, перекиси водорода и очень активных свободных радикалов.
Вода — слабый электролит.
При комнатной температуре лишь одна из 10 млрд. молекул диссоциирует.
Так что при 25 °С в чистой воде концентрации Н+ и OH- составляют всего 10-7 г-ионов/л.
Это соответствует водородному
показателю рН=7.
При повышении температуры электролитическая диссоциация воды усиливается.
При 700 °С и давлении 130000 атм концентрация Н+ становится такой же, как при обычных условиях у 10%-ной соляной кислоты.
Ион водорода Н+ в растворах не существует в свободном состоянии, а присоединяется к молекуле Н²О и образует ион гидроксония Н³О+.
Қак и все другие ионы, гидроксоний в водной среде, в свою очередь, гидратирован, то есть окружён несколькими молекулами H²0.
Водная оболочка Земли гидросфера — составляет около 71% земной поверхности.
В связанном состоянии вода находится и в земно коре — литосфере, причем подсчитано, что запасы такой воды (на секундочку!!) примерно равны массе свободной воды в гидросфере.
Найдено, что 1 км³ гранита при плавлении может выделить 26 млн. тонн воды.
Ещё больше «резервы» В., заключённые в
более глубоких недрах Земли — в мантии.
Считают, что здесь до 13 млрд. км³ воды, то есть, вдесятеро больше, чем в гидросфере.
Но на поверхность вулканы выносят лишь 1 км³ такой воды ежегодно.
Вода играла и играет определяющую роль
в геологической истории Земли, в формировании её теплового режима, климата и погоды.
Сегодня далеко не всё известно об этом интереснейшем, давно знакомом, но во многом загадочном, таком обильном и таком дефицитном веществе, О ПРОСТОЙ ВОДЕ.
Осторожно! Монооксид Дигидрогена
Недавно исследователи открыли факт загрязнения наших водопроводных систем опасным химикатом. Этот химикат бесцветный, безвкусный и не имеет запаха. Он убивает бесчисленное множество людей каждый год. Правительство не предприняло никаких попыток регулирования этого опасного заражения. Данный химикат называется «дигидрогена монооксид» (Dihydrogen monoxide). Химикат используется для следующих целей:
• В производстве как растворитель и охладитель
• В ядерных реакторах
• В производстве пенопласта
• В химических и биологических лабораториях
• В производстве пестицидов
• В искусственных пищевых добавках
• Химикат является основной составляющей кислотных дождей
• Способствует эрозии почвы
• Ускоряет коррозию и вредит большинству электроприборов
• Длительный контакт с химикатом в его твёрдой форме приводит к серьёзным повреждениям кожи человека
• Контакт с газообразной формой химиката приводит к сильным ожогам
• Вдыхание даже небольшого количества химиката грозит смертельным исходом
• Химикат обнаружен в злокачественных опухолях, нарывах, язвах и прочих болезненных изменениях тела
Несмотря на эти опасности, химикат активно и безнаказанно используется в индустрии. Многие корпорации ежедневно получают тонны химиката через специально проложенные подземные трубопроводы. Люди, работающие с химикатом, как правило, не получают спецодежды и инструктажа. Отработанный химикат тоннами выливается в реки и моря.
Мы призываем население проявить сознательность и протестовать против дальнейшего использования этого опасного химиката. Призываем депутатов немедленно принять закон запрещающий использование хранение и оборот данного вещества.
Дайте этот текст своим знакомым, коллегам, родственникам и задайте вопрос, готовы ли они выступить за запрет данного химиката? 80% согласятся с тем, что следует запретить данное вещество.
А если снять ролик, страшным голосом сообщить населению об опасности, навставлять картинок с трупами, дымящими трубами, дохлой рыбой и показать например на НТВ?
А если дать этот текст депутатам? Какова вероятность, что они запретят это вещество и будут поддержаны населением?
Между тем, H2 «дигидроген» — двойной гидроген (англ. hydrogen — водород), а O — «монооксид» (кислород). Н2О — Вода.
Вот так, руководствуясь собственной дремучестью, легковерием, отсутствием критического мышления можно запретить обыкновенную воду.
Пользуясь легковерием народа, и управляемостью через федеральные каналы, власть должна улучшать жизнь людей, их быт, воспитывать и просвещать, чтобы войти в историю как мудрые правители создавшие новую, процветающую Россию. Вместо этого идет повальная дебилизация, переворачивание всего и вся с ног на голову и восхищение своей безнаказанностью.
Кин дза дза стала реальностью. Это и надувание шаров господина пэ жэ, это и супертехнологии, обладая которыми можно летать по космосу, но жить под землей в рванье. Это и разделение на чатлан и пацаков, где одним можно, а другим нельзя. Это и желание массы носить малиновые штаны, чтобы плевать на всех и эцилоп не мог их бить по ночам, никогда….
Диоксид водорода что это
Согласно недавнему исследованию, опубликованному в журнале Applied Materials & Interfaces, группа ученых создала новый аэрогель, который повышает эффективность преобразования света в водородную энергию, производя «до 70 раз больше водорода», чем альтернативные методы. Это может стать началом нового способа производства водородного топлива в промышленных масштабах. В результате появятся автомобили, работающие на водороде, новые силовые установки для самолетов и возможно, энергосистемы будущего.
реклама
Легированные наночастицы могут поглощать больше солнечного света
Аэрогели на основе наночастиц могут служить фотокатализатором, который позволяет ускорять химические реакции (в присутствии солнечного света) для получения важных в современном мире веществ, в том числе водорода. Оптимальным материалом для производства фотокатализаторов является полупроводник диоксид титана (TiO2). Но у диоксида титана есть серьезный недостаток: он поглощает только ультрафиолетовое излучение, что составляет всего 5% от всего потока солнечного излучения. Чтобы задействовать их в энергетике, фотокатализаторы должны работать более эффективно и использовать более широкий диапазон длин волн.
Именно эту цель поставили перед собой профессор Маркус Нидербергер и его команда из лаборатории многофункциональных материалов ETH Zurich (Швейцарская высшая техническая школа Цюриха). Аспирант Нидербергера, Джунгоу Квон, искала новые и альтернативные методы повышения эффективности аэрогелей, полученных из наночастиц диоксида титана (TiO2). Она обнаружила, что при «легировании» наночастиц TiO2 азотом, (в результате чего отдельные атомы кислорода заменяются атомами азота), аэрогель становится способным поглощать даже видимые части солнечного спектра. Кроме того, этот процесс позволил сохранить пористую структуру аэрогеля.
Аэрогели с использованием палладия могут генерировать в 70 раз больше водорода
Для производства аэрогеля Квон сначала использовала наночастицы диоксида титана TiO2 в сочетании с небольшим количеством благородного металла палладия (Pd). Использование палладия в данном случае является обязательным, поскольку это важный элемент в фотокаталитическом производстве водорода.
Далее Квон поместила аэрогель, резервуар, в который подавался газообразный аммиак, заставляя атомы азота (N) встраиваться в кристаллическую структуру наночастиц TiO2, сообщается на сайте ETH Zurich.
Для того чтобы проверить, действительно ли аэрогель, модернизированный подобным образом, может повысить эффективность необходимой химической реакции ( преобразования метанола (CH3OH) и воды в водород), Квон изготовила специальный реактор. Затем она ввела в аэрогель водяной пар и метанол, после чего облучила смесь светодиодными лампами. В результате образовалось газообразное вещество, которое проникало через поры аэрогеля, где на поверхности диоксида титана (TiO2) и наночастиц палладия (Pd) оно превращалось в водород H2.
Аэрогель VS Огонь VS Вода