диосгенин что это такое
Климактерические расстройства и средства растительного происхождения как альтернатива заместительной гормонотерапии
Фитогормоны, как альтернатива ЗГТ, значительно снижают частоту климактерических симптомов, могут использоваться для профилактики остеопороза и рака молочной железы, а также улучшают внешний вид женщины.
О. В. Евдокимова, к. м. н., кафедра фармации с курсом социальной фармации ММА им. И. М. Сеченова
Климакс – естественный этап в жизни женщины, переходный период от репродуктивной фазы жизни к старости. Однако высокая частота и тяжесть симптомов дефицита половых гормонов значительно снижают качество жизни и превращают этот период в своеобразную болезнь. Различные по степени тяжести проявления климактерического синдрома встречаются у 40-60% женщин старше 40 лет.
Патогенетическим методом коррекции климактерических нарушений являются заместительная гормональная терапия (ЗГТ). Экзогенные эстрогены, принимаемые в период менопаузы, вызывают быстрое ослабление климактерических симптомов, снижают риск сердечно-сосудистых заболеваний и остеопороза. Тем не менее, в большинстве европейских стран лишь 10-15% женщин в период постменопаузы регулярно применяют ЗГТ.
К применению ЗГТ имеются серьёзные противопоказания, такие как:
• рак молочной железы, в настоящее время или подозрения на него,
• эстрогензависимые злокачественные опухоли (рак эндометрия, молочной железы),
• гинекологические кровотечения неясной этиологии,
• нелеченая гиперплазия эндометрия,
Альтернативные методы коррекции климактерических нарушений – это методы терапии, обладающие сходным с гормональной терапией механизмом действия, но не вызывающие отрицательных побочных влияний (пролиферативную активность в миометрии и эндометрии, молочной железе, повышения тромбогенного потенциала крови).
В настоящее время существует несколько видов альтернативной терапии, и одним из них является применение натуральных продуктов: фитоэстрогенов и фитогормонов.
Фитоэстрогены – это природные вещества, содержащиеся в растениях и обладающие эстрогенным и антиэстрогенным эффектом. По сравнению с эстрадиолом-17b они обладают более слабым эффектом (100-1000 раз). Но фитоэстрогены хорошо усваиваются организмом человека, в 5000 раз лучше накапливаются в организме, чем эстрогены. Правда, накапливаются медленно.
Фитоэстрогены обладают следующими свойствами:
• незначительно повышают синтез белка, связывающего эстрогены, что ведёт к некоторому снижению уровней свободного эстрадиола и прогестерона,
• связываясь с эстрогенными рецепторами, вытесняют эстрадиол из связи с рецепторами, что может частично объяснять их антипролиферативный эффект,
• ингибируют ферменты, участвующие в функции рецепторов, контролирующих факторы роста,
• устраняют активность свободных радикалов, способствуют снижению окисления ЛПНП и снижают концентрацию ЛПНП,
• снижают риск возникновения рака предстательной железы, молочной железы и толстого кишечника,
• они активно участвуют в обменных процессах костной ткани. Стимулируют остеогенез, препятствуют потере кальция организмом,
• снижают метаболические симптомы – сухость влагалища, недержание мочи, боли в мышцах и суставах,
• снижают утомляемость, нормализуют либидо, улучшают настроение.
Особенность фитоэстрогена состоит в том, что он способен уменьшить уровень человеческого эстрогена, если он завышен, и увеличивать уровень эстрогена, что необходимо в период менопаузы. Фитоэстрогены оказывают как эстрогенное, так и противоэстрогенное действие, в зависимости от концентрации циркулирующих эндогенных эстрогенов в крови, их количества и чувствительности рецепторов эстрогена. Чем выше концентрация фитоэстрогенов, тем более выражен антиэстрогенный эффект.
Структура фитоэстрогенов подобна структуре эндогенных эстрогенов, что позволяет фитоэстрогенам связываться с эстрогенными рецепторами и проявлять свою эстрогенную активность. В желудочно-кишечном тракте под действием кишечной флоры, ферментов и клеток слизистой оболочки происходит метаболическая конверсия фитоэстрогенов, которая приводит к формированию гетероциклических фенолов. Именно эти соединения схожи по своей структуре с эстрогенами. Все фитоэстрогены способны активизировать специфические рецепторы на мембранах клеток.
Выделяют три основных класса фитоэстрогенов:
1. Изофлавоны (генистеин, даидзеин, биоканин А, формононетин).
2. Лигнаны (энтролактон, энтрадиол).
3. Куместаны (куместрол).
Изофлавоны присутствуют почти исключительно в бобовых – соя, фасоль, клевер красный, солодка, чечевица. Кроме того, они присутствуют в винограде (красное вино).
Высокой концентрацией лигнанов (растительные волокна) отличаются семена льна, более низкой – цельные зерна (рожь, рис), орехи и семена, фрукты (цитрусовые, яблоки, вишня), овощи (шпинат, морковь, брокколи, чеснок, петрушка).
Куместаны в небольшом количестве содержатся в клевере красном, люцерне.
Фитогормоны – это природные вещества, содержащиеся в растениях, не обладающие эстрогенным эффектом, но способные положительно влиять на типичные симптомы климактерических нарушений, а также на симптомы предменструального синдрома, альгодисменореи, менорагии и др.
Они значительно снижают частоту климактерических симптомов, могут использоваться для профилактики остеопороза и рака молочной железы, а также улучшают внешний вид женщины.
Показаниями к применению фитогормонов при климаксе являются:
противопоказания к ЗГТ,
климактерический синдром легкой и средней степени тяжести,
остеопороз (в комплексной терапии),
онкологические заболевания половых органов, рак молочной железы.
Фитогормоны содержаться в цимицифуге (клопогоне), рапонтицине, мельброзии, сое, диоскореи.
В клопогоне и рапонтицине фитогормоны представлены терпенгликозидами. В мельброзии кроме белков и липидов содержатся флавоноиды. В диоскореи фитогормоны представлены стероидными сапонинами (диосгенин).
Кроме веществ, обладающих эстрогеноподобным действием, в растениях содержатся соединения – стероидные сапонины (диоскорея японская), которые аналогичны другому гормону – прогестерону. Они применяются для снятия болезненных симптомов. Диоскорея способствует укреплению костей.
Диосгенин, содержащийся в диоскореи, усиливает чувствительность рецепторов к прогестерону. Прогестероновой активностью обладает также витекс священный, который стимулирует выработку лютеинизирующего гормона, который в свою очередь стимулирует выработку прогестерона.
Прогестеронмодулирующим действием обладает и сумма токоферолов (дудник) и примула вечерняя.
При недостаточности функции надпочечников используют солодку, юкку, володушку и другие кортикостероидмодулирующие средства.
Таким образом, средства растительного происхождения можно рассматривать в качестве альтернативы ЗГТ.
В качестве средств, рекомендуемых для нормализации гормонального баланса женского организма, можно предложить БАДы компании Santegra:
1. MenoFix МеноФикс – витамин Е и витекс священный (прутняк) обладают прогестеронмодулирующим действием, клопогон кистевидный (цимецифуга) является селективным эстрогенорецепторным модулирующим активатором.
2. PerFem Forte ПерФем Форте – изофлавоноиды клевера и сои обладают эстрогенподобными свойствами, а тритерпеновые сапонины клопогона является селективными эстрогенорецепторными модулирующими активаторами.
3. Alfalfa Алфалфа, куместрол и изофлавоноиды люцерны повышают лактацию, люцерна обладает антисклеротическим действием, т. к. способствует снижению уровня холестерина в крови.
4. VAG Forte – фитогормоны клопогона рекомендуются при нарушениях менструального цикла, ПМС, воспалительных процессах в геникологии.
5. Wild Yam GP Дикий Ямс – диоскорея содержит прогормоны (диосгенин – природный предшественник прогестерона), из которых в организме синтезируются половые гормоны. Стероидные сапонины, попадая в организм женщины, нормализуют ее гормональный статус, регулируют менструальный цикл, устраняют неприятности (спазмы, судороги), связанные с пре – и постклимактерическими изменениями. Диоскорея благоприятно влияет на желтое тело и сохранение беременности. Её рекомендуют при ранних токсикозах, для препятствования чрезмерной выработке эстрогена при эндометриозе.
Стероидные сапонины диоскореи способны связывать холестерин, снижать артериальное давление, нормализовывать сон, улучшать память.
Заместительная гормональная терапия для мужчин с возрастным андрогенным дефицитом
Специализация: урология, андрология
Синдром возрастного андрогенодефицита у мужчин — это нарушение биохимического баланса, возникающее в зрелом возрасте по причине недостаточности андрогенов в сыворотке крови, нередко сопровождающейся снижением чувствительности организма к андрогенам. Как правило, это приводит к значительному ухудшению качества жизни и неблагоприятно сказывается на функциях практически всех систем организма. Естественно, что огромный интерес вызывают вопросы терапии андрогенного дефицита, поскольку именно она ставит сложную задачу перед врачом-клиницистом: выбрать из широкого арсенала методов и препаратов гормональной терапии наиболее оптимальный, сочетающий в себе качество, эффективность, а также удобство в применении.
В настоящее время врачи-урологи и андрологи наиболее часто применяют заместительную терапию тестостероном. Данный метод позволяет решить целый ряд задач: снизить симптомы возрастного андрогенодефицита путем повышения либидо, общей сексуальной удовлетворенности, уменьшить выраженность либо полностью ликвидировать вегетососудистые и психические расстройства. Кроме того, если заместительная терапия тестостероном применяется более 1 года, у пациентов наблюдается повышение плотности костной массы, снижение выраженности висцерального ожирения, а также нарастание мышечной массы. Также после длительного курса лечения нормализуются лабораторные параметры: наблюдается повышение уровня гемоглобина или количества эритроцитов, снижение уровня ЛПОНП (липопротеинов очень низкой плотности) и ЛПНП (липопротеинов низкой плотности) при неизмененном уровне ЛПВП (липопротеинов высокой плотности). Многие авторы считают, что такого эффекта можно достичь, добившись восстановления концентрации тестостерона в крови до нормального уровня (10–35 нмоль/л). Следует также учитывать, что *17α-алкилированные препараты тестостерона флуоксиместеролон и метилтестостерон обладают выраженной гепатотоксичностью, оказывая токсическое и канцерогенное влияние на печень, а также отрицательно воздействуют на липидный спектр крови (резкое повышение уровня атерогенных и снижение уровня антиатерогенных липопротеидов). Поэтому применение этих производных тестостерона в клинической практике было прекращено.
В настоящее время из пероральных препаратов предпочтение отдается тестостерону ундеканоату (Андриол). Указанный эфир тестостерона не подвергается первичному печеночному метаболизму, так как всасывается в лимфатическую систему, минуя печень. После гидролиза тестостерона ундеканоата в лимфатической системе в системный кровоток поступает тестостерон, который оказывает лечебное действие как сам по себе, так и через свои основные метаболиты – дигидротестостерон (ДГТ) и эстрадиол, обусловливающие полный спектр андрогенной активности тестостерона. Таким образом, тестостерона ундеканоат сохраняет свою активность при пероральном применении. Вместе с этим, минуя систему воротной вены и прохождение через печень, тестостерона ундеканоат не оказывает гепатотоксического и гепатоканцерогенного действия. Период полувыведения препарата из плазмы составляет 3–4 часа. В связи с этим режимом дозировки тестостерона ундеканоата является 2-кратный прием в течение суток, это не всегда удобно для пациентов. Исходя из собственного опыта, мы считаем, что Андриол является достаточно мягким препаратом и помогает только в случаях начальных и минимальных проявлений возрастного андрогенного дефицита.
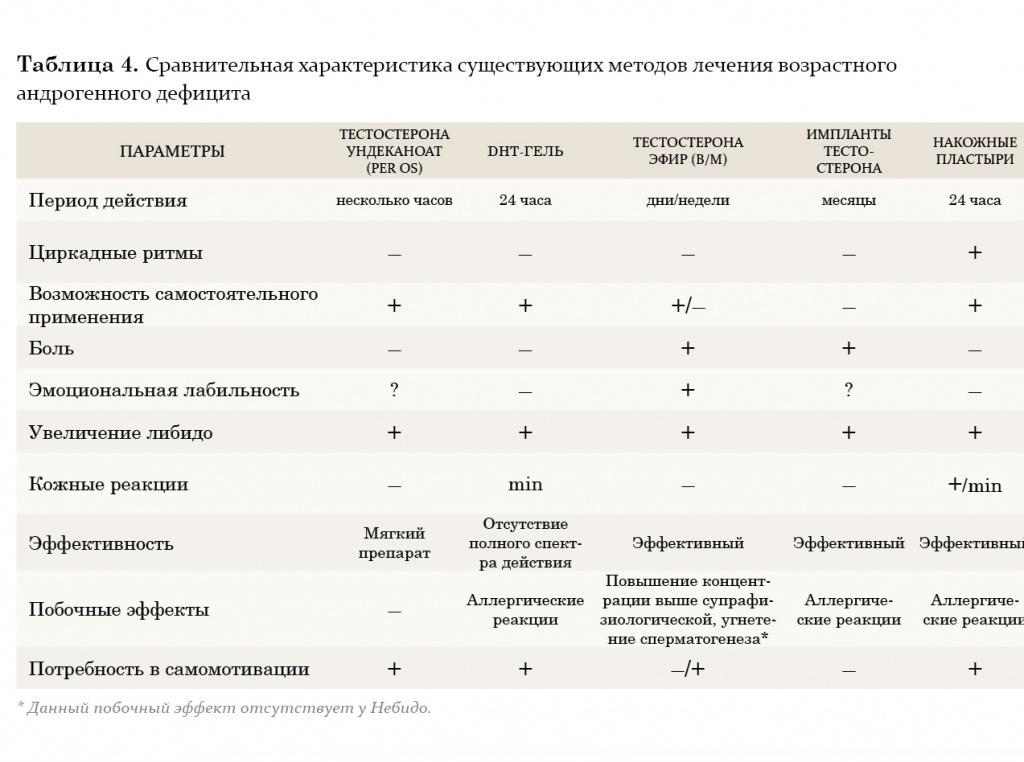
Внутримышечные инъекции пролонгированных эфиров тестостерона также являются широко применяемым методом заместительной терапии у мужчин с гипогонадизмом. Два наиболее известных эфира тестостерона – тестостерона ципионат и тестостерона энантат, имеют похожую фармакокинетику. При внутримышечном введении этих препаратов создается депо, из которого препарат высвобождается в кровеносное русло. В течение первых 2–3 дней после введения уровень тестостерона повышается до супрафизиологических цифр, а затем медленно снижается на протяжении последующих 2 недель до субнормальных значений. Положительной стороной этих препаратов является длительность терапевтического действия. Тем не менее резкие изменения в уровне тестостерона, зачастую ощущаемые самим пациентом в виде подъемов и снижения либидо, общего самочувствия, эмоционального статуса, являются нежелательными качествами данных препаратов. В связи с этим большие надежды возлагаются на новый препарат Небидо (Шеринг), фармакокинетика которого значительно отличается от других эфиров тестостерона. Небидо представляет собой тестостерона ундеканоат и является препаратом, не обладающим пиком повышения концентрации.
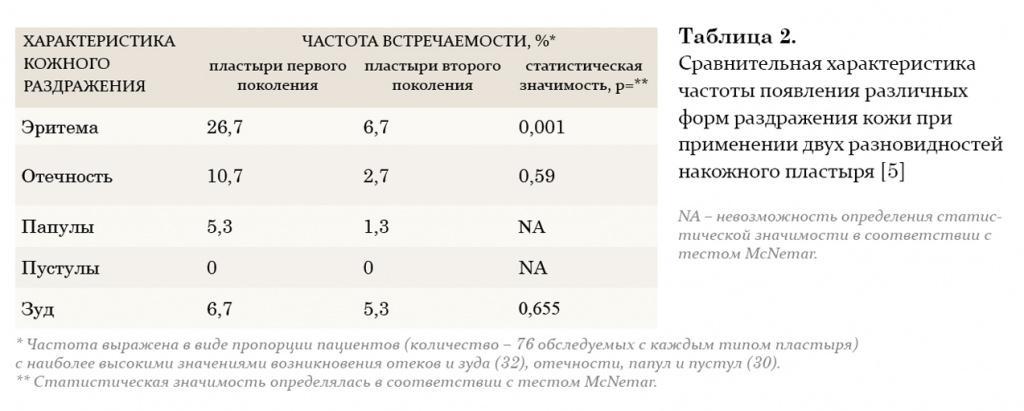
На протяжении двух последних десятилетий большое внимание уделяется исследованию преимуществ трансдермального применения препаратов тестостерона. Мошоночные пластыри обладают эффективным действием, и некоторые пациенты считают их наиболее удобным методом лечения. Накожные пластыри наиболее хорошо воспринимаются пациентами и дают эффективный уровень тестостерона в сыворотке крови. Тем не менее существуют некоторые различия между этими двумя разновидностями пластырей относительно их аллергогенного потенциала: при применении накожных пластырей отмечается гораздо большая частота возникновения аллергических реакций и раздражения кожи, чем при применении мошоночных пластырей.
Гель тестостерона обладает всеми преимуществами пластырей и не вызывает развития кожных реакций. Единственный его недостаток заключается в наличии возможности контакта геля с партнершей и недостаточном количестве долговременных исследований по его применению.
Трансдермальный путь введения тестостерона позволяет избежать его первичного метаболизма в печени и инактивации, как это происходит при применении пероральных андрогенных препаратов, а также позволяет имитировать циркадные ритмы высвобождения физиологического немодифицированного тестостерона и его естественных метаболитов, эстрадиола и ДГТ. К тому же терапию с использованием пластырей и геля в случае необходимости можно легко прервать. К положительным моментам этого метода лечения также относится низкий риск возникновения лекарственной зависимости.
Европейский препарат 5-α-дигидротестостерон-гель (ДГТ) хотя и признан эффективным, однако неизвестно, оказывает ли изолированное применение неароматизированного андрогена, каким является ДГТ, такое же действие, как тестостерон, в связи с тем, что метаболиты тестостерона включают эстрадиол. По мнению многих авторов, применение препарата не рекомендуется, так как ДГТ вследствие невозможности превращения в эстрадиол не обладает полным спектром терапевтических свойств тестостерона (например, влиянием на костную ткань и сердечно-сосудистую систему).
Некоторые из препаратов заместительной терапии, такие как тестостерона ундеканоат, ДГТ-гель и мошоночные пластыри, вызывают существенное увеличение концентрации ДГТ в сыворотке крови. ДГТ известен как главный андроген простаты, и в связи с этим проводилось много дискуссий по поводу способности его вызывать заболевания предстательной железы. Однако, несмотря на эти предположения, в последнее 10-летие не зафиксировано данных в пользу увеличения частоты возникновения патологии простаты при назначении препаратов ДГТ.
Таким образом, существует множество препаратов заместительной андрогенотерапии, однако все они имеют те или иные побочные эффекты, а также обладают угнетающим действием на сперматогенез. В последнее время появляется все больше работ, демонстрирующих вторичный характер возрастного андрогенного дефицита. Согласно материалам ВОЗ, получены данные о сохранении секретирующей функции клетками Лейдига у пожилых мужчин, что позволило ученым предложить принципиально новый подход в лечении возрастного андрогенного дефицита, основанный на стимуляции синтеза эндогенного тестостерона.
Однако не стоит забывать, что наряду с абсолютными противопоказаниями для заместительной терапии андрогенами (рак грудной и предстательной желез) существуют и дополнительные (доброкачественная гиперплазия предстательной железы с выраженной обструкцией, пролактинома, полицитемия). К относительным противопоказаниям относятся нарушения сна в виде апноэ, обструктивные заболевания легких, интенсивное курение.
К побочным эффектам андрогенов относятся усиление ночного апноэ, полицитемия, гинекомастия, приапизм, задержка жидкости, повышение АД, отеки, увеличение размеров простаты, торможение сперматогенеза.
То есть сегодня существуют методы лечения возрастного андрогенного дефицита, которые можно разделить на две группы, принципиально различающиеся по механизму действия:
заместительная терапия экзогенными андрогенными препаратами; терапия, стимулирующая синтез эндогенного тестостерона.
Таким образом, можно сказать, что оптимального для всех средства для лечения возрастного андрогенного дефицита у мужчин не существует. И к выбору препарата следует подходить строго индивидуально, учитывая возраст пациента, индекс массы тела, необходимость сохранения сперматогенеза, показатели гематокрита и сопутствующие заболевания.
Диосгенин – это гликозид растительного происхождения, который содержится в некоторых продуктах питания. Организм человека получает этот элемент только извне, а его воздействие может быть довольно широким и эффективным.
Полезные свойства
Элемент такого типа относится к категории анаболических препаратов и содержится в таких растениях, как пажитник, косту, триллиум и тригонелла. Полезные свойства не ограничиваются противовоспалительным эффектом и при правильном применении могут оказывать следующее воздействие на организм:
понижают уровень холестерина в крови и служат отличным профилактическим средством от образования холестериновых бляшек;
стабилизирует артериальное давление и снижает опасности спазмов сосудов;
снижает риск спазмолитического характера;
воздействуют на метаболизм организма;
обладают способностью стабилизировать соотношение женских гормонов.
Диосгенин входит в группу фитоэстрогенов, которые применяются для нормализации гормонального фона женщины. Лечебный курс такого препарата поможет нормализовать менструальный цикл, ослабляют симптомы наступления климакса и поддерживают тонус женских половых органов. Эстрогенный эффект элемента обладает сильным воздействием на выработку гормонов, поэтому его не следует принимать мужчинам.
Противопоказания и применение
Помимо стимуляции выработки необходимых женских гормонов, диосгенин может использоваться и для облегчения следующих симптомов:
Диосгенин обладает антиоксидантным свойством и предотвращает старение организма, восстанавливая клетки изнутри.
Гликозид обладает жиросжигающим эффектом и способствует ускорению метаболизма.
Эффективно воздействует на очищение крови от вредных элементов и стимулирует дыхательную систему.
Противопоказаний к применению диосгенина нет, но его не следует принимать в больших количествах мужчинам. Экстракт такого типа содержит большое количество фитоэстрогенов, которые воздействуют на женскую репродуктивную систему. Активность препарата выражается в стимуляции процессов выработки разнообразных гормонов для поддержания активности и нормализации половой системы.
Одно свойство диосгенина позволило включить его в состав тестостеронового бустера для мужчин, которые активно занимаются спортом. Элемент помогает быстрее восстановиться после усиленной тренировки и повышает физическую активность во время тренировки.
Передозировка диосгенином не имеет яркого выражения и симптоматики, а все излишки быстро выводятся из организма. Рассчитать суточную дозу поможет консультирующий врач, у которого будут все данные о нарушении гормонального фона. При этом, лечебный курс не следует принимать самостоятельно, без предварительного анализа содержания всех гормонов. Получить диосгенин с пищей довольно сложно, потому что он содержится в экзотических растениях. Но можно использовать концентрированный экстракт, который будет намного эффективнее.
Инновационная технология таблеток «ДИОСКЛЕФИТ», на основе Диоскореи Кавказской
ВВЕДЕНИЕ
Известно, что атеросклероз является одной из главных причин высокой общей смертности в современном урбанизированном обществе [1–3]. Он развивается как хроническое заболевание артерий эластического и мышечно-эластического типа вследствие нарушения липидного и белкового обмена и сопровождается отложением холестерина и некоторых фракций липопротеидов при их избыточном присутствии в кровотоке [4–6].
Существует множество представлений о механизмах возникновения атеросклеротических отложений («бляшек») и их профилактики, однако все они сводятся к обоснованной необходимости контролировать уровень концентрации в крови так называемого «плохого» холестерина [7].
На сегодняшний день установлено, что правильное питание является важным, но не единственным фактором, влияющим на развитие атеросклероза, в частности, роль жиров животного происхождения в патогенезе пересматривается и они подвергаются своеобразной реабилитации, в то время как на первый план выходит полиэтиологическая теория, включающая множество причин атеросклероза ― малоподвижный образ жизни, диабет, вредные привычки, воспалительные процессы и др. [2, 4, 7].
Одним из факторов развития атеросклероза и сопутствующих ему заболеваний является недостаточное поступление в организм минорных и эссенциальных биологически активных веществ (БАВ) животного и растительного происхождения, например полиненасыщенных жирных кислот (омега-3, омега-6 и др.), мелатонина, токоферолов, водорастворимых витаминов, полифенолов, фитостеринов, тритерпенов, сапонинов и др. [8, 9]. Ставшая уже хронической нехватка данных веществ в повседневном рационе человека, определяет актуальность исследований по созданию новых лекарственных препаратов и функциональных разработок, призванных обеспечить организм необходимым количеством природных БАВ, обладающих антиатеросклеротической и противовоспалительной активностью.
Целью данной работы является обобщение литературных данных об опыте медицинского применения корневищ с корнями диоскореи в терапии сердечно-сосудистых заболеваний, обоснование состава и разработка технологии таблеток «Диосклефит», содержащих сумму БАВ диоскореи кавказской, вербены лекарственной и клевера лугового. Новизна проводимых исследований заключается в использовании в составе таблеток нативного высушенного лекарственного растительного сырья (ЛРС) в виде высокодисперсного, так называемого микронизированного, порошка, а также полученного из того же сырья полиэкстракта, позволяющего исключить введение традиционно применяемых вспомогательных компонентов.
Опыт применения диоскореи в терапии сердечно-сосудистых заболеваний
Диоскорея кавказская ― эндемичное растение Кавказа, встречается главным образом в западной части Закавказья ― в Краснодарском крае, Республике Адыгея, а также в Абхазии [10, 11]. Естественные запасы диоскореи очень ограничены, поэтому она была занесена в Красную книгу, введена в культуру. Перемены, произошедшие в постсоветское время, привели к тому, что на сегодняшний день государственное промышленное возделывание диоскореи не осуществляется. Опытное промышленное производство сырья диоскореи кавказской становится задачей малых частных коммерческих предприятий.
Лекарственным растительным сырьем диоскореи служат подземные органы ― корневища с корнями, которые заготавливаются в течение всего вегетативного периода, с конца апреля до глубокой осени.
Биологически активные вещества в составе корневищ с корнями диоскореи кавказской представлены стероидными сапонинами, содержание которых может достигать 10 % от массы высушенного сырья [10, 12]. Основным соединением сапониновой природы, определяющим активность препаратов диоскореи, является рамноглюкозид диосгенина ― диосцин (рисунок 1) [10, 13].
Рисунок 1. Химическое строение диосцина
Таким образом, создание на основе диоскореи кавказской лекарственного препарата, предназначенного для комплексной терапии заболеваний, вызванных гиперхолестеринемией, атеросклерозом различной локализации, хронической гипертонией, реабилитации после инсульта и инфаркта, является актуальной задачей.
Инновационные подходы в технологии препаратов диоскореи
Основными целевыми биологически активными веществами, извлекаемыми из корневищ с корнями диоскореи, являются сапонины. Технология, по которой получают очищенную сумму водорастворимых сапонинов диоскореи, включает в себя несколько основных стадий.
Собранное в течение всего вегетационного периода сырье, высушенное и измельченное до размера частиц не более 7 мм, исчерпывающе извлекают спиртом 80 % методом дробной мацерации. Извлечения фильтруют, упаривают в роторно-пленочном испарителе под вакуумом до полного удаления спирта. Водный остаток охлаждают и выдерживают при температуре не выше 10 °С для осаждения нерастворимых в воде компонентов, которые затем отделяют на фильтре.
Фильтрат упаривают на роторном испарителе под вакуумом до густой консистенции, выгружают в горячем виде на рабочую поверхность полочного вакуум-сушильного шкафа и сушат до остаточной влажности не более 3,5 %. Выход субстанции от исходного сырья может варьировать от 9 % до 50 % и более. Готовый продукт (экстракт сухой) представляет собой аморфный порошок от светло-коричневого с желтоватым оттенком до коричневого цвета, гигроскопичный; при попадании на слизистую оболочку способен вызывать раздражение. Стандартизуется субстанция методом спектрофотометрии по содержанию суммы фуростаноловых агликонов, которых в пересчете на диосгенин должно быть не менее 1,0 %, или по содержанию сапонинов в пересчете на диосцин, которых должно быть не менее 17 %.
Одним из перспективных направлений развития фитотехнологий является включение в состав лекарственной формы стандартизованного ЛРС в виде мелкодисперсного порошка. В частности, такие подходы реализованы в лекарственных препаратах «Аллохол, таблетки, покрытые оболочкой», «Таблетки от кашля», биологически активной добавке к пище «Гинкготропил» и др. [28, 29, 30]. Данное направление активно развивается компанией «Витаукт» (Республика Адыгея) при создании новых функциональных разработок, включая таблетки «Диосклефит» (Diosklephyt). Включение лекарственного растительного сырья в виде высокодисперсного порошка в состав таблеток является прогрессивным направлением, имеющим ряд достоинств, среди которых основные – сохранение нативного комплекса БАВ, соответственно придание современного дизайна растительным компонентам, хорошо зарекомендовавшим себя в народной и официнальной медицине, точность дозирования, удобства и преимущества таблеток как лекарственной формы.
Компоненты таблеток «Диосклефит» подобраны с учетом потенциальных полезных свойств БАВ включенных в него лекарственных растений, опыта их практического применения в народной медицине и в составе многочисленных разработок, относящихся к лечебной и профилактической медицине и здоровому питанию (из расчета на одну таблетку):
Вербена лекарственная (Verbena officinalis L, сем. вербеновые ― Verbenaceae) ― многолетнее травянистое растение высотой до 1 м. Стебель прямостоячий, кверху ветвистый; нижние листья черешковые, обратнояйцевидные, трехраздельные; верхние – сидячие, ланцетовидные; цветки мелкие, светлолиловые, собраны в длинные тонкие колосовидные тирсы. Вербена встречается в европейской части России, на Кавказе, в Центральной Азии.
Трава вербены заготавливается во время цветения, содержит эфирное масло, иридоиды (аукубин, вербеналин), тритерпеновые сапонины (лупеол, урсоловая кислота), кумарины, флавоноиды (артеметин), стерины (β-ситостерин). Вербены трава входит в Британскую травяную фармакопею и фармакопеи ряда европейских стран как сырье, обладающее противолихорадочным, потогонным и противомалярийным действием. В народной медицине вербена используется многогранно, в основном при простудных заболеваниях, опухолях различного генеза, как общеукрепляющее, а также при заболеваниях печени и почек, для очистки крови и др. [25].
Клевер луговой, или клевер красный (Trifolium pratense L., сем. бобовые – Fabaceae) – многолетнее травянистое растение с ветвистым стеблем высотой 15–50 см. Листья тройчатосложные, листочки нижних листьев яйцевидные, верхних – эллиптические, со слегка заостренной верхушкой. Соцветия головчатые, реже яйцевидные, книзу окружены верхушечными листьями с расширенными прилистниками.
Цветки мотыльковые, от розового до темно-красного цвета.
Цветки клевера, как и трава, содержат эфирное масло, флавоноиды (трифолин, формононетин, ононин, генистеин, кверцетин и др.), кумарины, обладающие эстрогенными свойствами, витамины, стерины (β-ситостерин). По экспериментальным данным, флавоноиды клевера обладают противосклеротическим и анаболическим действием. В народной медицине трава и цветки клевера в составе сборов применяется как отхаркивающее, мочегонное, желчегонное и противосклеротическое средство [25].
Сырье данных растений входит в состав сборов и комплексных препаратов, предназначенных для лечения и профилактики атеросклероза, нарушений обменных процессов и для улучшения капиллярного кровотока [27, 31, 32]. К ним, в частности, относятся биологически активная добавка к пище «Вербена ― чистые сосуды» (капли для приема внутрь, сбор. капсулы), лекарственный препарат «Атероклефит» (экстракт для приема внутрь жидкий) [27, 31].
Наиболее активным классом БАВ, определяющим полезные фармакологические свойства таблеток «Диосклефит», являются сапонины диоскореи кавказской.
Учитывая ограниченные запасы диоскореи в природе, компания «Витаукт» успешно реализует перспективную задачу ― обеспечить собственные потребности в корневищах с корнями диоскореи кавказской путем введения ее в культуру на плантациях. Сырье вербены лекарственной и клевера лугового заготавливается от дикорастущих растений в соответствии с правилами сбора, сушки и хранения ЛРС.
Схема производства таблеток «Диосклефит» представлена на рисунке 2 и состоит из следующих основных стадий:
Рисунок 2. Схема производства таблеток «Диосклефит»: A ― корневища с корнями диоскореи кавказской; Б ― цветки (соцветия) клевера лугового; В ― трава вербены лекарственной; Г ― смесь ЛРС в порошкованном виде; Д ― влажные гранулы; Е ― сухие откалиброванные гранулы; Ж ― таблетки; З ― готовая продукция.
Одной из особенностей представленной схемы является использование на стадии влажного гранулирования полиэкстракта, полученного из входящей в состав фитопрепарата смеси ЛРС методом т.н. «каскадной» экстракции, описанной в работе [33]. Включение полиэкстракта в состав фитопрепарата позволило исключить традиционные для данной лекарственной формы вспомогательные компоненты.
Сушка лекарственного растительного сырья проводится в установке для инфракрасной сушки «Ураган-100Г» (Россия). Перед загрузкой сырья проверяется чистота внутренней поверхности сушилки, загрузочного бункера, конвейерных лент. Загрузку сырья осуществляют через подающий транспортер, который состоит из бункера-накопителя и транспортирующей сетчатой ленты из нержавеющей стали. Сырье попадает на конвейерные ленты, которые движутся одна навстречу другой, и проходит сквозь ряд инфракрасных излучателей. Одновременно происходит подача сухого воздуха внутрь установки и отвод влажного воздуха.
Сушку осуществляют до достижения остаточной влажности не более 5 %, оптимальной для его последующего измельчения и просеивания. Контроль остаточной влажности осуществляется сразу после окончания процесса до выгрузки, которая проводится только после достижения требуемого уровня. Охлаждение сырья происходит конвекцией чистого воздуха, после чего сырье выгружается в емкость и передается на стадию измельчения и просеивания. Исследуется также возможность использования озонированного воздуха на стадии охлаждения с целью снижения микробной обсемененности ЛРС.
Сухое растительное сырье подают на роторно-вихревую мельницу РВМ-22 «Флаттор» (Россия). Измельчение происходит с помощью горизонтального ножа, быстро вращающегося в помольной камере. Степень измельчения зависит от скорости подачи и выгрузки измельчаемого материала. Измельченное сырье собирают в емкости, взвешивают. К емкостям прикрепляют идентификационные этикетки и направляют на стадию «Приготовление массы для таблетирования». На этой стадии расчетное количество измельченного растительного сырья загружают в смеситель-гранулятор марки HLSG-100 (Китай), смешивают до однородности и постепенно, с помощью перистальтического насоса через распылитель подают водно-спиртовой полиэкстракт из смеси равных частей корневищ с корнями диоскореи кавказской, травы вербены лекарственной и цветков клевера лугового, который служит на данной стадии увлажнителем.
Равномерно увлажненная и перемешанная масса должна быть однородной, образовывать комки при сжатии. В таком виде масса подвергается влажному гранулированию.
Гранулирование влажной массы для таблетирования осуществляют в грануляторе с диаметром сит 1–5 мм. В загрузочный бункер влажную массу подают порциями, затем пропущенная сквозь сита масса поступает на стадию сушки.
Сушка гранулята осуществляется в сушилке-грануляторе марки FL-B45 (Китай). Процесс осуществляется до остаточной влажности не более 5 % при температуре подаваемого воздуха не выше 60 °С. Высушенная гранулированная масса переносится в промежуточные емкости и передается на сухое гранулирование, которое заключается в калибровке высушенной гранулированной массы через сита с размером ячеек 2 мм. Откалиброванную массу принимают в сухие чистые емкости, взвешивают, прикрепляют идентификационные этикетки и передают на стадию «Таблетирование».
Для получения таблеток используют пуансоны плоскоцилиндрической формы с фаской диаметром 12 мм. В загрузочные бункеры таблеточной машины РТМ-41 (Украина) порциями загружают таблеточную массу, регулируя глубину заполнения матрицы и устанавливая массу таблетки в пределах 0,650 г.
Регулируя усилие прессования, добиваются необходимой прочности таблеток. Таблетки принимают в сухие чистые емкости, взвешивают, герметично закрывают, прикрепляют идентификационные этикетки и передают на стадию «Фасовка, упаковка, маркировка», одновременно ведут отбраковку таблеток по внешнему виду.
Некондиционные таблетки собирают в емкости, взвешивают, прикрепляют идентификационные этикетки и передают на стадию грануляции в переработку (стадия «Приготовление массы для таблетирования»). Загрязненные таблетки, пыль с таблеточной машины собирают отдельно, взвешивают, прикрепляют идентификационные этикетки и отправляют на утилизацию.
Лекарственная форма представляет собой плоскоцилиндрические таблетки, от светло-зеленого с коричневатым оттенком до зеленовато-коричневого цвета, со слабым характерным запахом; возможны более темные и более светлые вкрапления.
Фасовка таблеток осуществляется с помощью многоканального счетно-фасовочного автомата PAY2000I (Китай) в баночки по 60, 90 или 180 штук. Для завинчивания крышек используют автомат PС2000III (Китай). Нанесение этикеток и маркировку осуществляют на этикетировочном автомате модели PF2000II-C (Китай).
Анализ литературных данных, посвященных применению диоскореи и ее препаратов в народной и официальной медицине, показывает высокую фармакотерапевтическую эффективность стероидных сапонинов, производных диосгенина, в профилактике и лечении атеросклероза и связанных с его развитием заболеваний ― артериальной гипертензии, ишемической болезни сердца, ишемического инсульта, инфаркта миокарда. Влияние комплекса БАВ корневищ с корнями диоскореи на патогенез атеросклероза включает в себя несколько направлений, среди которых основные ― коррекция процесса всасывания холестерина из желудочно-кишечного тракта, препятствие адсорбции липопротеидов и холестерина в сосудистую стенку, прямое воздействие на функции печени, активизация местного кровотока и др.
Опыт практического применения диоскореи кавказской, вербены лекарственной и клевера лугового в терапии заболеваний сердечно-сосудистой системы послужил основанием для создания инновационного препарата ― таблеток «Диосклефит», в состав которых входит нативный комплекс БАВ исследуемых лекарственных растений. В ходе исследований, проведенных специалистами компании «Витаукт», был подобран состав таблеток, отработаны все стадии их промышленного производства, предложены оптимальные способы подготовки растительного сырья, обосновано использование в качестве связующего компонента полиэкстракта, полученного из того же сырья методом «каскадной» экстракции.






