для чего нужен гипохлорит натрия
Применение гипохлорита натрия в водоочистке
Дезинфекция питьевой воды
Технический гипохлорит натрия является наиболее предпочтительным реагентом на стадии предварительного окисления и для стерилизации воды в конце обработки перед подачей ее в распределительную сеть. Он используется также для дезинфекции насосных станций и водонапорных башен, канализации, вспомагательных устройств.
К гипохлориту натрия, применяемому вместо жидкого хлора для дезинфекции питьевой воды, предъявляются определенные требования, касающиеся концентрации щелочи и тяжелых металлов, например железа, стабильности, цветности.
Обычно в систему водоочистки гипохлорит натрия вводят после предварительного разбавления. После разбавления в 100 раз гипохлорита натрия, содержащего 12,5% активного хлора и имеющего рН 12-13, происходит понижение рН до 10-11 и концентрации активного хлора до 0,125 (в действительности величина рН имеет более низкое значение).
При использовании вместо газообразного хлора гипохлорита натрия в процессе ввода этого реактива в систему трубопроводов для его разбавления там образуется осадок, состоящий из гидроксида магния и диоксида кремния, забивающий водные каналы.Поэтому концентрация щелочи в гипохлорите натрия должна быть такой, чтобы не вызывать образования осадка. Для обработки питьевой воды применяется гипохлорит натрия характеризующийся следующими показателями:
Проведенные в Японии исследования показали, что при использовании гипохлорита натрия для дезинфекции воды необходимо учитывать концентрацию щелочи в гипохлорите и поддерживать ее ниже определенного уровня. Концентрация остаточной щелочи в момент окончания реакции хлорирования влияет на концентрацию растворенных в готовом продукте ионов тяжелых металлов, поэтому следует по мере возможности снижать остаточную концентрацию щелочи.
Данные по избытку активного хлора, необходимому для полной стерилизации питьевой воды, при различных температурах, времени воздействия и величине рН
| Температура воды, С0 | Время воздействия, мин | Требуемый избыток хлора, мг/л | ||
|---|---|---|---|---|
| pН 6 | pН 7 | pН 8 | ||
| 10 | 5 | 0,5 | 0,7 | 1,2 |
| 10 | 0,3 | 0,4 | 0,7 | |
| 30 | 0,1 | 0,12 | 0,20 | |
| 45 | 0,07 | 0,07 | 0,14 | |
| 60 | 0,05 | 0,05 | 0,01 | |
| 20 | 5 | 0,3 | 0,4 | 0,7 |
| 10 | 0,2 | 0,20 | 0,4 | |
| 15 | 0,1 | 0,15 | 0,25 | |
| 30 | 5 | 0,06 | 0,12 | |
| 45 | 0,04 | 0,04 | 0,08 | |
| 60 | 0,03 | 0,03 | 0,06 | |
Наиболее допустимое содержание гипохлорита натрия в воде, по данным ФРГ, составляет 0,3 мг/л активного хлора. Допускается повышение содежания активного хлора в питьевой воде до 0,06 мг/л, если это временно совершенно необходимо для обеззараживания воды (такие же концентрации поддерживаются при обработки воды хлором, гипохлоритом кальция, хлорной известью). После обработки воды в ней должно содержаться не менее 0,1 мг/л свободного хлора.
Для осуществления дезинфекции питьевой воды все шире применяются электрические установки для получения гипохлорита натрия.
Дезинфекция воды плавательных бассейнов и прудов
Обычно для этой цели используются разбавленные растворы гипохлорита натрия. Их умеренная цена, эффективность по отношению к водорослям и бактериям, а также безвредность для человека делают этот продукт наиболее пригодным для обработки воды в бассейнах. Технический гипохлорит натрия позволяет получить чистую прозрачную воду, лишенную водорослей и бактерий. Он обеспечивает полноту дезинфекции воды и осуществляет ее защиту от бактериальных загрязнений.
Как и при дезинфекции питьевой воды, при использовании гипохлорита для дезинфекции воды плавательных бассейнов большое значение придается контролю за содержанием активного хлора. Важное значение имеет также поддержание рН на определенном уровне, обычно 7,4-8,0, а еще лучше 7,0-7,4. Регулирование рН осуществляется с помощью растворов соляной или серной кислоты.
Проведенные в России исследования по дезинфекции воды плавательных бассейнов показали, что эффективное обеззараживание при поддержании остаточного хлора на уровне 0,3-0,5 мг/л. Надежное обеззараживание в течение 30 мин обеспечивают растворы, содержащие 0,1-0,2% гипохлорита натрия. Содержание хлора в зоне дыхания не должно превышать 0,1 мг/м 3 в публичных плавательных бассейнах и 0,03 мг/м 3 в спортивных бассейнах. Замена газообразного хлора гипохлоритом натрия приводит к снижению выделения хлора в воздух и, кроме того, позволяет легче поддерживать остаточное количество активного хлора воде. Несмотря на появление новых более перспективных дезинфицирующих средств, гипохлорит натрия продолжает использоваться для дезинфекции воды плавательных бассейнов.
Обработка бытовых и промышленных сточных вод
Гипохлорит натрия применяется для обработки бытовых и промышленных вод, для разрушения животных и растительных микроорганизмов, устранения запахов (особенно образующихся из серосодержащих веществ), обезвреживания промышленных стоков, например, от цианистых соединений.
Он может быть использован для обработки воды, содержащей аммоний. Процесс осуществляют при температуре выше 70 0 С в щелочной среде с добавлением CaCl2 или СаСО3 для разложения соединений аммиака.
Для очистки от фенолов (содержание 0,42-14,94 мг/л) используют 9% раствор гипохлорита натрия в количестве 0,2-8,6 мг/л. Степень очистки достигает 99,99%. При обработке гипохлоритом воды, содержащей фенолы, происходит образование фенолоксифенолов.
В ходе обработки вод, содержащих гуминовые вещества, последние превращаются в хлороформы, дихлоруксусную кислоту, трихлоруксусную кислоту, хлоральдегиды и некоторые другие вещества, концентрация которых в воде значительно ниже. Известны данные об использовании гипохлорита натрия для удаления ртути из сточных вод.
Использование гипохлорита натрия в пищевой промышленности
В начале восьмидесятых годов институт биологии и ее применения к проблемам питания в Дижоне (Франция) провел изучение дезинфицирующих средств, используемых в пищевой промышленности. Гипохлорит натрия был оценен среди этих продуктов по первому классу как наиболее пригодный для этих целей и наиболее экономичный. Он показал высокую эффективность в отношении почти всех растительных клеток, спор и бактерий. По этой причине гипохлорит натрия находит широкое применение в пищевой промышленности для дезинфекции с целью уничтожения ракообразных и моллюсков; для различных промывок; для борьбы против бактериофагов в сыроваренной промышленности; для дезинфекции резервуаров, загонов для скота.
Гипохлорит натрия относится к числу средств используемых в пивоваренной промышленности. Обычно применяют раствор, содержащий 30-40 мг/л активного хлора. Гипохлорит натрия является отличным антимикробным агентом. В частности в США его применяют для обработки зерна.
Использование гипохлорита натрия в молочной промышленности
Гипохлорит натрия является достаточно эффективным средством, используемым для этой цели. В России применяют для этих целей гипохлорит натрия марки А. Он содержит 170 г/л активного хлора и 40- 60 г/л щелочи. Бактерицидное действие гипохлорита натрия проявляется при 20-25 0 С и экспозиции 3-5 минут.Для снижения корозирующего действия гипохлорита был предложен препарат ГИПОХЛОР. Его получают смешением гипохлорита натрия, каустической соды и метасиликата натрия. Коррозирующее действие этого препарата на металлические поверхности в 10-15 раз меньше, чем обычного гипохлорита натрия. В молочной промышленности традиционные средства дезинфекции начинают вытесняться новыми препаратами, обладающими одновременно и моющими и дезинфицирующими свойствами.
Наиболее перспективными из них являются натриевая и калиевая соли трихлоризоциануровой кислоты.
Использование гипохлорита в рыбоводстве
Гипохлорит натрия в виде разбавленных растворов уничтожает все виды патогенных агентов и используется для дезинфекции водоемов с твердым дном и берегами. Кроме того он используется при дезинфекции рыболовных сетей, сачков и баков из пластика для хранения рыбы.
Использование гипохлорита в здравоохранении
В комплексе профилактических мероприятий, направленных на ограничение больничных инфекции, важную роль играет дезинфекция. Для этой цели может быть использован гипохлорит натрия. В частности, в ПНР для этих целей используют гипохлорит натрия производства Тарновского азотного предприятия, с содержанием активного хлора не менее 55. Гипохлорит натрия оказывает дезинфицирующее действие на грамм-положительные и грамм-отрицательные бактерии, туберкулезные палочки, споры бактерий, болезнетворные грибки и вирусы. Имеются сведения (Россия) использования растворов гипохлорита натрия (0,03-0,05%) для лечения гнойных абцессов, гнойных гайморитов, розовых угрей и трофических язв как наружное средство и средство для инъекций.
Другие области применения
Гипохлорит входит в составы синтетических моющих средств, используемых в бытовой химии, в составы дезинфицирующей пасты с отбеливающим эффектом, дезинфицирующих средств с окислительными, хлорирующими и бактерицидными свойствами.
В настоящее время за рубежом и в России наметилась тенденция развития использования гипохлорита натрия для дезинфекции небольших объемов воды с применением электролитического метода его получения. Этот метод находит все большую популярность во всем мире.
Хотя гипохлорит натрия продолжает использоваться в пищевой, молочной промышленности, но он все более вытесняется другими видами средств, обладающими сочетанием моющих и дезинфицирующих свойств. Все чаще его вводят в составы таких средств.
Для чего нужен гипохлорит натрия
1. ОБЩИЕ СВЕДЕНИЯ
2. ОПИСАНИЕ И ОСНОВНЫЕ ХАРАКТЕРИСТИКИ
| Температура, °С | — 10 | 0 | 10 | 25 | 30 |
| Растворимость, % | 20,6 | 22,8 | 27,5 | 45,0 | 50,0 |
Плотность водных растворов гипохлорита натрия
| Концентрация, % | 1 | 2 | 4 | 6 | 8 | 10 | 14 |
| Плотность, г/л | 1005,3 | 1012,1 | 1025,8 | 1039,7 | 1053,8 | 1068,1 | 1097,7 |
| Концентрация, % | 18 | 22 | 26 | 30 | 34 | 38 | 40 |
| Плотность, г/л | 1128,8 | 1161,4 | 1195,3 | 1230,7 | 1268,0 | 1308,5 | 1328,5 |
Температура замерзания водных растворов гипохлорита натрия
| Концентрация | 0,8 % | 2 % | 4 % | 6 % | 8 % | 10 % | 12 % | 15,6 % |
| Температура замерзания, °C | − 1,0 | − 2,2 | − 4,4 | − 7,5 | − 10,0 | − 13,9 | − 19,4 | − 29,7 |
Термодинамические характеристики гипохлорита натрия в бесконечно разбавленном водном растворе:
Водные растворы ГПХН весьма неустойчивы и со временем разлагаются даже при обычной температуре (со скоростью 0,08 до 0,1 % в сутки). На скорость распада ГПХН влияет воздействие солнечного излучения, наличие катионов тяжелых металлов и хлоридов щелочных металлов. При этом наличие в водном растворе сульфата магния или кальция, борной кислоты, силикатов и пр. замедляют процесс разложения ГПХН. Следует заметить, что наиболее устойчивы растворы с сильнощелочной средой (значение pH > 10).
У гипохлорита натрия известно три кристаллогидрата:
2.1 Химические свойства ГПХН
Диссоциация, гидролиз и разложение ГПХН в водных растворах
Гипохлорит натрия (ГПХН) – неустойчивое соединение, легко разлагающееся с выделением кислорода. Самопроизвольное разложение медленно происходит даже при комнатной температуре: например, за 40 суток наиболее устойчивая форма – пентагидрат ГПХН (NaOCl·5H2O) теряет около 30 % активного хлора:
2 NaOCl → 2 NaCl + O2
При нагревании ГПХН параллельно с его разложением происходит реакция диспропорционирования:
3 NaOCl → NaClО3 + 2NaCl
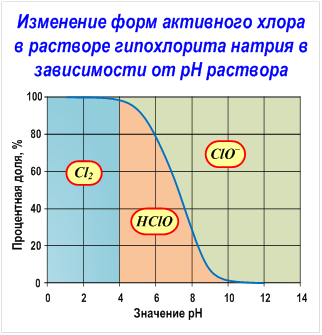
Гипохлорит натрия образует в воде хлорноватистую кислоту и гипохлорит ион в соотношениях, определяемых рН раствора, а именно соотношение между ионом гипохлорита и хлорноватистой кислотой определяется протеканием реакций гидролиза гипохлорита натрия и диссоциации хлорноватистой кислоты (см. Рис. Изменение форм активного хлора в растворе гипохлорита натрия в зависимости от рН раствора).
Растворяясь в воде, ГПХН диссоциирует на катионы натрия и анионы хлорноватистой кислоты:
NaOCl → Na + + OCl −
Так как хлорноватистая кислота (HOCl) является очень слабой, гипохлорит-ион в водной среде подвергается гидролизу:
OCl − + Н2О ↔ НОСl + ОН −
Так как же происходит разложение ГПХН?
В сильнощелочной среде (pH > 10), когда гидролиз гипохлорит-иона подавлен, разложение происходит следующим образом:
2 OCl − → 2 Cl − + O2
При температурах выше 35°C распад сопровождается реакцией диспропорционирования:
OCl − → ClO3 − + 2 Cl −
В среде со значением рН от 5 до 10, когда концентрация хлорноватистой кислоты в растворе заметно выше, разложение протекает по следующей схеме:
HOCl + 2 ClO − → ClO3 − + 2 Cl − + H +
HOCl + ClO − → O2 + 2 Cl − + H +
При дальнейшем уменьшении рН, когда в растворе уже нет ClO − ионов, разложение идет следующим путем:
3 HClO → ClO3 − + 2 Cl − + 3 H +
2 HClO → O2 + 2 Cl − + 2 H +
В конце концов, когда рН раствора ниже 3, разложение будет сопровождаться выделением молекулярного хлора:
NaOCl + 2HCl → NaCl + Cl2 + H2O.
Окислительные свойства ГПХН
Водный раствор гипохлорита натрия, являющийся сильным окислителем, вступает в многочисленные реакции с разнообразными восстановителями, независимо от кислотно-щелочного характера среды.
Основные варианты развития окислительно-восстановительного процесса в водной среде мы уже рассмотрели:
в кислой среде:
NaOCl + H + → Na + + HOCl
2 HOCl + 2 H + + 2e − → Cl2↑ + 2 H2O
HOCl + H + + 2e − → Cl − + H2O
в нейтральной и щелочной среде:
NaOCl → Na + + OCl −
2 OCl − + 2H2O + 2e − → Cl2↑ + 4OH −
OCl − + H2O + 2e − → Cl − + 2 OH −
Ниже приведены основные окислительно-восстановительные реакции с участием гипохлорита натрия.
Так в слабокислой среде иодиды щелочных металлов окисляются до йода:
NaClO + 2 NaI + H2O → NaCl + I2 + 2 NaOH, (1)
в нейтральной среде до иодата:
3 NaClO + NaI → 3 NaCl + NaIO3,
в щелочной среде до периодата:
4 NaClO + NaI → 4 NaCl + NaIO4
Надо упомянуть, что на реакции (1) основан принцип колориметрического определения хлора в воде.
Под воздействием гипохлорита натрия сульфиты окисляются до сульфатов:
нитриты до нитратов:
оксалаты и формиаты до карбонатов:
NaClO + NaOH + CHOONa → NaCl + Na2CO3 + H2O
и т.д.
Фосфор и мышьяк растворяются в щелочном растворе гипохлорита натрия, образуя соли фосфорной и мышьяковой кислот.
Аммиак под действием гипохлорита натрия через стадию образования хлорамина, превращается в гидразин (аналогично реагирует и мочевина). Мы уже рассматривали этот процесс в своей статье «Хлорирование питьевой воды», поэтому здесь приведем только суммарные химические реакции этого взаимодействия:
Приведенные окислительно-восстановительные реакции очень важны, т.к. влияют на потребление активного хлора и переход его в связанное состояние при хлорировании воды. Расчет дозы потребления активного хлора при использовании в качестве хлорагента аналогичен тому, что мы приводили в статье «Хлорирование питьевой воды».
2.2. Бактерицидные свойства ГПХН
Наличие хлорноватистой кислоты в водных растворах гипохлорита натрия объясняет его сильные дезинфицирующие и отбеливающие свойства.
Гипохлорит натрия (NaOCl) на сегодняшний момент одно из лучших известных средств, проявляющих благодаря гипохлорит-аниону сильную антибактериальную активность. Это средство убивает микроорганизмы очень быстро и при достаточно низких концентрациях, поскольку разложение гипохлорита сопровождается образованием ряда активных частиц (радикалов) и, в частности, синглетного кислорода, обладающего высоким биоцидным действием. (подробнее см. в статье «Хлорирование питьевой воды». Образующиеся при распаде ГПХН частицы (радикалы) способствуют в уничтожении микроорганизмов (способных к окислению), разрушая окружающую их биопленку, что приводит к «гибели» микроорганизмов.
Примечание: Исследованиями установлено, описанный выше процесс аналогичен тому, что происходит естественным образом во всех высших организмах. Так, некоторые клетки человека (нейтрофилы, гепатоциты и др.) синтезируют хлорноватистую кислоту и сопутствующие ей высокоактивные радикалы для борьбы с микроорганизмами и чужеродными субстанциями.
Наивысшая бактерицидная активность гипохлорита натрия проявляется в нейтральной среде, когда концентрации HClO и гипохлорит-анионов ClO − в процессе гидролиза и диссоциации ГПХН приблизительно равны.
Что касается бактерицидных свойств ГПХН, то можно привести несколько примеров:
Количественная оценка эффективности химических бактерицидов и их квалификация приведена в Таблице 2.2.
Спектральная активность дезинфицирующих средств по отношению к определенным видам микроорганизмов приведена в Таблице 2.3.
Высокие окислительные свойства гипохлорита натрия позволяют его успешно использовать для обезвреживания различных токсинов (см. Таблицу 2.4).
2.3. Коррозионная активность ГПХН
Гипохлорит натрия оказывает довольно сильное коррозионное воздействие на различные материалы. Это обусловлено его высокими окислительными свойствами, которые были рассмотрены нами ранее. Поэтому при подборе конструкционных материалов для изготовления установок очистки воды это необходимо учитывать. В таблице, которая приводится ниже, представлены данные по скорости коррозии некоторых материалов при воздействии на них растворов гипохлорита натрия различной концентрации и при различной температуре. Более подробную информацию по коррозионной устойчивости различных материалов по отношению к растворам ГПХН можно найти в Таблице химической совместимости (в формате rar-архива), размещенной на нашем сайте.
Не менее важно учитывать и то обстоятельство, что фильтрующие загрузки, которые используются для скорых насыпных фильтров, могут изменять свои фильтрующие свойства при воздействии на них ГПХН, точнее активного хлора, например, при подборе фильтрующей среды для процесса каталитического обезжелезивания – катализаторов обезжелезивания.
Не следует забывать, что активный хлор оказывает негативное влияние на мембранные процессы, в частности он вызывает деструкцию мембран обратного осмоса (об этом мы рассказывали в нашей статье «Обратный осмос. Теория и практика применения.»), а при высоком содержании (более 1 мг/л) отрицательно влияет на процессы ионного обмена.
Что касается материалов, из которых следует изготавливать собственно систему дозирования ГПХН, то здесь надо ориентироваться на концентрации активного хлора в рабочих растворах ГПХН, которые, естественно, существенно выше концентраций в обрабатываемой воде. Об этом мы поговорим немного позже.
Скорость коррозии некоторых материалов при воздействии на них растворов ГПХН
И вот в этих «адских» для ГПХН условиях от него нужно добиться максимальной отдачи.
Как это делается на практике? Вообще все начинается еще на этапе проектирования бассейна. При размещении оборудования циркуляционной петли бассейна стараются сделать так, чтобы от точки внесения в воду дезинфектанта до поступления воды в бассейн между ними был бы максимальный временной контакт. Поэтому точкой введения дезинфектанта обычно является напорный трубопровод циркуляционного насоса, т.е. максимально удаленная точка от возвратных форсунок. Там же устанавливается датчик измерения рН, а корректирующий состав вводится на всасывающем патрубке циркуляционного насоса, который служит в этом случае своеобразным узлом смешения. Подогреватель воды в бассейне размещают как можно ближе к возвратным форсункам, чтобы, во-первых, сократить потери тепла, а во-вторых, раньше времени не начинать деструкцию ГПХН.
Ну а теперь опишем алгоритм выполнения операций при эксплуатации бассейна:
Как мы убедились, процесс дезинфекции воды в бассейне достаточно сложен и включает в себя несколько стадий. Поэтому для полной автоматизации этого процесса и исключения из него «человеческого» фактора были разработаны системы дозирования, состоящие из одного, двух или даже трех насосов-дозаторов, контроллеров, датчиков, электрохимических ячеек и т.д. Их описание можно найти на этой страничке.
Дозирование гипохлорита марки «Э» мало чем отличается от дозирования стабилизированных препаратов на основе гипохлорита натрия марки «А». Разве что появляется необходимость отслеживания общего солесодержания воды в бассейне, поскольку гипохлорит марки «Э», содержит поваренную соль (см. описание процесса получения). Поэтому при его дозировании эта соль поступает в обрабатываемую воду и повышает общее солесодержание (с учетом того, что система рециркуляции замкнута, а общий приток свежей воды составляет всего лишь 10% от объема).
3.2. Обработка бытовых и промышленных сточных вод
Очистка сточных вод заключается в их обезвреживании и обеззараживании.
Обеззараживание сточных вод может производиться несколькими методами: хлорированием, озонированием и УФ-излучением.
Обеззараживание (хлором, гипохлоритом натрия, или прямым электролизом) бытовых сточных вод и их смесей с производственными стоками производится после их очистки. При раздельной механической очистке бытовых и производственных вод, но совместной их биологической очистке, допускается (СНиП 2.04.03-85) предусматривать обеззараживание только бытовых вод после их механической очистки с дехлорированием их перед подачей на биологическую очистку. Вопрос об отводе сточных вод, после обеззараживания должен решаться в каждом конкретном случае по согласованию с территориальными учреждениями Госсанэпидслужбы в соответствии требованиями СанПиН 2.1.2.12-33-2005 «Гигиенические требования к охране поверхностных вод».
Перед обеззараживанием сточные воды осветляют, освобождая их от взвешенных частиц (механическая очистка), а затем уже осветленные воды окисляют биологическим путем (биологическая очистка). Биологическая очистка осуществляется двумя методами: 1) интенсивным (искусственная очистка) и 2) экстенсивным (естественная очистка).
Интенсивный метод позволяет очищать сточную жидкость на специальных очистных сооружениях, располагающихся на небольшой территории, но требует затрат электроэнергии, строительства очистных сооружений, квалифицированного персонала для управления ими и хлорирования. К сооружениям интенсивной очистки относятся аэротенки и биоокислители (биологические фильтры, перколяторы).
Экстенсивный метод требует большей территории, но менее дорогой в строительстве и эксплуатации и дает сток, свободный от яиц гельминтов и патогенных бактерий. Хлорирование в этом случае не требуется. К сооружениям экстенсивной очистки относятся биологические пруды, поля орошения и поля фильтрации.
Хлорирование сточных вод.
Хлорирование применяется для обработки бытовых и промышленных вод, для разрушения животных и растительных микроорганизмов, устранения запахов (особенно образующихся из серосодержащих веществ), обезвреживания промышленных стоков, например, от цианистых соединений.
Сточные воды характеризуются высокой степенью органической нагрузки. Эмпирически установленные значения обеззараживающих концентраций активного хлора в сточных водах могут достигать 15 мг/л. Поэтому необходимые дозы активного хлора и продолжительность контакта его со сточной водой определяют пробным хлорированием. Для предварительных расчетов обеззараживания сточных вод принимают следующие дозы активного хлора: после механической очистки – 10 мг/л; после полной искусственной биологической очистки – 3 мг/л, после неполной – 5 мг/л.
Производительность установки для хлорирования рассчитывают на принятую дозу активного хлора с коэффициентом 1,5. Продолжительность контакта хлора с обеззараживаемой водой зависит от формы соединений хлора. Для свободного активного хлора продолжительность контакта составляет 0,5 ч, для связанного активного хлора – 1 ч. Остаточный хлор после контакта со сточной водой должен включать: свободный активный хлор – 1 мг/л, связанный активный хлор – 1,5 мг/л.
Доза активного хлора должна превышать удельную величину хлорпоглощения воды таким образом, чтобы возникающая при этом концентрация активного хлора в воде обеспечивала требуемый технологический эффект (уровень обеззараживания, степень осветления и т.д.). При расчете дозы активного хлора для обработки загрязненной воды должна учитываться величина ее хлорпоглощения, определяемая в соответствии с требованиями стандарта ASTM D 1291-89.
При необходимости борьбы с энтеровирусами предусматривают двойное хлорирование: первичное хлорирование после полной биологической очистки и вторичное — после дополнительного фильтрования или отстаивания воды. Дозы активного хлора для первичного хлорирования при борьбе с энтеровирусами принимают 3 – 4 мг/л при контакте продолжительностью 30 мин, вторичного 1,5 – 2 мг/л при контакте 1,5 – 2 ч.
Хлорирование может быть использовано для обработки воды, содержащей аммоний. Процесс осуществляют при температуре выше 70 о С в щелочной среде с добавлением CaCl2 или СаСО3 для разложения соединений аммиака.
В ходе обработки вод, содержащих гуминовые вещества, последние превращаются в хлороформы, дихлоруксусную кислоту, трихлоруксусную кислоту, хлоральдегиды и некоторые другие вещества, концентрация которых в воде значительно ниже.
Для очистки от фенолов (содержание 0,42-14,94 мг/л) используют 9% раствор гипохлорита натрия в количестве 0,2-8,6 мг/л. Степень очистки достигает 99,99%. При хлорировании воды, содержащей фенолы, происходит образование фенолоксифенолов.
Известны данные об использовании гипохлорита натрия для удаления ртути из сточных вод.
Хлорирование сточных вод жидким хлором при помощи хлораторов имеет более широкое применение по сравнению с процессом, где используется ГПХН. Жидкий хлор вводят в сточную воду либо непосредственно (прямое хлорирование), либо при помощи хлоратора. Подробнее об этих процессах мы расскажем при рассмотрении процесса дезинфекции (хлорировании) питьевой воды.
При использовании в качестве хлорагента гипохлорита натрия ввод рабочего раствора ГПХН в обрабатываемую воду осуществляют методом пропорционального дозирования с помощью насосов-дозаторов .
Гигиенические требования к организации и контролю за обеззараживанием сточных вод установлены в методических указаниях МУ 2.1.5.800-99.
3.3. Использование гипохлорита натрия в пищевой промышленности
Помимо своих специфических критериев и соответствующего случаю применения дезинфектанта необходимой эффективности и селективности, химические дезинфицирующие средства в пищевой промышленности выбираются исходя из того, как будут они применяться «открытым» или «закрытым» способом.
При дезинфекции в закрытой системе (метод CIP) в результате использования широко распространенного на сегодняшний день автоматического пропорционального дозирования, а также автоматического управления процессом мойки и дезинфекции, как правило, не происходит прямой контакт между обслуживающим персоналом и химическим продуктом (за исключением момента приготовления рабочего раствора). Поэтому в этом случае нет прямой потенциальной опасности для обслуживающего персонала в отношении опасных и агрессивных сред, какими являются дезинфектанты и их растворы.
При открытом способе дезинфекции, где необходим ручной метод обработки, наблюдается обратная ситуация. Здесь обслуживающий персонал с одной стороны должен следить за тем, чтобы избежать прямого контакта с химическим продуктом, используя средства индивидуальной защиты, а с другой стороны по возможности использовать максимальные дезинфицирующие возможности продукта.
В пищевой промышленности применяются, как правило, не чистые активные дезинфицирующие вещества, а их разбавленные растворы, которые помимо активных веществ содержат некоторое количество вспомогательных средств. Этими веществами могут быть: поверхностно-активные вещества для улучшения смачивания подлежащих дезинфекции поверхностей; комплексообразователи для снижения жесткости воды; эмульгаторы и диспергаторы для равномерного распределения реагента по обрабатываемой поверхности и т.д.
Кроме того, поскольку любой дезинфектант «активно работает» в определенном диапазоне значений рН, то в зависимости от основного вещества (дезинфектанта) готовые к применению дезинфицирующие растворы или их концентраты должны иметь кислую, нейтральную или щелочную среду. Несколько примеров: как мы убедились, гипохлорит натрия и хлорсодержащие соединения проявляют наибольшую активность только в щелочной среде, а надуксусная кислота более эффективна в кислой среде. Четвертичные аммонийные соединения в кислой среде рН резко теряют свои дезинфицирующие свойства, а альдегиды можно использовать и в кислой, и нейтральной средах и т.д.
Дезинфекция с помощью хлорагентов достаточно распространена в пищевой промышленности. В данной публикации мы остановимся только на дезинфицирующих хлорсодержащих препаратах, которые имеют в своем составе гипохлорит натрия.
В самом начале необходимо отметить, что, как правило, все дезинфицирующие средства на основе ГПХН, применяемые в пищевой промышленности, помимо своего основного назначения – разрушения бактерий и вирусов, грибов и плесени, удаляют масла, жиры, белки, остатки крови, пятна чая, кофе, фруктов и т.д., поскольку обладают отбеливающими свойствами. Все дезинфицирующие средства на основе ГПХН поставляются в концентрированном виде, а рабочий раствор готовится на месте путем разбавления концентрата. Как правило, все средства щелочные (значение рН рабочего раствора колеблется в пределах от 11 до 13). Связано это с химическими свойствами ГПХН, которые мы рассматривали ранее. Содержание активного хлора в рабочем растворе колеблется от 60 до 240 мг/л. В таблице приведены некоторые из наиболее популярных дезинфицирующих и моющих средств на основе ГПХН.
| Торговая марка | Состав | Изготовитель | |||||||||
| ГПХН (Ср.р.) | Щелочь (рН) | С | П | О | Ф | А | И | СЖ | К | ||
| SR 3000 D | + 2% | + рН=12 | + | + | HWR-Chemie GmbH, Германия | ||||||
| DM CID | + 2% | + рН=12 | + | + | + | ||||||
| DM CID S | + 2% | + рН=12 | + | + | + | + | |||||
| Катрил-хлор | + 2% | + рН=12 | + | + | ЗАО «Экохиммаш», Россия | ||||||
| Катрил-хлор пенный | + 2% | + рН=12 | + | + | + | ||||||
| Neomoscan® RD-B | + 1% | + рН=12 | + | Chemische Fabrik DR. WEIGERT GmbH & Co. KG, Германия | |||||||
| Divosan Hypochlolite | + 1% | + рН=11 | + | + | + | JohnsonDiversey, Великобритания | |||||
| Калгонит ЦФ 312 | + 1% | + рН=12 | + | Calvatis GmbH, Германия | |||||||
| Калгонит ЦФ 353 | + 2,4% | + рН=12 | + | + | + | ||||||
| Калгонит ЦФ 315 | + 1% | + рН=12 | + | + | |||||||
| Калгонит 6010 | + 4% | + рН>12 | + | ||||||||
| СИП-БЛЮ 5 | + 3% | + рН=11 | + | + | «НПО СпецСинтез», Россия | ||||||
| АКТИВ – ЛЮКС Д | + 2% | + рН=11,5 | + | ||||||||
Принятые в таблице обозначения: С – силикаты; П – поверхностно-активные вещества, О – отдушки; Ф – фосфаты; А – альдегиды; И – ингибиторы коррозии; СЖ – стабилизаторы жесткости; К – комплексообразователи.
Нам хорошо известно, что решающим фактором при приобретении какого-либо пищевого продукта являются его вкусовые характеристики. Поэтому технологи пищевой промышленности неохотно используют средства дезинфекции с хлорсодержащими агентами, поскольку активный хлор уж очень «активно влияет» на вкус и запах продукции. Исключение составляет наружная дезинфекция технологического оборудования, ввиду того, что хлор обладает замечательным пролонгирующим действием. Гипохлорит натрия относится к числу таких средств. Обычно для дезинфекции технологического оборудования применяют раствор ГПХН, содержащий 30-40 мг/л активного хлора. Бактерицидное действие гипохлорита натрия проявляется после нанесения раствора при 20-25оС и его экспозиции в течение 3-5 минут. Правда, в этом случае надо учитывать коррозионную активность растворов ГПХН, поэтому для снижения коррозирующего действия используют смесь гипохлорита натрия, каустической соды и метасиликата натрия (препарат «Гипохлор»). Коррозионная активность этого препарата в 10-15 раз меньше, чем обычного гипохлорита натрия.
Что касается обработки внутренних полостей технологического оборудования пищевой промышленности, то ГПХН активно вытесняется препаратами, не содержащими хлор.
3.4. Использование гипохлорита в рыбоводстве
Рыбоводные пруды, орудия лова, живорыбная тара, рыбоводный инвентарь, а также спецодежда и обувь лиц, участвующих в проведении рыбоводных и ветеринарно-санитарных мероприятий, подлежат периодической очистке и дезинфекции (дезинвазии). Чаще всего для этого используется хлорная известь. Однако в последнее время для этой цели стали использовать гипохлорит натрия в виде разбавленных растворов.
Достаточно активно ГПХН используется при дезинфекции рыболовных сетей, сачков и баков из пластика для хранения рыбы.
При использовании растворов ГПХН в рыбоводстве следует выполнять пересчет концентрации активного хлора, получающейся при использовании растворов хлорной извести и растворов ГПХН. При этом руководствуются: «Ветеринарно-санитарными правилами для рыбоводных хозяйств» и «Инструкцией по ветеринарному надзору за перевозками живой рыбы, оплодотворенной икры, раков и других гидробионтов».
3.5. Использование гипохлорита в здравоохранении
3.6. Использование ГПХН для отбеливания белья в фабриках-прачечных
Считается, что отбеливание белья при промышленной стирке – самая потенциально опасная операция из всех операций, применяемых в стирке белья, а отбеливатель, соответственно, – самое опасное вещество для ткани. Большинство отбеливателей, применяемых при промышленной стирке, являются сильными окислителями, под воздействием которых большинство окрашенных веществ после их окисления становятся или бесцветными, или растворимыми в воде. И как любой окислитель, отбеливатель одновременно «атакует» как пятна, так и волокна ткани. Поэтому всегда при отбеливании побочным процессом будет разрушение волокна ткани. Отбеливатели, применяемые при промышленной стирке, бывают трех типов: пероксидные (перекисные или кислородосодержащие), хлорные и серосодержащие. В рамках данной публикации мы остановимся только на одном из хлорсодержащих отбеливателей тканей – гипохлорите натрия.
Отбеливание тканей с помощью ГПХН имеет более чем двухсотлетнюю историю. Историческое название раствора гипохлорита натрия, применяемого для отбеливания, – лабарракова вода или жавелевая вода. Как это не покажется странным, но за два столетия в технологии отбеливания тканей с помощью растворов ГПХН практически ничего не изменилось. Гипохлорит натрия широко используется в качестве отбеливателя и пятновыводителя в текстильном производстве и промышленных прачечных и химчистках. Он может быть безопасно использован для многих видов тканей, включая хлопок, полиэстер, нейлон, ацетат, лён, вискозу и другие. Он очень эффективен для удаления следов почвы и широкого спектра пятен в том числе, кровь, кофе, трава, горчица, красное вино и т. д.
Отбеливающие свойства гипохлорита натрия основаны на образовании ряда активных частиц (радикалов) и, в частности, синглетного кислорода, обладающего высоким биоцидным и окислительным действием (подробнее см. в статье «Хлорирование питьевой воды»), образующегося при разложении гипохлорита:
NaOCl → NaCl + [O].
Поэтому без гипохлорита натрия не обойтись при отбелке больничного белья или белья, пораженного плесенью.
Отбеливающие (окислительные) свойства растворов гипохлорита натрия зависят от его концентрации, рН раствора, температуры и времени воздействия. И хотя мы их уже рассматривали в разделе 2 настоящей публикации, немного повторимся применительно к процессу отбеливания.
В общем, чем выше концентрация ГПНХ в растворе (больше активность ГПХН) и дольше время воздействия, тем выше эффект отбеливания. А вот зависимость активности воздействия от температуры имеет более сложный характер. Он прекрасно «работает» уже при низких температурах (
40°С). При повышении температуры (вплоть до 60°С) активность отбеливателя на основе ГПНХ растет линейно, а при более высокой температуре наблюдается экспоненциальная зависимость роста активности отбеливателя.
Зависимость отбеливающих свойств ГПХН от значения рН напрямую связана с химическими свойствами ГПХН.При высоком значении рН среды (рН>10) активность отбеливателя на основе ГПНХ относительно невелика, т.к. в процессе отбеливания в основном участвует активный кислород – он действует довольно медленно. Если значение рН среды начать уменьшать, то активность отбеливателя вначале увеличивается, достигая максимума при оптимальном значении рН=7 для гипохлорита, а затем ростом кислотности активность снова снижается, но медленнее, чем это наблюдается при росте рН в щелочную сторону.
В промышленной стирке операцию отбеливания обычно совмещают с операциями стирки и полоскания, а не проводят ее отдельно. Это удобнее и быстрее. При этом длительность самих операций увеличивают, чтобы отбеливатель успел бы обработать все вещи закладки равномерно. При этом также следят, чтобы отбеливатель на основе ГПХН не был слишком активным, поскольку при его слишком активной реакции он будет израсходован до того, как сможет проникнуть в центр закладки, что повлияет на процесс выведения пятенв центре закладки,а волокна тканей, находящихся на поверхности закладки,получат дополнительные повреждения.
Британской Ассоциацией «Стирка и Чистка» (British Launderers Research Association, BLRA) были разработаны рекомендации по применению гипохлорита натрия при выведении пятен и отбеливании тканей в процессе промышленной стирки. Приведем некоторые из них:
Как утверждают специалисты BLRA, если следовать этим рекомендациям, то в процессе отбеливания при использовании ГПХН удаляется большинство обычных пятен, а ткань получает минимальные повреждения.
3.7. Дезинфекция питьевой воды
Дозу хлора устанавливают технологическим анализом из расчета, чтобы в 1 л воды, поступающей к потребителю, оставалось 0,3…0,5 мг хлора, не вступившего в реакцию (остаточного хлора), который является показателем достаточности принятой дозы хлора. За расчетную следует принимать ту дозу хлора, которая обеспечивает указанное количество остаточного хлора. Расчетная доза назначается в результате пробного хлорирования. Для осветленной речной воды доза хлора обычно колеблется в пределах 1,5 – 3 мг/л; при хлорировании подземных вод доза хлора чаще всего не превышает 1– 1,5 мг/л; в отдельных случаях может потребоваться увеличение дозы хлора из-за наличия в воде закисного железа. При повышенном содержании в воде гуминовых веществ требуемая доза хлора возрастает.
После введения хлорагента в обрабатываемую воду должны быть обеспечены хорошее смешивание его с водой и достаточная продолжительность (не менее 30 мин) его контакта с водой до подачи ее потребителю. Контакт может происходить в резервуаре фильтрованной воды или в трубопроводе подачи воды потребителю, если последний имеет достаточную длину без водозабора. При выключении на промывку или ремонт одного из резервуаров фильтрованной воды, когда не обеспечивается время контакта воды с хлором, доза хлора должна быть увеличена вдвое.
Хлорирование уже осветленной воды обычно производят перед поступлением ее в резервуар чистой воды, где и обеспечивается необходимое для их контакта время.
Вместо хлорирования воды после отстойников и фильтров в практике водоочистки иногда применяют хлорирование ее перед поступлением на отстойники (предварительное хлорирование) – до смесителя, а иногда перед подачей на фильтр.
Предварительное хлорирование способствует коагуляции, окисляя органические вещества, которые тормозят этот процесс, и, следовательно, позволяет уменьшить дозу коагулянта, а также обеспечивает хорошее санитарное состояние самих очистных сооружений. Предварительное хлорирование требует повышения доз хлора, так как значительная часть его идет на окисление органических веществ, содержащихся в еще неосветленной воде.
Вводя хлор до и после очистных сооружений, можно снизить общий расход хлора по сравнению с расходом его при предварительном хлорировании, сохранив преимущества, даваемые последним. Такой метод носит название двойного хлорирования.
Обеззараживание хлором.
Коротко мы уже рассматривали вопрос об аппаратурном оформлении процесса хлорирования воды с использованием жидкого хлора в качестве хлорагента. В данной публикации мы остановимся на тех аспектах, которые нами не были отражены.
Обеззараживание воды жидким хлором имеет пока более широкое применение по сравнению с процессом, где используется ГПХН. Жидкий хлор вводят в обрабатываемую воду либо непосредственно (прямое хлорирование), либо при помощи хлоратора – устройства, которое служит для приготовления раствора хлора (хлорной воды) в водопроводной воде и его дозировании.
Для дезинфекции воды чаще всего применяют хлораторы непрерывного действия, лучшими из них считаются вакуумные, в которых дозируемый газ находится под разрежением. Это предотвращает проникание газа в помещение, что возможно при напорных хлораторах. Вакуумные хлораторы выпускаются двух типов: с жидкостным измерителем расхода хлора и газовым измерителем расхода хлора.
В случае использования прямого хлорирования должно быть обеспечено быстрое распределение хлора в обрабатываемой воде. Для этой цели служит диффузор приспособление, при помощи которого хлор вводится в воду. Слой воды над диффузором должен быть около 1,5 м, но не меньше 1,2 м.
Для смешивания хлора с обрабатываемой водой могут быть применены смесители любого типа, устанавливаемые перед контактными резервуарами. Наиболее простым является ершовый смеситель. Он представляет собой лоток с пятью вертикальными перегородками, поставленными перпендикулярно или под углом 45° против течения воды. Перегородки суживают сечение и вызывают вихреобразное движение, при котором хлорная вода хорошо смешивается с обрабатываемой. Скорость движения воды через суженное сечение смесителя должна быть не менее 0,8 м/сек. Дно лотка смесителя устраивается с уклоном, равным гидравлическому уклону.
Далее смесь обрабатываемой воды и хлорной воды направляется в контактные емкости.
Итак, налицо основные преимущества применения хлора для хлорирования воды:
Не оставляет сомнения, что оборудование, необходимое для дозирования столь смертоносного реагента (об этом почти регулярно свидетельствует статистика) должно обладать целым рядом степеней безопасности.
Поэтому, ПБХ («Правила безопасности при производстве, хранении, транспортировании и применении хлора») предполагают следующее обязательное периферийное оборудование:
а при потреблении газообразного хлора из баллонов более 2 кг/час или более 7 кг/час при потреблении хлора из контейнера – испарители хлора, к которым предъявляются особые требования. Они должны быть оснащены автоматическими системами, предотвращающими:
Испаритель должен быть снабжен специальным отсекающим электромагнитным вентилем на входе, манометром и термометром.
Весь процесс обработки воды хлором осуществляется в специальных помещениях – хлораторных, которым также предъявляются особые требования. Хлораторная обычно состоит из блоков помещений: расходного склада хлора, хлордозаторной, вентиляционной камеры, вспомогательных и бытовых помещений.
Хлораторные должны размещаться в отдельно стоящих капитальных зданиях второй степени огнестойкости. Вокруг склада хлора и хлораторной со складом хлора должно быть сплошное глухое ограждение, высотой не менее двух метров, с глухими плотно закрывающимися воротами для ограничения распространения газовой волны и исключения доступа посторонних лиц на территорию склада. Вместимость расходного склада хлора должна быть минимальной и не превышать 15-суточного потребления водопроводной станцией.
Радиус опасной зоны, в пределах которой не допускается располагать объекты жилищного и культурно-бытового назначения, составляет для складов хлора в баллонах 150 м, в контейнерах – 500 м.
Хлораторные должны располагаться в пониженных местах площадки водопроводных сооружений и преимущественно с подветренной стороны преобладающих направлений ветров относительно ближайших населенных пунктов (кварталов).
Расходный склад хлора следует отделять от других помещений глухой стеной без проемов, в складе должно быть два выхода с противоположных сторон помещения. Один из выходов оборудован воротами для транспортирования баллонов или контейнеров. Въезд автомобилей в помещение склада не допускается, должно быть предусмотрено грузоподъемное оборудование для транспорта сосудов с кузова автомобиля на склад. Порожнюю тару надлежит хранить в помещении склада. Двери и ворота во всех помещениях хлораторной должны открываться по ходу эвакуации. На выходах из склада предусматриваются стационарные водяные завесы. Сосуды с хлором должны размещаться на подставках или рамках, иметь свободный доступ для строповки и захвата при транспортировании. В помещении склада хлора располагается оборудование для нейтрализации аварийных выбросов хлора. Должна быть обеспечена возможность подогрева баллонов на складе перед доставкой их в хлораторную. Следует отметить, что при длительной эксплуатации баллонов с хлором в них накапливается чрезвычайно взрывчатый трихлорид азота, и поэтому время от времени баллоны с хлором должны проходить плановую промывку и очистку от хлорида азота.
Хлордозаторные размещать в заглубленных помещениях не допускается, от других помещений они должны быть отделены глухой стеной без проемов и снабжены двумя выходами наружу, при этом один из них через тамбур. Вспомогательные помещения хлораторных должны быть изолированы от помещений, связанных с применением хлора и иметь самостоятельный выход.
Хлораторные оборудуются приточно-вытяжной вентиляцией. Выброс воздуха постоянно действующей вентиляцией из помещения хлордозаторной надлежит осуществлять через трубу высотой на 2 м выше конька кровли самого высокого здания, находящегося в радиусе 15 м, а постоянно действующей и аварийной вентиляцией из расходного склада хлора – через трубу высотой 15 м от уровня земли.
То есть степень опасности хлора минимизируется наличием целого комплекса мер по организации его хранения и использования, в том числе за счет организации санитарно-защитных зон (СЗЗ) складов реагента, радиус которых достигает 1000 м для наиболее крупных сооружений.
Однако по мере роста городов, жилая застройка вплотную приближалась к границам СЗЗ, а в ряде случаев размещалась внутри этих границ. Кроме того увеличилась опасность транспортировки реагента от места производства к месту потребления. Согласно статистическим данным, именно при транспортировке происходит до 70% различных аварий химически опасных веществ. Полномасштабная авария железнодорожной цистерны с хлором способна нанести урон различной степени тяжести не только населению, но и природной среде. В то же время токсичность хлора, усиленная высокой концентрацией реагента, снижает промышленную безопасность и антитеррористическую устойчивость систем водоснабжения в целом.
В последние годы нормативная база в области промышленной безопасности при обращении с хлором ужесточается, что отвечает требованиям дня. В связи с этим у эксплуатирующих служб возникает желание перейти к более безопасному способу обеззараживания воды, т.е. к способу, который не поднадзорен Федеральной службе по экологическому, технологическому и атомному надзору, но обеспечивает выполнение требований СанПиНа по безопасности в эпидемиологическом отношении питьевой воды. С этой целью в качестве хлорсодержащего реагента, наиболее часто используемого при хлорировании (второе место после жидкого хлора), выступает гипохлорит натрия (ГПХН).
Обеззараживание гипохлоритом натрия
В практике водоснабжения для обеззараживания питьевой воды используются концентрированный гипохлорит натрия марки А с содержанием активной части 190 г/л и низкоконцентрированный гипохлорит натрия марки Э с содержанием активной части около 6 г/л.
Обычно в систему водоочистки товарный гипохлорит натрия вводят после предварительного разбавления. После разбавления в 100 раз гипохлорита натрия, содержащего 12,5% активного хлора и имеющего рН = 12-13, происходит понижение рН до 10-11 и концентрации активного хлора до 0,125 (в действительности величина рН имеет более низкое значение). Чаще всего для обработки питьевой воды применяется раствор гипохлорита натрия, характеризующийся показателями, перечисленными в Таблице:
| Содержание активного хлора, % | 5 |
| Содержание свободной щелочи, % | 2 |
| Нерастворимая часть, % | 0,01 |
| Mg, мг/л | 1 |
| As, мг/л | 1 |
| Pb, мг/л | 1 |
| Температура воды, о С | Время воздействия, мин | Требуемый избыток хлора, мг/л | ||
| pН 6 | рН 7 | рН 8 | ||
| 10 | 5 | 0,50 | 0,70 | 1,20 |
| 10 | 0,30 | 0,40 | 0,70 | |
| 30 | 0,10 | 0,12 | 0.20 | |
| 45 | 0,07 | 0,07 | 0.14 | |
| 60 | 0,05 | 0,05 | 0,10 | |
| 20 | 5 | 0,30 | 0,40 | 0,70 |
| 10 | 0,20 | 0.20 | 0,40 | |
| 15 | 0,10 | 0,15 | 0,25 | |
| 30 | 005 | 0,06 | 0,12 | |
| 45 | 0,04 | 0,04 | 0,08 | |
| 60 | 0,03 | 0,03 | 0,06 | |
Потерю активности растворов ГПХН со временем наглядно иллюстрирует следующая таблица:
| Концентрация NaOCl, % | Период полураспада, сутки | |
| 25 °C | 35 °C | |
| 15 | 144 | 39 |
| 12 | 180 | 48 |
| 9 | 240 | 65 |
| 6 | 360 | 97 |
| 3 | 720 | 194 |
| 1 | 2160 | 580 |
Ввод рабочего раствора ГПХН в обрабатываемую воду осуществляют методом пропорционального дозирования с помощью насосов-дозаторов. При этом пропорциональное дозирование ( управление насосом-дозатором ) может производиться как с использованием импульсных счетчиков воды, так и по сигналу датчика хлора, установленного либо непосредственно в трубопроводе, либо после контактной емкости. После узла ввода ГПХН или на входе в контактную емкость обычно устанавливают динамический смеситель для тщательного перемешивания обрабатываемой воды с рабочим раствором ГПХН.
Гипохлорит натрия электролизный марки «Э», полученный на бездиафрагменных электролизерах, подается в поток обрабатываемой воды либо посредством прямого ввода (в случает применения электролизеров проточного типа), либо через накопительную емкость (в случае применения электролизеров непроточного типа), оборудованную автоматической или управляемой вручную системой дозирования. Управление системой дозирования может производиться как с использованием импульсных счетчиков воды, так и по сигналу датчика хлора, установленного либо непосредственно в трубопроводе, либо после контактной емкости.
Таким образом, казалось бы, преимущества применения гипохлорита натрия перед хлором при хлорировании воды, достаточно явные: он значительно безопаснее – не горюч и не взрывоопасен; нет необходимости в дополнительном оборудовании, обеспечивающего безопасность процесса хлорирования, кроме наличия: 6-кратной вентиляции, резервуара для сбора вытекшего гипохлорита натрия и емкости с нейтрализующим раствором (тиосульфат натрия). Применяемое при использовании ГПХН оборудование для обеспечения процесса обеззараживания на станциях водоподготовки не относится к категории промышленно опасного и не поднадзорно Федеральной службе по экологическому, технологическому и атомному надзору. Это облегчает жизнь эксплуатационникам.
Но так ли это? Давайте вернемся к свойствам ГПХН.
3.8. Обеззараживание ГПХН оборудования для очистки воды
При обеспечении населения питьевой водой безупречно чистой в микробиологическом отношении не только сама вода должна быть очищена от патогенных бактерий, вирусов и паразитов, но и оборудование, используемое для водоснабжения: трубопроводы, емкости (резервуары), арматура, фильтры и насосы, которые используются при обработке воды и находятся в непосредственном контакте с ней.
Уже на стадии проектирования при выборе строительных и конструкционных материалов (арматура, трубы, уплотняющие материалы, краска и т.д.) нужно обращать внимание на свойства этих материалов, и ориентироваться на те, которые способствуют предотвращению или сокращению роста микробиологических загрязнений. В то же время эти материалы должны быть устойчивыми к методам и реагентам, используемым для обеззараживания воды.
На стадии строительства и монтажа систем водоснабжения должны соблюдаться меры предосторожности, препятствующие проникновению микроорганизмов монтируемую систему из воздуха, от персонала, с рабочих инструментов и т.д. Во время монтажа оборудования и строительных работ в системе водоснабжения необходимо вести профилактические работы с целью предотвращения возможного микробиологического заражения частей системы.
Обеззараживание всего оборудования необходимо проводить перед началом его эксплуатации, после каждого ремонта всего оборудования или его отдельных узлов или после длительных перерывов в эксплуатации. Во всех этих случаях необходимо провести обеззараживание оборудования, чтобы предотвратить угрозу загрязнения питьевой воды патогенными микроорганизмами после ввода системы очистки воды в эксплуатацию.
Методы обеззараживания (дезинфекции) систем питьевого водоснабжения выбираются исходя из местных условий, однако в любом случае должны включать в себя определенные стадии. Чаще всего для обеззараживания оборудования всей системы водоснабжения используются любые средства, обладающие пролонгирующим действием. Само собой разумеется, это требование исключает использование озона и ультрафиолетового излучения.
Коротко рассмотрим алгоритм проведения дезинфекции отдельных технологических элементов, которые, как правило, включаются в состав технологической цепочки систем очистки воды.
Так для резервуаров с питьевой водой должны быть включены следующие стадии очистки и дезинфекции: