дмпп сердца у новорожденных что это комаровский
Дефект предсердной перегородки (Q21.1)
Версия: Справочник заболеваний MedElement
Общая информация
Краткое описание
ДМПП составляют неоднородную группу аномалий эмбрионального развития межпредсердной перегородки. Они различаются:
— по расположению дефекта: центральный, верхний, нижний, задний, передний;
— по размеру дефекта: от небольшого щелевидного отверстия (например, при незаращении овального отверстия), до полного отсутствия межпредсердной перегородки (единое предсердие);
— по количеству дефектов: от 1-2 до множественных.
Автоматизация клиники: быстро и недорого!
— Подключено 300 клиник из 4 стран
Автоматизация клиники: быстро и недорого!
Мне интересно! Свяжитесь со мной
Классификация
1. Первичный ДМПП (частичный дефект атриовентрикулярной перегородки, частичный атриовентрикулярный канал). Составляет около 15% от всех ДМПП. Локализуется в месте соединения всех четырех камер сердца. При этом атриовентрикулярные клапаны, как правило, деформированы, что осложняется регургитацией крови различной степени тяжести.
2. Вторичный ДМПП. Составляет 80% от всех ДМПП. Локализуется в области овальной ямки или рядом с ней.
3. Дефект синуса верхней полой вены. Составляет 5% от всех ДМПП. Локализуется в области впадения верхней полой вены. Сочетается с частичным или полным соединением между правыми легочными венами и верхней полой веной или правым предсердием.
4. Дефект синуса нижней полой вены. Составляет менее 1% от всех ДМПП. Локализуется в области впадения нижней полой вены.
5. Локализованный ДМПП у коронарного синуса (дефект крыши коронарного синуса). Составляет менее 1% от всех ДМПП. Характеризуется частичным либо полным отсутствием отделения от левого предсердия.
ДМПП часто сочетается с другими пороками:
— аномальное соединение легочных вен;
— персистирующая левая верхняя полая вена;
— стеноз клапанов легочного ствола;
— пролапс митрального клапана;
— вторичный ДМПП может сочетаться с патологией верхней конечности (синдром «рука-сердце», синдром Холта-Орама): наблюдается деформация верхней конечности.
Этиология и патогенез
По эмбриологическому происхождению
1. Первичный ДМПП. Возникает вследствие незаращения первичного сообщения между предсердиями. Располагается в нижнем отделе межпредсердной перегородки непосредственно над отверстиями. Нижним краем дефекта является перегородка между ними. В изолированном виде порок встречается крайне редко.
Эпидемиология
Дефект межпредсердной перегородки (ДМПП) встречается в 3-20% случаев от всех врожденных сердечных пороков.
Факторы и группы риска
Факторы риска, влияющие на формирование врожденных пороков сердца у плода
Семейные факторы риска:
— наличие детей с врожденными пороками сердца (ВПС);
— наличие ВПС у отца или ближайших родственников;
— наследственные заболевания в семье.
Клиническая картина
Клинические критерии диагностики
Cимптомы, течение
Клинически дефект межпредсердной перегородки (ДМПП) относится к гемодинамически длительно компенсированным и маломанифестным порокам. Выраженность его симптоматики зависит от величины и локализации дефекта, а также от длительности существования порока и развития вторичных осложнений.
В связи с частичным «обкрадыванием» большого круга кровообращения и недостаточным притоком крови на периферию, к 5-7 годам жизни дети чаще выглядят бледными, субтильными, умеренно равномерно отставая в росте, массе тела и физическом развитии. Предположительно это обуславливает склонность таких детей к головокружениям, обморокам, а также характерные жалобы на быструю утомляемость и одышку при физической нагрузке.
В некоторых случаях быстрая утомляемость и одышка, неадекватные нагрузке, являются единственными жалобами на фоне отсутствия или неопределенности какой-либо другой симптоматики.
Появляющиеся позже жалобы на колотье в сердце, перебои, сердцебиение и чувство замирания связаны с перегрузкой правых отделов сердца на фоне неадекватно низкого коронарного кровотока.
При небольшой величине дефекта (до 10-15 мм) дети развиваются нормально, удовлетворительно переносят нагрузки. Первые симптомы порока могут появляться у них в возрасте старше 10 лет.
Аускультация
I тон чаще усилен. II тон, как правило, усилен и расщеплен над легочной артерией.
Диагностика
4. МРТ и КТ сердца являются альтернативными методами исследования, если при эхокардиограмме не было получено достаточно данных. В частности, при оценке перегрузки объемом правого желудочка и состояния легочных венозных анастомозов.
Дифференциальный диагноз
Дифференциальную диагностику дефекта межпредсердной перегородки с большим сбросом следует проводить:
1. С врожденными пороками сердца, протекающими с обогащением малого круга кровообращения (дефект межжелудочковой перегородки, открытый артериальный проток, аномальный дренаж легочных вен, атриовентрикулярная коммуникация).
2. С умеренным изолированным стенозом легочной артерии.
При малых вторичных дефектах межпредсердной перегородки необходимо проводить дифференциальную диагностику с функциональной кардиопатией и нейроциркуляторной дистонией.
Осложнения
Лечение
Хирургическая коррекция
Показания к проведению коррекции дефекта межпредсердной перегородки (ДМПП):
1. Пациентам со значительным сбросом крови (есть признаки перегрузки правого желудочка объемом) и легочным сосудистым сопротивлением 1,5) следует рассматривать как кандидатов на закрытие дефекта (класс рекомендаций: IIb, уровень доказательности: C).
При ранней хирургической коррекции дефекта и при отсутствии легочной артериальной гипертензии отмечается низкий уровень смертности (менее 1 % больных без серьезных сопутствующих заболеваниях) и хороший отдаленный прогноз (нормальная продолжительность жизни и низкий уровень заболеваемости в отдаленном будущем).
Летальный исход наблюдается чаще среди пожилых пациентов и пациентов с сопутствующими заболеваниями.
Прогноз
Естественное течение дефекта межпредсердной перегородки (ДМПП) и прогноз определяются размером дефекта и величиной артериовенозного сброса.
Дети с вторичными ДМПП и малым сбросом крови развиваются нормально, не предъявляют жалоб, многие годы у них сохраняется физическая работоспособность, а первые симптомы неблагополучия иногда выявляются лишь в третьем десятилетии жизни. Однако в дальнейшем заболевание быстро прогрессирует, и большая часть пациентов умирает в возрасте до 40 лет, оставшаяся часть больных к 50 годам становятся инвалидами.
Описаны случаи, когда больные с вторичным ДМПП доживали до 70-80 лет. У некоторых пациентов с небольшим дефектом происходит спонтанное закрытие дефекта в течение первых 2- 5 лет жизни.
Младенческая смертность в основном обусловлена первичным ДМПП и (или) наличием ДМПП, дефектов атриовентрикулярных клапанов, а также сочетанием ДМПП с другими экстракардиальными врожденными аномалиями. Непосредственными причинами смерти чаще всего являются тяжелые вирусные инфекции, рецидивирующие пневмонии, кишечные инфекции.
Профилактика
Профилактика возникновения врожденных пороков сердца (ВПС) очень сложна и в большинстве случаев сводится к медико-генетическому консультированию и разъяснительной работе среди людей, относящихся к группе повышенного риска заболевания. К примеру, в случае, когда 3 человека, состоящие в прямом родстве, имеют ВПС, вероятность появления следующего случая составляет 65-100% и беременность не рекомендуется. Нежелателен брак между двумя людьми с ВПС. Помимо этого необходимо тщательное наблюдение и исследование женщин, имевших контакт с вирусом краснухи или имеющих сопутствующую патологию, которая может привести к развитию ВПС.
Профилактика неблагоприятного развития ВПС:
— своевременное выявление порока;
— обеспечение надлежащего ухода за ребенком с ВПС;
— определение оптимального метода коррекции порока (чаще всего, это хирургическая коррекция).
Обеспечение необходимого ухода является важной составляющей в лечении ВПС и профилактике неблагоприятного развития, так как около половины случаев смерти детей до 1-го года во многом обуславливаются недостаточно адекватным и грамотным уходом за больным ребенком.
Специальное лечение ВПС, (в том числе, кардиохирургическое) должно проводиться в наиболее оптимальные сроки, а не немедленно по выявлению порока, и не в самые ранние сроки. Исключение составляют только критические случаи угрозы жизни ребенка. Оптимальные сроки зависят от естественного развития соответствующего порока и от возможностей кардиохирургического отделения.
«Любая женщина может родить ребенка с пороком сердца». Кардиохирург об актуальности проблемы
Каждый день в Беларуси рождаются по трое детей с пороками сердца. О том, почему так происходит, что делать будущей матери для профилактики и почему операция не панацея, — в интервью с кардиохирургом Виталием Дедовичем.
На тысячу новорожденных — восемь с пороком сердца
— Есть общемировая статистика, которая привязана к показателям младенческой рождаемости: на 1 тысячу новорожденных приходится 8 с пороком сердца. Получается, что если в 2016 году в Беларуси появились на свет 117,8 тысячи малышей (данные Белстат), около тысячи из них — с пороком сердца. Но это не значит, что всем этим детям необходимо оказывать экстренную медицинскую помощь.
Операция не панацея
Врач объясняет, различают критический (сложный) и простой порок сердца. Разница заключается в том, что при критическом врожденном пороке сердца без срочной операции ребенок может умереть сразу после рождения.
— У нас в Беларуси эти вопросы отрегулированы: женщина в первом триместре беременности проходит УЗИ, и если врач заподозрит что-то неладное, ее отправляют на повторное обследование. Таким образом, есть возможность выявить и отследить внутриутробное развитие порока.
Если это порок, который сразу после рождения станет критическим, то, как правило, на третьем триместре беременности женщину направляют в стационар.
— Другая часть детей — те, кто должен быть прооперирован в первый месяц жизни. Это, как правило, тоже сложный порок сердца, который может привести к летальному исходу и неоперабельности, но позже. В данном случае сначала делают инициирующую операцию, на первом году жизни — вторую, а на втором — третью. Таких пациентов в два раза больше, чем с критическим пороком сердца.
Все остальные малыши рождаются с простым пороком сердца. За ними наблюдают и оценивают их состояние в течение первого года жизни. Бывает, что ребенок родился с пороком сердца, но в данный момент это никак ему не мешает. Таких детей около 30%.
Люди до старости не знают, что у них порок сердца
— Оставшиеся 40% пациентов — те, кто рождается и не знает, что у них есть порок сердца. Удивительно, но у нас до сих пор встречаются такие случаи. Например, недавно к нам в центр попала женщина, которая только в 68 лет узнала о своем заболевании. Такие люди рожают детей и даже занимаются спортом. Это говорит о том, что порок сердца есть с точки зрения анатомии, но с точки зрения гемодинамики он незначим.
Как появляется врожденный порок
— Если хрестоматийно, то врожденные пороки сердца формируются под воздействием химических, физических, биологических и прочих факторов. Ко мне в кабинет часто приходили мамы с вопросом: «Почему это случилось?». Я перечислял эти факторы, но понимал, что ни один из них не подходит.
Любая женщина может родить ребенка с пороком сердца с вероятностью до 10-12% в зависимости от возраста беременной. Ученые подсчитали, вероятность рождения второго ребенка с пороком сердца у пары, у которой уже есть ребенок с такой проблемой, примерно такая же, как и у остальных пар. Эта вероятность возрастает до 12-14% в случае, если порок сердца есть у самой мамы.
Лечить порок сердца — это уже риск
— Все пороки сердца можно исправить хирургически с разной степенью риска. У половины деток после операции все будет хорошо, и они никогда об этом не вспомнят. Другая половина — пациенты, которые нуждаются в многоэтапных операциях. При успешном их исходе малыши будут жить, взрослеть и вести активный образ жизни, но не смогут заниматься спортом.
При лечении любого порока сердца — сложного или простого — есть определенный риск. Мировое сообщество по этому критерию разделяет все пороки на шесть групп, которые отражают риск и тяжесть хирургической коррекции.
Один из самых сложных пороков — это гипоплазия левых отделов сердца. Мы всегда объясняем родителям своих пациентов, что даже при идеально выполненной операции ребенок может умереть. В некоторых странах мира с этим заболеванием связывают такой термин, как «пассивная эвтаназия»: ребенка с гипоплазией не лечат. Для него обеспечивают комфортное пребывание, обезболивание и питание. В таком случае малыш умирает вскоре после рождения. Достаточно трудно судить, насколько это гуманно.
Факторы, которые влияют на проблемы с сердцем
— Главная причина — инфекции. Вирусные, микробные, грибковые или аутоимунные. А вот другие причины, вроде воздействия радиации или вредных химических продуктов, влияния не оказывают.
Статистика говорит о том, что если человек курит или злоупотребляет алкоголем, у него возрастает риск возникновения ишемической болезни сердца. Но если речь идет о детях, то к ним неприменимы причины, которые влияют на приобретенный порок сердца у взрослых.
Можно ли защитить ребенка от порока сердца?
— Вакцины от кардиологического заболевания не существует, защититься никак нельзя. Это подтверждает один факт: 100 лет тому назад показатель этого заболевания среди новорожденных был таким же, как и сегодня.
Сердце и сосуды можно укрепить еще до планирования беременности
— Улучшить состояние сердечно-сосудистой системы поможет бег на низких пульсах (оздоровительный). Благодаря регулярным тренировкам организм станет выносливее, сможет легче воспринимать физические нагрузки.
Доктор рассказывает, что сам начал бегать около года назад. Поначалу приходилось себя заставлять. Выходишь из операционной, кажется, что самый уставший человек в мире. Постепенно стал входить во вкус, читать специальную литературу. Стал более выносливым в операционной.
— Со временем вместе со мной начала бегать жена, студенты и коллеги по работе. Недавно участвовал в благотворительной инициативе компании velcom «Забег тысячи сердец», участники которой с помощью бега собирали средства в помощь детям с сердечно-сосудистыми заболеваниями. Решил поучаствовать в ней и пробежал 22 км — это мой небольшой вклад в общую сумму, которая составила 90 тысяч белорусских рублей.
Как определяют проблему еще в утробе матери
Когда на первом триместре беременности всем женщинам делают УЗИ, скрининг позволяет выявить грубые врожденные пороки развития. Если есть подозрение на порок сердца у ребенка, об этом сразу же сообщают врачу из женской консультации. Такой женщине медики всегда уделяют особое внимание, и до родов она наблюдается по индивидуальной программе. Если возникают малейшие проблемы или недомогание, ее сразу же кладут на сохранение. Мониторинг осуществляется на каждом из этапов развития плода. У нас в стране этот механизм досконально отработан.
— Как возникает приобретенный порок?
— Врожденный порок сердца — болезнь, которая сформировалась внутриутробно и была обнаружена сразу после рождения ребенка. Приобретенный порок, как правило, формируется с течением времени под влиянием каких-то внешних факторов. Пациенты с приобретенным пороком сердца занимают около 5% от общего числа детей с этим заболеванием.
Что делать женщине, которой сказали, что у будущего малыша уже есть порок сердца?
— Беременной необходимо, прежде всего, определиться с желанием: хочет она этого ребенка или нет. Не нужно искать виноватых, корить себя или родственников. Женщина и плод представляют собой мир, в который никого, кроме мамы и папы, лучше не пускать. Сохраняйте равновесие и помните, что беременная женщина самая красивая и самая счастливая. Нужно следить за собой так, как будто ничего не произошло, потому что от вашего состояния зависит вес и внутриутробное развитие ребенка. Всем я посоветую внимательно слушать и исполнять рекомендации врачей. Это общий, но очень важный совет.
Тактика педиатра при критических врожденных пороках сердца у новорожденных детей
В структуре младенческой смертности аномалии развития занимают третье место, и половину случаев летальности определяют врожденные пороки сердца (ВПС).

Масштаб проблемы подчеркивает высокая частота ВПС: в разных странах этот показатель варьирует от 0,6% до 2,4% в год у детей, родившихся живыми, с учетом внутриутробной гибели плода и ранних выкидышей общая частота ВПС составляет 7,3% [1, 3].
Пренатальная диагностика. С целью снижения младенческой смертности используется пренатальный ультразвуковой скрининг, позволяющий выявить большинство ВПС до 24-й недели гестации. При подозрении на порок проводится прицельное УЗИ плода на аппарате экспертного класса. Основная задача — предотвратить рождение детей с неоперабельными пороками — синдромом гипоплазии левого сердца (СГЛС), гипертрофической кардиомиопатией с признаками органического поражения миокарда, множественными пороками развития плода. Пренатальный консилиум должен предложить прерывание беременности только при условии точной диагностики некурабельного порока [2, 4].
Учитывая высокую летальность новорожденных детей и младенцев от ВПС, для данной возрастной группы пациентов создана классификация, основанная на определении ведущего клинического синдрома, эффективности терапевтической тактики и определяющая сроки хирургического вмешательства [3, 4].
Синдромальная классификация ВПС у новорожденных и детей первого года жизни (Шарыкин А. С., 2005)
Данные состояния могут сочетаться, усугубляя тяжесть состояния детей, 50% этих детей требуют хирургического или терапевтического вмешательства на первом году жизни.
Гемодинамика. Критические пороки характеризуются дуктус-зависимым легочным или системным кровообращением, их объединяет внезапное резкое ухудшение внешне благополучного при рождении ребенка, связанное с уменьшением кровотока через артериальный проток. Дуктус-зависимое легочное кровообращение при ТМС, атрезии (или критическом стенозе легочной артерии) с интактной МЖП обеспечивает кровоток через проток в малый круг кровообращения, и при его ограничении или прекращении развивается тяжелая артериальная гипоксемия, острая гипоксия органов и тканей.
Клиника ВПС с легочным дуктус-зависимым кровообращением
Анатомия одного из самых частых критических пороков — транспозиции магистральных сосудов — заключается в неправильном отхождении аорты — из правого и легочной артерии — из левого желудочка, что способствует разобщению кругов кровообращения: в системе малого круга циркулирует артериальная кровь, в системе большого круга — венозная.
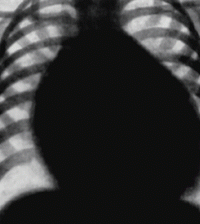
Естественное течение порока очень тяжелое. Ребенок рождается в срок с нормальной массой тела, но в первые часы после рождения появляется диффузный цианоз кожи, особенно выраженный на периферии — цианоз лица, кистей, стоп. Состояние крайней степени тяжести обусловлено тяжелой артериальной гипоксемией. Одышка, тахикардия появляются через 1–2 часа после пережатия пуповины. Отмечается прогрессирующее ухудшение состояния. Ребенок вялый, заторможенный, легко охлаждается.
При закрытии фетальных коммуникаций острая гипоксия приводит к развитию полиорганной недостаточности и гибели новорожденного в течение нескольких часов. При выживании ребенка в течение нескольких недель нарастает сердечная недостаточность. Быстро развивается тяжелая гипотрофия. Необходимо отметить, что в случае адекватной тактики наблюдения и лечения, а также своевременной — до месяца — хирургической коррекции порока у ребенка (так как только в этот период возможна радикальная коррекция методом артериального переключения магистральных сосудов) полностью восстанавливается физиологическая гемодинамика, темпы роста и развития, физическая и в последующем социальная адаптация. Если коррекция порока проводится позже — исходы менее благоприятны.
Диагностические критерии ТМС включают:
Схема обследования новорожденного ребенка с подозрением на ВПС:
Кроме того, наблюдение ребенка предполагает мониторинг газов крови (рО2, рСО2), сатурации кислорода (SatO2) с помощью пульсоксиметрии и метаболических показателей — рН, ВЕ. Газообмен в легких не нарушен, если РаО2 находится в пределах 60–80 мм рт. ст., SаО2 — 96–98%. Артериальная гипоксемия развивается при РаО2 менее 60 мм рт. ст. и уровне насыщения гемоглобина 85–75%.
Задачи педиатра (неонатолога):
Транспортировка в кардиохирургический центр оптимальна в течение первых недель, первого месяца жизни. Предварительно необходимо сообщить в кардиохирургический стационар о больном с врожденным пороком сердца с дуктус-зависимым кровообращением. Период наблюдения до момента перевода и транспортировка в центр проводится на фоне инфузии препарата простагландина Е (Алпростан, Вазапростан).
Клиника ВПС с системным дуктус-зависимым кровообращением (группа пороков включает СГЛС, выраженную коарктацию аорты, перерыв дуги аорты). Наиболее позитивным примером пороков данной группы является выраженная предуктальная коарктация, занимающая от 1% до 10% среди критических ВПС. При данном пороке резко ограничен или полностью отсутствует кровоток из проксимальной ее части (ниже места отхождения артериального протока) к дистальной. Нарушение гемодинамики, соответственно, заключается в том, что в нисходящую аорту (в большой круг) небольшой объем крови поступает только из легочной артерии через артериальный проток. При закрывающемся артериальном протоке остро развивается гипоперфузия органов и тканей и полиорганная недостаточность. Клиника: доношенный новорожденный с резким ухудшением в первые несколько дней жизни — адинамия, холодные конечности, симптом гипоперфузии периферических тканей («белого пятна»), пульс малого наполнения, высокое АД на руках и низкое или не определяется на ногах, одышка, тахикардия, олигоурия с нарастающей азотемией, гепатомегалия с ростом трансаминаз, некротизирующий энтероколит.
Рассмотрим диагностику и оптимальную терапевтическую тактику в отношении пациента с выраженной коарктацией аорты на конкретном клиническом примере.
Из анамнеза: состояние ухудшилось внезапно на 14-е сутки жизни, когда ребенок стал вялым, появилась выраженная одышка, госпитализирован машиной «скорой помощи». Мальчик от второй, нормально протекавшей беременности, срочных родов с массой 3220 г, оценкой по шкале Апгар 5 (9) баллов. Выписан из родильного дома в удовлетворительном состоянии, находился на естественном вскармливании. Периодически отмечались эпизоды беспокойства, метеоризм.
При поступлении ребенок интубирован, проводится ИВЛ с низким содержанием кислорода во вдыхаемой смеси. Обследование в стационаре выявило кардиомегалию (кардиоторакальный индекс — 80%), обеднение легочного рисунка, по данным электрокардиографии — сочетанную перегрузку обоих желудочков. Эхокардиография установила гипоплазию аорты ниже места отхождения левой подключичной артерии (и выше локализации артериального протока), в типичном для артериального протока месте — точечный кровоток (закрывающийся артериальный проток). Через 6 часов состояние ребенка ухудшилось: развилась олигурия, отмечен рост креатинина до 213 ммоль/л, трансаминаз в 4–5 раз от уровня лабораторной нормы. Гуморальная активность не установлена.
Обоснование диагноза и тактики: учитывая клинику выраженной дыхательной и в последующем — полиорганной недостаточности в сочетании с кардиомегалией, системной артериальной гипертензией, почечной и печеночной недостаточностью, по клиническим данным следовало заподозрить коарктацию аорты. Внезапное ухудшение состояния ребенка в отсутствие признаков инфекции позволяет думать о дуктус-зависимом системном кровообращении, с учетом данных визуализации сердца и сосудов имеет место диагноз: «ВПС, предуктальная коарктация аорты, артериальная гипертензия 2 ст., вторичная, полиорганная недостаточность».
С момента подтверждения диагноза по данным ЭхоКГ необходимо начать терапию Вазапростаном 0,02 (с увеличением дозы до 0,05 мкг/кг/мин) с целью восстановления кровотока через артериальный проток. При данном пороке шунт направлен из легочной артерии в нисходящую аорту, и только эта небольшая порция крови обеспечивает весь большой круг кровообращения.
Расчет дозы и методика введения. Вес ребенка при поступлении — 3220 г. В 1 ампуле содержится 20 мкг Вазапростана. В данном случае введение препарата начали с дозы 0,02 мкг/кг/мин, то есть потребовалось 0,02 ´ 3,2 = 0,064 мкг/кг/мин. За час доза препарата составила 0,064 ´ 60 = 3,8 мкг/час. Для введения препарата 1 ампулу (20 мкг Вазапростана) развели в 20 мл физиологического р-ра (в 1 мл — 1 мкг). При отсутствии эффекта в течение двух часов доза была увеличена до 0,04–0,05 мкг/кг/мин: соответственно скорость введения препарата увеличилась до 7,6–9,5 мл/час. В данном случае был очень показателен контроль терапии — через 6 часов инфузии отмечено улучшение состояния, усиление дующего систолического шума во втором межреберье слева, увеличение размеров потока через артериальный проток по данным ЭхоКГ. Переведен на поддерживающую дозу Вазапростана — 0,01 и затем 0,005 мкг/кг/мин, которая сохранялась в течение всего периода наблюдения в педиатрическом стационаре и в ходе транспортировки при переводе в кардиохирургический стационар. В данном клиническом случае полностью отойти от ИВЛ было невозможно (учитывая тяжесть дыхательной недостаточности), на 5-й день госпитализации (19-е сутки жизни) ребенок на фоне терапии переведен в клинику им. Мешалкина, где была успешно проведена коррекция порока — формирование аортолегочного шунта.
В случаях развития сердечной недостаточности у новорожденных при пороках, сопровождающихся массивным сбросом крови в малый круг кровообращения, применяется тот же принцип мониторинга основных показателей и симптоматическая терапия:
При появлении симптомов перегрузки малого круга (аускультативно — усиление, расщепление 2-го тона на легочной артерии, на ЭхоКГ — увеличение давления в легочной артерии более 30 мм рт. ст. после шести суток жизни), а также признаков нарушения диастолической функции сердца рекомендуется применять препараты из группы ингибиторов ангиотензин-превращающего фермента (иАПФ). Используется Капотен (каптоприл) в дозе 0,5–1 мг/кг при условии контроля системного АД. Терапевтическое действие иАПФ связано со снижением периферического сопротивления сосудов и частичным депонированием крови, в результате чего уменьшается объем крови, возвращаемой в правые отделы сердца. Соответственно уменьшается объем шунта и нагрузка на левые камеры и сосуды малого круга. Кроме того, известно, что иАПФ являются ингибитором апоптоза, стимулированного гипоксией, что объясняет ангио- и кардиопротективный эффект препаратов.
Таким образом, тактика педиатра, включающая раннюю диагностику критических ВПС и терапию, управляющую внутрисердечной, центральной и периферической гемодинамикой, а также по возможности ранняя координация действий с кардиохирургическим центром способны существенно улучшить прогноз больных и уменьшить показатели младенческой смертности.
Литература
Е. Ю. Емельянчик*, доктор медицинских наук, профессор
Д. Б. Дробот*, доктор медицинских наук, профессор
Е. П. Кириллова*, кандидат медицинских наук, доцент
В. А. Сакович*, доктор медицинских наук, профессор
Е. В. Басалова**
А. Ю. Черемисина*
*ГОУ ВПО Красноярский ГМУ им. профессора В. Ф. Войно-Ясенецкого,
**Краевая клиническая детская больница, Красноярск




