дроспиренон и дидрогестерон чем отличаются
Средства заместительной гормонотерапии (часть II)
Препараты различают в зависимости от содержания компонентов на эстроген–гестагенные, эстроген–андрогенные, эстроген–антиандрогенные. Эстроген–гестагенные препараты, в свою очередь, подразделяются на монофазные, двухфазные и трехфазные.
Преферанская Нина Германовна
Доцент кафедры фармакологии фармацевтического факультета Первого МГМУ им. И.М. Сеченова, к.фарм.н.
Часть II. Комбинированные гормональные эстрогенные препараты
МОНОФАЗНЫЕ ЭСТРОГЕН–ГЕСТАГЕННЫЕ ПРЕПАРАТЫ
Содержат одинаковое количество эстрогенов и гестагенов во всех таблетках, блистер (28 тб.) рассчитан 28 дней, в остальные дни цикла — перерыв.
К монофазным препаратам относятся:
Фемостон, Фемостон 1/10, Фемостон 1/5 Конти (тб., покр. обол. пленочной) – 1 мг эстрадиол + 5 мг дидрогестерон;
Клиогест, Паузогест — 2 мг эстрадиола гемигидрата + 1 мг норэтистерона ацетата в 1 тб.;
Анжелик — 1 мг эстрадиола гемигидрата + 2 мг дроспиренона в 1 тб.;
Климодиен — 2 мг эстрадиола валерата + 2 мг диеногеста в 1 тб.;
Индивина — 1 мг (2 мг) эстрадиола валерата + 25 мг (5 мг) медроксипрогестерона ацетата в 1 тб.
ДВУХФАЗНЫЕ ЭСТРОГЕН–ГЕСТАГЕННЫЕ ПРЕПАРАТЫ
Содержат разное количество таблеток двух цветов в блистере. В первую фазу таблетки содержат эстроген, а во вторую фазу помимо эстрогена добавлен гестагенный препарат.
К двухфазным эстроген-гестагеным препаратам относят:
Фемостон (блистер 28 тб.) — 1 мг (2 мг) 17β-эстрадиол (14 тб.) + 1 мг (2 мг) 17β-эстрадиол + 10 мг дидрогестерон (14 тб.);
Климонорм (блистер 21 тб.) — 2 мг эстрадиола валерата (9 тб.) + 0,15 мг левоноргестрела (12 тб.);
Дивина (блистер 21 тб.) — 2 мг эстрадиола валерата (11 тб.) + 10 мг медроксипрогестерон ацетат (10 тб.);
Цикло–Прогинова (блистер 21 тб.) — 1 мг (2 мг) эстрадиола валерата (9 тб.) + 1 мг (2 мг) эстрадиола валерата + 0,5 мг норгестрела (12 тб.).
ТРЕХФАЗНЫЕ ЭСТРОГЕН–ГЕСТАГЕННЫЕ ПРЕПАРАТЫ
Рассчитаны на три фазы менструального цикла, поэтому блистер в виде календарного диска или пластины содержит три разных по составу и цвету таблетки, в составе которых меняется количество эстрогена и во вторую серию таблеток добавлен гестаген.
Трисеквенс — 2 мг эстрадиола гемигидрата (12 тб.) + 1 мг норэтистерона ацетат (10 тб.) + 1 мг эстрадиола гемигидрата (6 тб.).
Обращаю внимание! Добавление гестагена в препараты ЗГТ особенно важно, т.к. они предотвращают развитие побочных эффектов, вызванных длительным применением эстрогенов, таких как гиперплазия эндометрия или рак эндометрия. Добавление гестагенного компонента позволяет усилить некоторые эффекты эстрадиола, в частности на сердечно-сосудистую и костную системы организма. От гестагенного компонента зависит переносимость препарата и частота побочных эффектов.
Используемые в настоящее время в ЗГТ гестагены помимо прогестагенного эффекта обладают эстрогенными и андрогенными свойствами – норэтистерона ацетат и тиболон; антиэстрогенными свойствами обладают прогестерон и дидрогестерон; антиандрогенными – медроксипрогестерона ацетат и диеногест.
Гестагены взаимодействуют с прогестероновыми рецепторами и оказывают специфические гестагенные эффекты. Наличие и выраженность того или иного эффекта при применении ЗГТ зависит от входящих в комбинированный препарат компонентов. Наиболее часто в качестве гестагена используют медроксипрогестерона ацетат, который входит в состав препаратов Дивина, Индивина.
Препараты Клиогест, Трисеквенс, Паузогест содержат синтетический гестаген — норэтистерона ацетат, который подобно прогестерону проникает в цитоплазму клетки, связывается с цитозольными рецепторами, образуя комплекс. Далее попадает в ядро и за счет прямого связывания с ядерными прогестиновыми рецепторами вызывает инициацию транскрипции и увеличение белкового синтеза. Служит для снижения повышенной стимуляции и пролиферации эндометрия, возникающих под воздействием эстрогена. При совместном применении с эстрадиолом влияет на липидный обмен, повышая концентрации антиатерогенных липопротеинов и снижая общий холестерин крови и триглицеридов. Применение норэтистерона ацетата обеспечивает предсказуемый контроль кровотечений у большинства женщин. Усиливает защитное действие эстрогенов на костную ткань, что сопровождается достоверным увеличением минерализации костей и ингибированием костной резорбции при его применении.
К препаратам, содержащим аналог природного прогестерона — дидрогестерон, относят Дюфастон и Фемостон, которые эффективны, начиная с ранних симптомов менопаузы. Они хорошо зарекомендовали себя при климактерических расстройствах в период менопаузы. Дюфастон не обладает эстрогенной активностью, его используют у женщин с расстройствами, обусловленными естественной или хирургической менопаузой, и показан во всех случаях недостаточности лютеиновой фазы.
Дроспиренон, входящий в состав противоклимактерического препарата Анжелик, является производным спиронолактона, калий-сберегающего диуретического средства, обладает гестагенным, антиадрогенным, антигонадотропным и антиминералокортикоидным действием. Препарат применяется при преждевременном истощении яичников, при климактерических расстройствах в постменопаузе и в целях профилактики постменопаузного остеопороза.
Диеногест — новый «гибридный» гестаген, входящий в состав препарата Климодиен, оказывает трансформирующее влияние на эндометрий, обладает умеренным антигонадотропным эффектом, антиандрогенной активностью и, что не менее важно, антипролиферативной активностью на раковые клетки молочной железы. Также оказывает минимальное влияние на метаболические процессы, т.к. имеет короткий период полувыведения и в организме не кумулирует.
При пероральном приеме имеет высокую биодоступность, не связывается с транспортными глобулинами крови и циркулирует в крови в виде свободной фракции, что позволяет применять препарат малыми дозами. Антигонадотропный эффект связан с заметным увеличением элиминации с мочой эстрогенов и уменьшением выведения гонадотропинов. Климодиен начинают применять не ранее чем через один год после наступления менопаузы, когда системная терапия вместе с эстрогенами приводит к уменьшению физиологической инволюции кожи при старении, оказывает протективное действие на сердечно-сосудистую систему, понижает уровень общего холестерина в крови, предупреждает потерю костной массы, улучшает настроение.
Климен относят к препаратам, содержащим эстроген–антиандроген (2 мг эстрадиола валерата (11 драже белого цвета) + 2 мг эстрадиола валерата + 1 мг ципротерона ацетата (10 драже розового цвета). Обладая антиандрогенной активностью, некоторые прогестины устраняют юношескую себорею, появление вторичных мужских половых признаков, умеренную вирилизацию (появление на лице волосяного пушка, усов и роста волос на подбородке). Ципротерона ацетат блокирует андрогенновые рецепторы в клетках-мишенях, уменьшает уровень андрогенов в крови, угнетает секрецию гипофизом гонадотропного гормона и тормозит овуляцию. Способствует исчезновению угревой сыпи, уменьшает повышенное салоотделение на волосистой части головы и коже лица, устраняет выпадение волос. Восполняет в организме женщины дефицит половых гормонов; устраняет симптоматику климактерических расстройств, гиперплазии эндометрия, понижает уровень холестерина ЛПНП в сыворотке крови. Его применяют для профилактики постменопаузного остеопороза; при эстрогенной недостаточности (овариоэктомия по поводу незлокачественных новообразований), нарушениях менструального цикла — первичная и вторичная аменорея и др.
Тиболон (в блистере 28 тб.) относится к препаратам, содержащим синтетические эстрогены, выпускается под ТН «Ледибон» и «Ливиал» и используется при климактерическом синдроме. 1 тб. содержит 2,5 мг тиболона. Препарат нивелирует климактерические изменения гипоталамо-гипофизарной системы, подавляет секрецию гонадотропинов ФСГ и ЛГ, а у фертильных женщин ингибирует овуляцию. Восстанавливает слизистую оболочку влагалища, предотвращает потерю костной массы, подавляет менопаузные расстройства, такие как приливы, повышенная потливость, головные боли, положительно влияет на либидо и настроение. Применяется для устранения симптомов менопаузы (естественной и после хирургических операций).
Важно! При применении данного препарата наблюдаются побочные эффекты: головная боль, головокружение, отек голеней, диспептические расстройства, влагалищное кровотечение, изменение показателей функции печени, себорейный дерматоз, усиление роста волос на лице, возможно снижение уровней общего и свободного тироксина и тироксинсвязывающего глобулина. Прием следует прекратить при появлении признаков тромбоэмболии, изменении лабораторных показателей функции печени, развитии холестатической желтухи.
Абсолютными противопоказаниями приема препаратов ЗГТ являются: геморрагический или ишемический инсульт, инфаркт миокарда, сердечная недостаточность, тяжелая форма гипертонии, тромбоэмболия, тромбофлебит, сахарный диабет, хронические заболевания печени и почек, новообразования половых органов и молочных желез (рак шейки и тела матки, миома матки, рак яичников, рак молочной железы), склонность к маточным кровотечениям и др. Курение повышает риск осложнений со стороны сердечно-сосудистой системы и снижает эффективность ЗГТ.
Замена таблеток ЗГТ
На сервисе СпросиВрача доступна консультация гинеколога онлайн по любой волнующей Вас проблеме. Врачи-эксперты оказывают консультации круглосуточно и бесплатно. Задайте свой вопрос и получите ответ сразу же!
2. И какого производителя/страну лучше принимать?
3. препарата Тиблон- нет, есть аналоги, все разные, не понимаю что надо.
У него совсем другие компоненты. Подскажите это организм снова будет перестраиваться?
4. Очень переживаю, что много отрицательныъ последствий в описании:
пишут вес увеличивается
и волосы начинают расти везде.
Очень хочется избежать таких последствий. И хочется оптимальный вариант, чтобы подошел! Буду признательна за уточнения.
И если из Тилона, то какой препарат иметь ввиду?
Валерия, спасибо, пояснили про эстроген)
Светлана, ДД! Спасибо за ответ и совет!
1.Если сравнивать эти уже 6 дней без таблеток то, до приема Микро Анжелик, то все супер, но сейчас появляется немного жар иногда и реакция бывает слезная((
Здравствуйте. А если совсем убрать? как вы сейчас себя чувствуете?
можно попробовать фемостон мини.
Любовь, дд! Спасибо за ответ.
1. Смптомы немного есть, жарко бывает и слезность появляется.
Как это сказывается на нас? От этого идут побочки?
5. У Тиболона- столько расписано последствий, или он хорош при приеме? И совсем другой состав.
Индивидуализация выбора заместительной гормональной терапии с учетом разных типов климактерических расстройств (с преимущественным дефицитом эстрогенов и андрогенов, по смешанному типу)
СЮ.Калинченко, С.С.Апетов
Кафедра эндокринологии ФПКМР ГБОУ ВПО РУДН, Москва
В настоящее время существуют разные классификации климактерического синдрома (по тяжести, времени возникновения и пр.), но по сути ни одна из них не учитывает индивидуальных особенностей течения данной патологии, которая в своих клинических проявлениях бывает весьма вариабельной.
Так, некоторых женщин беспокоят преимущественно приливы жара, повышенное потоотделение, прибавка массы тела и артериальная гипертензия. У других эти жалобы отсутствуют, но они отмечают постоянную необъяснимую слабость, повышенную утомляемость, упадок жизненных сил, психоэмоциональные и сексуальные расстройства, разные нарушения мочеиспускания. У третьих присутствуют и те и другие жалобы.
Почему остеопороз развивается только у 45% женщин в постменопаузе, хотя дефицит эстрогенов есть у 100%? Почему ожирение у 60, приливы у 65%? В доступной медицинской литературе мы не встретили убедительного объяснения такой вариабельной клинической картины у разных женщин.
В то же время в последнее десятилетие ряд зарубежных исследований 5, а также наши собственные наблюдения 10 показали негативное влияние андро-генного дефицита и позитивное влияние его коррекции (или его отсутствия) на течение разных проявлений климактерического синдрома.
Проявления андрогенной недостаточности
К ним относят следующие симптомы (группы симптомов):
Костно-мышечные:
• снижение мышечной массы;
• неадекватный физическим нагрузкам прирост мышечной массы;
• боли в костях, суставах;
• мышечные боли.
Психоэмоцион альные:
• быстрая утомляемость;
• лабильность настроения со склонностью к депрессиям;
• нарушение памяти;
• снижение творческой продуктивности;
• снижение мотивации и самооценки;
• расстройство сна, не связанное с приливами.
Сексуальные:
• снижение либидо;
• возбуждаемости;
• чувствительности эрогенных зон;
• возможности достижения оргазма.
Кожные:
• сухость кожи;
• выпадение волос на лобке;
• гипотония мимических мышц (появление носогубного треугольника, опускание углов рта)
Типы климактерических расстройств
Согласно нашим наблюдениям и проведенным исследованиям можно выделить 3 клинических типа климактерических расстройств у женщин в период пери-менопаузы:
Сравнительная характеристика симптомов в зависимости от типа течения перименопаузы представлена в табл. 1.
Таблица 1. Клинические симптомы и типы течения климактерических расстройств
Клинический признак
Приливы жара, потливость
Проблемы со
сном, не связанные с приливами
Раздражительность, нервозность, тревожность, сниженная самооценка
Сексуальные расстройства
Вагинальная атрофия
Ноктурия
Висцеральное ожирение
Остеопороз
Боли в суставах и мышцах, снижение мышечного тонуса и силы
Пациентки с разными типами климактерических расстройств имеют различные антропометрические и конституциональные характеристики.
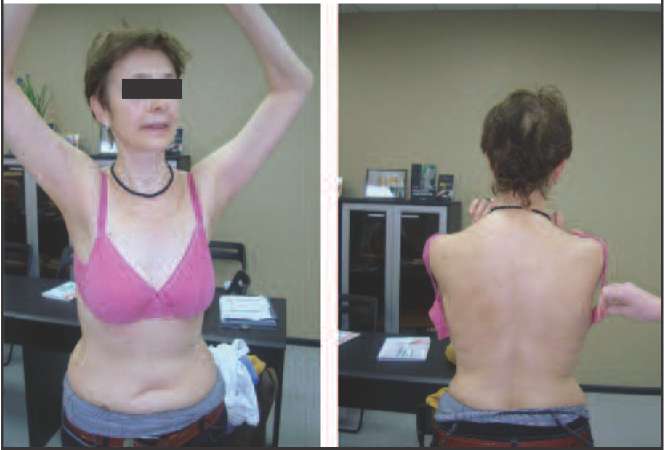
Так, к 1-му типу, протекающему с преимущественным снижением эстрогенов (эстроген-дефицитный тип), можно отнести пациенток, у которых не происходит выраженной прибавки массы тела, не характерно висцеральное ожирение, нет снижения либидо, благодаря чему они сохраняют сексуальную активность, нет депрессии и нарушения мочеиспускания, поэтому при данном типе климактерических расстройств пациентки зачастую продолжают работать и жить активной жизнью (рис. 1).
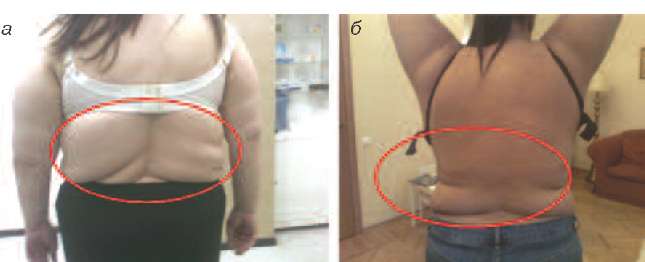
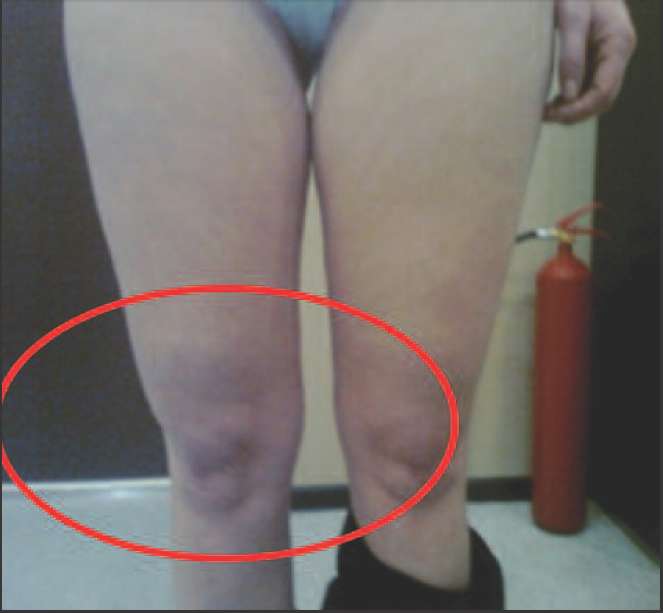
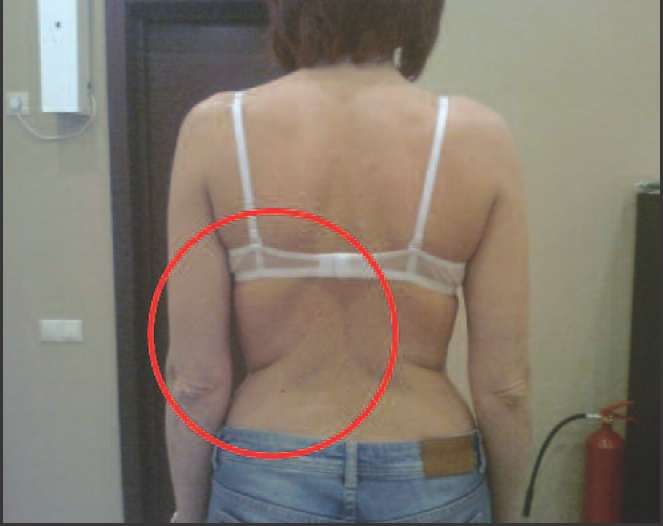
Ко 2 типу, протекающему преимущественно со снижением андрогенов (андроген-дефицитный тип) можно отнести пациенток, у которых в климактерии происходит прибавка массы тела преимущественно за счет отложения жира в области талии и живота (центральное, или висцеральное ожирение), отмечается гипотония мышц, что проявляется в провисании трицепса, появлении характерных складок на спине в виде «ламбрекенов», провисании передней группы мышц бедра (рис. 2-5).
Рис. 2. Пациентки 2-го типа (андроген-дефицитный): видны кожные складки на спине, являющиеся признаком гипотонии мышц спины вследствие дефицита андрогенов.
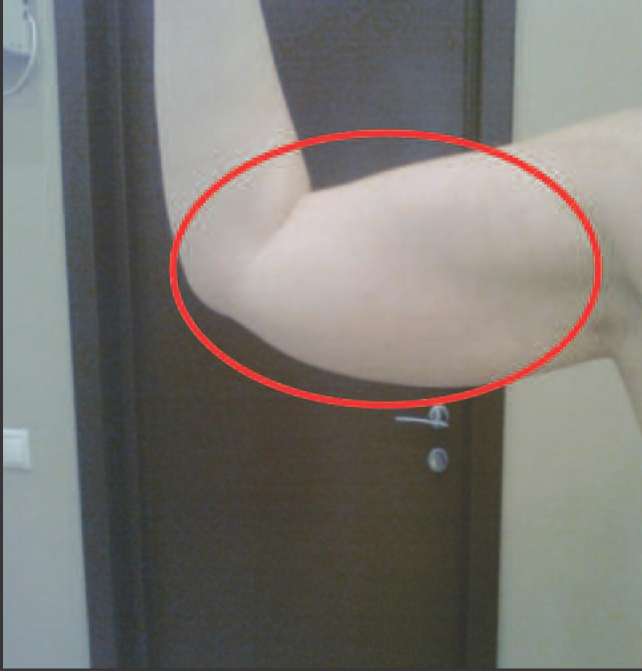
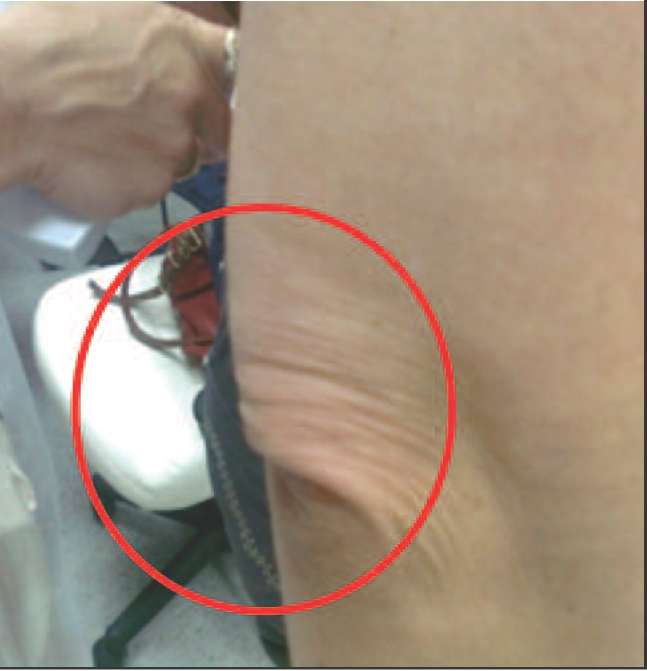
Рис. 3. Провисание трицепса плеча вследствие снижения мышечного тонуса на фоне андрогенного дефицита.
Рис. 4. Нависание трицепса, вертикальное положение (характерная складка над локтем).
Рис. 5. Нависание передней группы мышц бедра над коленной чашечкой вследствие снижения мышечного тонуса на фоне андрогенного дефицита.
Характерно также снижение либидо вплоть от отвращения к сексу, нарушения мочеиспускания, депрессии.
Рис. 6. Пациентка 3-го типа: отмечаются умеренная прибавку массы тела, гипотония мышц спины.
Возможности терапии
Учитывая разные типы течения климактерия и разные жалобы, пациенткам должна проводиться заместительная гормональная терапия (ЗГТ) с учетом данных особенностей.
Так, пациентки с клинически и лабораторно подтвержденным дефицитом андрогенов не должны получать препарат ЗГТ с антиандрогенными свойствами, в связи с тем что ряд жалоб (ожирение, снижение либидо, мышечная гипотония, ноктурия и др), обусловленных дефицитом андрогенов, могут только усугубиться.
В то же время при сохраненной секреции андроге-нов назначение препаратов с андрогенной активностью может привести к нежелательным явлениям андрогенизации: рост волос на лице, повышенная сальность кожи, чрезмерно повышенное либидо, прибавка мышечной массы.
Главная роль в лечении климактерических расстройств принадлежит эстрогенному компоненту, однако особенности гестагена, входящего в состав комбинированного препарата ЗГТ, также могут определять его дополнительные лечебные или потенциально негативные свойства [26].
Поэтому при отсутствии специальных показаний при выборе ЗГТ предпочтителен гестаген, обладающий высоким сродством к прогестероновым рецепторам для полноценной защиты эндометрия и при этом «нейтральный» в отношении других типов рецепторов, в том числе и андрогеновых.
Различия в сродстве гестагенов к тем или иным типам стероидных рецепторов представлены в табл.2.
Табл. 2 Относительное сродство прогестагенов к стероидным рецепторам [27]
Относительное сродство прогестагенов [% связывания стероидов]
Прогестероновые рецепторы
Андрогеновые рецепторы
Эстрогеновые рецепторы
Глюкокортикоидные рецепторы
Минералокорти-коидные рецепторы
Секс-стероид связывающий глобуллин (СССГ)
Adolf E. Schindler, Progestational effects of dydrogesterone in vitro, in vivo and on the human endometrium
Влияние заместительной эстроген-гестагенной и андрогензаместительной терапии на метаболические показатели у женщин в перименопаузе.
Метаболический синдром и СД являются главными факторами риска для развития сердечно-сосудистых осложнений, особенно в сочетании с артериальной ги-пертензией. Частота СД увеличивается с возрастом и менопаузой. Дефицит эстрогенов, возникающий в пе-рименопаузе в сочетании с абдоминальным ожирением и инсулинорезистентностью, является одним из факторов риска развития СД у женщин. В 2006 г. в мета-анализе, основанном на 107 исследованиях, было показано, что ЗГТ способствует уменьшению выраженности абдоминального ожирения, инсулинорезистентности, благоприятно влияет на липидный профиль и снижает число эпизодов впервые выявленного СД [12].
У относительно здоровых женщин в постменопаузе ни пероральный, ни трансдермальный эстрадиол существенно не влияли на уровень глюкозы. Однако было отмечено разное действие конъюгированных эквинных эстрогенов и эстрадиола (перорального и трансдермального) на чувствительность к инсулину: в то время как при назначении эстрадиола отмечалось увеличение чувствительности, конъюгирован-ные эквинные эстрогены, наоборот, ее уменьшали [13]. Прогестины оказывают влияние на углеводный обмен и инсулинорезистентность, однако их влияние зависит как от способа введения прогестина, так и от его типа. Такие прогестины, как медроксипроге-стерона ацетат (МПА) и норэтистерона ацетат, могут негативно влиять на углеводный обмен и усугублять инсулинорезистентность. Напротив, прогестерон и дидрогестерон не оказывают негативного влияния [13], поэтому назначение препаратов, в состав которых входит дидрогестерон (Фемостон®) является предпочтительным для женщин, у которых климактерические симптомы протекают на фоне ожирения, инсулинорезистентности, метаболического синдрома и СД, а также для тех, кому показана длительная ЗГТ.
Также в двойном слепом плацебо-контролируемом исследовании было показано, что назначение транс-дермального пластыря с тестостероном женщинам с андрогенной недостаточностью, вызванной гипопи-туитаризмом, приводило к улучшению чувствительности к инсулину [14].
Половые гормоны и функция эндотелия
Применение андрогенов у женщин показало положительное вазодилатирующее влияние. Так, S.Worboys и соавт. исследовали эффекты парентеральной терапии тестостероном у женщин, получающих ЗГТ. Было обследовано 33 женщины в постменопаузе, получающие ЗГТ более 6 мес в сочетании имплантами с тестостероном (50 мг). Контрольную группу составили 15 женщин, не получающих никакой терапии. При помощи ультразвукового исследования обследовались диаметр плечевой артерии, реактивная гиперемия (эн-дотелийзависимая вазодилатация) и действие нитроглицерина (эндотелийнезависимая вазодилатация). В основной группе отмечалось повышение уровней тестостерона, что ассоциировалось с увеличением на 42% эндотелийзависимой вазодилатации. В контрольной группе не было отмечено никаких изменений. Похожие данные были получены в отношении эндотелийнезави-симой вазодилатации. Авторы пришли к выводу, что парентеральная терапия тестостероном у женщин с дефицитом андрогенов в постменопаузе, длительно получающих ЗГТ, улучшает как эндотелийзависимую, так и эндотелийнезависимую вазодилатацию плечевой артерии [25].
Заключение
На сегодняшний день имеются данные, что андрогены у женщин могут оказывать положительное влияние на разные органы и системы, однако отсутствие в нашей стране сертифицированных для женщин препаратов тестостерона не позволяет широко применять их в гинекологической практике. Вместе с тем при выборе эстроген-гестагенных препаратов для ЗГТ необходимо учитывать индивидуальные особенности каждой пациентки. Препараты, содержащие дидрогестерон (Фемостон® 2/10, Фемостон® 1/10, Фемостон® 1/5 копти), обладают нейтральным эффектом в отношении андрогенного статуса женщины, не оказывая ни андрогенного, ни антиандро-генного действия, и не способны усугублять симптомы, вызванные снижением уровня тестостерона у пациенток, у которых менопауза протекает с дефицитом и эстрогенов, и андрогенов.
Статья подготовлена при поддержке компании Abbott. 2012/08-166
Что изменит дроспиренон в контрацепции и заместительной гормональной терапии?
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
Одним из важнейших экстрагенитальных эффектов эндогенного прогестерона является его антиминералкортикоидное действие как натурального антагониста альдостерона. Альдостерон, поддерживая активное поглощение натрия и выведение ионов калия и водорода с мочой в дистальных почечных канальцах, выполняет биологическую функцию регулятора внеклеточного обмена и метаболизма воды. В лютеиновую фазу менструального цикла на фоне увеличения секреции прогестерона происходит возрастание натрийуреза [4].
Эстрадиол и синтетические эстрогены обладают противоположным прогестерону натрий–сберегающим эффектом, который обусловлен в основном увеличением синтеза ангиотензиногена в печени и, соответственно, повышением уровня ангиотензина – главного стимулятора выработки альдостерона. Синтетические прогестагены – производные 17a–гидроксипрогестерона и 19–нортестостерона, не имеют антиминералкортикоидного эффекта и не противодействуют стимулирующему влиянию эстрогена на ренин–ангиотензин–альдостероновую систему (РААС). Результатом задержки натрия и жидкости у женщин, принимающих эстроген–содержащие препараты с целью контрацепции и заместительной гормональной терапии (ЗГТ), может быть увеличение массы тела вследствие задержки жидкости, отечность и повышение АД у предрасположенных женщин.
Дроспиренон – новый прогестаген – производное 17a–спиронолактона, спектр эффектов которого – прогестагенный, антиминералокортикоидный и антиандрогенный, свойственные натуральному прогестерону. Антиминералокортикоидная активность дроспиренона в 8 раз выше, чем у спиронолактона (диуретика с антиминералкортикоидной активностью) [5,6].
Результатами этого свойства препарата является уменьшение массы тела и снижение систолического и диастолического артериального давления. Вызываемая дроспиреноном потеря натрия в организме не приводит к клинически значимому повышению концентрации калия, что позволяет применять его даже у женщин с нарушением функции почек [1].
В исследовании Oelkers et al. установлено достоверное повышение кумулятивной экскреция натрия в группе здоровых женщин, получавших 2 мг дроспиренона, по сравнению с группой плацебо [7]. Следует отметить также и увеличение уровня альдостерона в плазме и экскреция его с мочой, что, по мнению авторов, характеризует компенсаторную активацию РААС в ответ на изменение электролитного состава крови.
В рамках того же исследования было показано, что дроспиренон достоверно повышает активность ренина плазмы, причем этот эффект не зависит от дозы препарата. Кроме того, выявлено некоторое снижение массы тела у пациенток, принимавших препарат, содержащий 30 мкг этинилэстрадиола и 3 мг дроспиренона (Ярина) [8,9], в отличие от женщин, принимавших контрацептив, содержащий 30 мкг этинилэстрадиола в сочетании с 150 мкг дезогестрела, у которых, наоборот, отмечалось некоторое увеличение массы тела [10,11].
Эти данные свидетельствуют о том, что дроспиренон в составе КОК способен эффективно противодействовать эстрoгензависимой задержке натрия и жидкости.
Дроспиренон является также антагонистом андрогенных рецепторов. Антиандрогенная активность дроспиренона выражена в 5–10 раз сильнее, чем у прогестерона, но ниже, чем у ципротерона ацетата [12–14].
Комбинированные оральные контрацептивы (КОК), угнетая секрецию андрогенов яичниками, оказывают положительное влияние на угревую сыпь и себорею. Кроме того, этинилэстрадиол (ЭЭ) вызывает повышение концентрации глобулина, связывающего половые стероиды (ГСПС), который уменьшает свободную фракцию андрогенов в плазме крови. Выраженность андрогенного эффекта прогестагена, входящего в состав комбинированных препаратов, существенно влияет на эффекты ЭЭ, такие как повышение ГСПС и антиатерогенные изменения спектра липопротеидов. Дроспиренон не снижает уровень ГСПС [15] и имеет антиатерогенное влияние на липидный обмен [16].
Применение комбинированных эстроген–гестагенных препаратов, содержащих дроспиренон, для контрацепции и заместительной гормональной терапии, позволяет получить дополнительные преимущества, связанные с фармакологическими и клиническими особенностями этого прогестагена.
Контрацепция с дроспиреноном
Современные гормональные контрацептивы дают реальную возможность регулировать сроки наступления беременности и таким образом снижать риск материнской смертности, связанной с абортами. Однако только этим не ограничивается их влияние на репродуктивное здоровье. Эстроген–гестагенные контрацептивы обладают многочисленными неконтрацептивными профилактическими и лечебными эффектами: уменьшают обильность, длительность и болезненность менструальной кровопотери, положительно влияют на состояние кожи, снижают риск анемии, внематочной беременности, воспалительных заболеваний органов малого таза, доброкачественных и злокачественных новообразований яичников, рака эндометрия.
В настоящее время, по данным ВОЗ (2001), гормональные методы контрацепции используют около 100 млн. женщин. Несомненно, что актуальность гормональной контрацепции будет возрастать и в дальнейшем.
Новый прогестаген дроспиренон входит в состав комбинированнного низкодозированного монофазного контрацептива Ярина (Schering AG, Германия), содержащего 30 мкг ЭЭ и 3 мг дроспиренона.
Как известно, эффективность методов контрацепции определяется числом беременностей, наступающих у 100 женщин за первые 12 месяцев использования контрацептива (индекс Перля). Для Ярины этот показатель составляет 0,07, что соответствует критериям высокоэффективного контрацептива [17].
Исследования длительности применения КОК показали, что около 30% женщин прекращают применение препаратов в течение первого года [18]. Основной причиной отмены КОК являются побочные эффекты [19]. Такие побочные эффекты, как увеличение массы тела, нагрубание и болезненность молочных желез, повышение уровня АД, связаны с влиянием ЭЭ на РААС.
Благодаря антиминералкортикоидной активности дроспиренон препятствует задержке натрия и жидкости в организме, что поддерживает стабильность массы тела, уровня АД и препятствует нагрубанию молочных желез при приеме Ярины. В течение первого месяца приема головная боль, напряжение молочных желез, снижение либидо, депрессия встречаются в 3,1–4,6%; тошнота – в 4,6–6,2% случаев. К шестому месяцу лечения все вышеуказанные симптомы в основном купируются [2].
Лечебные свойства КОК
с дроспиреноном
Дроспиренон, оказывающий на РААС эффект, подобный спиронолактону, открывает новые терапевтические возможности применения КОК.
В первую очередь это относится к терапии предменструального синдрома (ПМС). Не менее чем у 95% женщин репродуктивного возраста в той или иной степени за несколько дней до менструации наблюдаются такие симптомы, как раздражительность (93,8%), нагрубание и болезненность молочных желез (87,5%), метеоризм (75%), головная боль (56,3%), изменение настроения с наклонностью к депрессии (56,3%), отечность (50%) [3].
Применение КОК является наиболее распространенной терапевтической тактикой при ПМС. Однако при этом выраженность симптоматики ПМС не всегда уменьшается, а может даже усугубляться, что связано с дефицитом натурального прогестерона.
В многочисленных клинических исследованиях показано позитивное влияние препарата Ярина на соматические и психо–эмоциональные симптомы ПМС.
В открытом неконтролируемом исследовании, проведенном Apter D. и соавт. [20]. Эффективность препарата оценена у 336 женщин в возрасте от 18 до 42 лет с помощью опросника здоровья The Psychological General Well–Being Index (PGWBI), включающего такие показатели, как беспокойство, сниженное настроение, общее самочувствие, способность к контролированию своих эмоций, здоровье в целом, активность. Через три цикла лечения отмечалась тенденция к улучшению, а через шесть циклов было выявлено статистически значимое увеличение показателя общего самочувствия. Кроме того, проводилась оценка степени выраженности соматических симптомов. Уменьшение симптомов вздутия живота и нагрубания молочных желез произошло к 6 циклу приема препарата соответственно у 77,3 и 69% женщин. Кроме того, в 52% случаев больные отмечали уменьшение отечности конечностей. Масса тела оставалась стабильной или даже несколько снижалась. Несмотря на то, что в этом исследовании не была предусмотрена группа плацебо, этот недостаток компенсирован длительностью лечения (12 месяцев), т.к. известно, что уже через 3 – 6 месяцев эффект плацебо нивелируется [21].
В другом исследовании, проведенном в США в 2002 г., Borenstein J. и соавт. провели оценку влияния препарата на предменструальные симптомы и качество жизни более чем у тысячи женщин, страдающих ПМС. Предменструальные симптомы и качество жизни оценивались до начала лечения и через два цикла терапии. Использование Ярины привело к улучшению физических и психоэмоциональных симптомов ПМС, а также общего самочувствия и качества жизни [22].
Boschitsch E. и соавт. изучили эффективность применения Ярины и препарата, содержащего 30 мкг ЭЭ и 150 мкг дезогестрела, в терапии ПМС. В группе женщин, получавших Ярину, было отмечено достоверное снижение массы тела. Кроме того, произошло статистически значимое уменьшение тяжести предменструальных симптомов, таких как подавленное настроение, задержка жидкости, повышенный аппетит. Позитивное влияние препарат оказал на кожные проявления. Количество элементов угревой сыпи снизилось на 62,5%, себорея уменьшилась на 25,1%. После окончания исследования 75,6% женщин выразили желание продолжить прием препарата [23].
В исследовании Brown C. и соавт. 326 женщин в возрасте от 18 до 35 лет заполняли 23–компонентный опросник Women’s Health Assessment Questionnaire в начале наблюдения и после завершения 6 цикла приема Ярины. В конце 6 цикла было отмечено улучшение показателей по шкалам, характеризующим задержку жидкости и эмоциональный статус. Следует особо отметить, что результаты были аналогичны в группах пациенток, не пользовавшихся ранее оральными контрацептивами и использовавших ОК, не содержащие дроспиренон [24].
В рандомизированном плацебо–контролируемом исследовании Freeman E.W. и соавт. исследована эффективность препарата Ярина в течение 3 менструальных циклов у 82 женщины с тяжелым течением ПМС, так называемым предменструальным дисфорическим синдромом. У пациенток, получавших лечение препаратом, содержащим ЭЭ и дроспиренон, отмечалось значительно более выраженное улучшение по показателям опросника СОРЕ (the Calendar of Premenstrual Experiences) по всем 22 пунктам. Достоверная разница между группами была получена по фактору 3 – постоянный повышенный аппетит, акне [25,26].
Во всех вышеописанных исследованиях применялась стандартная схема приема препарата: прием 21–й таблетки с последующим семидневным перерывом. Известно, что именно в этот промежуток времени у женщин, принимающих оральные контрацептивы, чаще возобновляются симптомы ПМС [27].
Использование продленного режима КОК, когда больная получает препарат ежедневно в течение 9–12 недель и лишь затем делает перерыв, повышает эффективность терапии ПМС. Уменьшение симптомов в этом случае отмечают 74% женщин [28]. В случае использования такого режима приема кровотечения прорыва встречаются достаточно редко, менструальноподобная реакция наступает при отмене таблеток [29].
Учитывая эти данные, было проведено исследование применения Ярины в продленном режиме [30]. В нем приняли участие 1433 женщины, 175 из которых получали препарат непрерывно в течение 42–126 дней. Показано, что отечность конечностей уменьшилась на 49% у больных, принимавших препарат в продленном режиме по сравнению с 34% у пациенток, использовавших стандартную 21–дневную схему. Болезненность молочных желез снизилась на 50 и 40% соответственно, чувство вздутия живота на 37 и 29%. Также более эффективным является продленный режим приема у женщин с угревой сыпью. Частота кровотечений прорыва составила 15% в начале терапии и имела тенденцию к снижению по мере продолжения приема препарата. Не было отмечено повышения частоты других побочных эффектов.
Таким образом, продленный режим может быть использован для повышения терапевтической эффективности Ярины.
Антиандрогенные свойства КОК с дроспиреноном обусловлены несколькими механизмами: подавлением овуляции, способностью дроспиренона блокировать рецепторы к андрогенам и отсутствием снижения концентрации глобулина, связывающего половые стероиды [31].
Применение препарата Ярина патогенетически обосновано у женщин с избыточной массой тела или повышением артериального давления при приеме комбинированных контрацептивов, а также требующих терапии в связи с предменструальным синдромом, угревой болезнью, легкой артериальной гипертензией или «идиопатическими отеками».
Заместительная гормональная терапия с дроспиреноном
Прекращение эстроген–продуцирующей функции яичников, приводящее к развитию вазомоторных симптомов, нарушению сна, снижению устойчивости к психологическим и эмоциональным стрессам, урогенитальным и сексуальным расстройствам, изменению внешности, к остеопорозу, болям в спине и переломам, существенно снижает качество жизни женщин старшего возраста. Коррекция всех указанных проявлений является целью заместительной гормональной терапии в пери– и постменопаузе.
Дроспиренон входит в состав комбинированного препарата для непрерывной ЗГТ в постменопаузе Анжелик (Schering AG, Германия), содержащего 17b–эстрадиола и 2 мг дроспиренона.
Применение дроспиренона в комбинированном препарате для ЗГТ, аналогично Ярине, уменьшает частоту побочных эффектов (таких как мастодиния, отечность, увеличение веса вследствие задержки жидкости) и улучшает переносимость терапии. Повышение приемлемости терапии («комплаентности») является важнейшим условием ее максимальной эффективности, поскольку профилактические эффекты достигаются только при достаточной продолжительности терапии эстрогеном. Кроме того, антиальдостероновый эффект дроспиренона особенно важен для женщин старших возрастных групп, имеющих более высокую частоту гипертонической болезни и ишемической болезни сердца.
Известно, что ренин–ангиотензин–альдостероновая система имеет многокомпонентное воздействие на функцию сердечно–сосудистой системы. Ангиотензин II оказывает сильное прямое сосудосуживающее действие на артерии и менее сильное сосудосуживающее действие на вены. Кроме того, ангиотензин II служит главным стимулятором выработки альдостерона – основного регулятора водно–электролитного баланса, действующего через минералокортикоидные рецепторы в дистальных канальцах почек.
В то же время относительно недавно было обнаружено, что рецепторы альдостерона расположены также и в других органах, включая мозг, сосуды и сердце [32]. Это свидетельствует о роли альдостерона в физиологии и патологии сердечно–сосудистой системы. Избыточный синтез альдостерона, всегда сопровождающий течение сердечной недостаточности, приводит к стимуляции фибробластов, что, в свою очередь, вызывает повышение синтеза коллагена, развитие интерстициального фиброза, нарушение функциональной активности миокарда с развитием диастолической дисфункции левого желудочка. Кроме того, избыточный синтез альдостерона способствует повышению реабсорбции натрия, потере калия, ретенции воды в почечных канальцах, что, в свою очередь, приводит к увеличению объема циркулирующей крови и как следствие – к перегрузке левого желудочка сердца объемом и давлением, что также ведет к прогрессированию сердечной недостаточности.
Влияние альдостерона на развитие сердечно–сосудистой патологии включает воздействие на кардиальный и сосудистый фиброз, гипертензию, эндотелиальную дисфункцию, подавление фибринолиза, нарушение сердечного ритма. Показано, что применение блокатора альдостероновых рецепторов спиронолактона снижает уровень АД, улучшает функцию эндотелия, уменьшает гипертрофию левого желудочка сердца, снижает частоту фатальной аритмии и в результате приводит к 30%–ному снижению смертности среди пациентов с тяжелой сердечной патологией [32].
На больших когортах пациентов показано, что циркуляторный уровень норадреналина, ренина, ангиотензина II, альдостерона, эндотелина–1 и адреномедулина коррелирует как с тяжестью, так и с прогнозом хронической сердечной недостаточности. В частности, имеется сложная взаимосвязь между активностью ренин–ангиотензин–альдостероновой системы и гиперпродукцией эндотелина–1. Как показало исследование Framingham Offspring Study (Фрамингем, Массачусетс), даже у нормотензивных лиц однократное измерение в утренние часы альдостерона позволяло предсказывать вероятность повышения артериального давления спустя несколько лет.
В многоцентровом исследовании проведено изучение содержания калия в сыворотке крови и уровня АД у женщин 45–70 лет в постменопаузе, не имеющих и имеющих сахарный диабет, получающих препарат Анжелик и ингибиторы ангиотензинпревращающего фермента или блокаторы рецептора ангиотензина II [33]. У обследованных женщин отмечен гипотензивный эффект ЗГТ. Кроме того, ни в одной из наблюдаемых групп не было выявлено гиперкалиемии.
Гипотензивный эффект был подтвержден также результатами 12–недельного многоцентрового рандомизированного двойного слепого плацебо–контролируемого исследования влияния препарата Анжелик на уровень АД у 212 женщин в постменопаузе, имеющих умеренную гипертензию (АД в пределах 140/90–159/99 мм рт.ст.). По сравнению с группой плацебо у женщин, применявших Анжелик, отмечено достоверное снижение цифр АД и отсутствие значимых изменений содержания калия в сыворотке крови [34].
Представленные результаты исследований свидетельствуют о новых возможностях комбинированных эстроген–гестагенных препаратов, содержащих дроспиренон в качестве прогестагенного компонента. Контрацептивный препарат «Ярина» благодаря антиминерало кортикоидному и антиандрогенному эффекту дроспиренона обладает хорошей переносимостью, связанной с сохранением стабильного веса, отсутствием повышения АД, улучшением состояния кожи, эффективностью в отношении купирования предменструальных симптомов. Кроме того, получены данные, свидетельствующие о потенциальных возможностях ЗГТ с дроспиреноном снижать риск сердечно–сосудистой патологии у женщин в постменопаузе.
Литература
1. Андреева Е.Н. и др. Новые возможности гестагенов: дроспиренон – прогестаген с антиминералкортикоидными свойствами. Российский вестник акушера–гинеколога. 2004; 6.
2. Пасман Н.М. Ярина – первый опыт применения орального контрацептива с лечебными свойствами в Новосибирске. Российский вестник акушера–гинеколога. 2005;1.
3. Межевитинова Е.А., Прилепская В.Н. Предменструальный синдром. Гинекология 2002; приложение: 3–8.
4. Oelkers W. Drospirenone, a progestogen with antimineralocorticoid properties: a short review. Mol Cell Endocrinol. 2004 Mar 31;217(1–2):255–61.
5. Losert W, Casals–Stenzel J, Buse M. Progestogens with antimineralcorticoid activity. Arzneimittelforschung 1985;35:459–71.
6. Muhn P, Fuhrmann U, Fritzemeier KH, et al. Drospirenone: a novel progestogen with antimineralcorticoid and antiandrogenic activity. Ann N Y Acad Sci 1995; 761:311–35.
7. Oelkers W, Berger V, Bolik A, et al. Dihydrospirorenone, a new progestogen with antimineralcorticoid activity: effects on ovulation, electrolyte excretion, and the rennin–aldosterone system in normal women. J Clin Endocrinol Metab 1991;73:837–42.
8. Oelkers W, Helmerhorst FM, Wuttke W, et al. Effect of an oral contraceptive containing drospirenone on the rennin–angiotensin–aldosterone system in healthy female volunteers. Gynecol Endocrinol 2000;14:204–13.
9. Oelkers W, Foidart JM, Dombrovicz, et al. Effects of a new oral contraceptive containing an antimineralcorticoid progestogen, drospirenone, on the rennin–aldosterone system, body weight, blood pressure, glucose tolerance, and lipid metabolism. J Clin Endorinol Metab 1995;80:1816–21.
10. Huber J, Foidart JM, Wuttke W, Efficacy and tolerability of a monophasic oral contraceptive containing ethynilestradiol and drospirenone. Eur J Contracept reprod Health Care 2000;5:25–34.
11. Foidart JM, Wuttke W, Bouw GM, et al. A comparative investigation of contraceptive reliability, cycle control and tolerance of two monophasic oral contraceptives containing either drospirenone or desogestrel. Eur J Contracept Reprod Health Care 2000;5:124–34.
12. Huber J, Foidart JM, Wuttke W, Efficacy and tolerability of a monophasic oral contraceptive containing ethynilestradiol and drospirenone. Eur J Contracept reprod Health Care 2000;5:25–34.
13. Oelkers W, Berger V, Bolik A, et al. Dihydrospirorenone, a new progestogen with antimineralcorticoid activity: effects on ovulation, electrolyte excretion, and the rennin–aldosterone system in normal women. J Clin Endocrinol Metab 1991;73:837–42.
14. Fuhrmann U, Krattenmacher R, Slater EP, et al. The novel progestin drospirenone and its natural counterpart progesterone: biochemical profile and antiandrogenic potential. Contraception 1996;54:243–51.
15. van Vloten WA, van Haselen CW, van Zuuren EJ, Gerlinger C, Heithecker R. The effect of 2 combined oral Contraceptives containing either drospirenone or cyproterone acetate on acne and seborrhea. Cutis 2002 Apr;69(4 Suppl):2–15.
16. Gaspard U, Endrikat J, Desager JP, Buicu C, Gerlinger C, Heithecker R. A randomized study on the influence of oral contraceptives containing ethinylestradiol combined with drospirenone or desogestrel on lipid and lipoprotein metabolism over a period of 13 cycles. Contraception. 2004 Apr;69(4):271–8.
17. Huber J, Foidart JM, Wuttke W, Efficacy and tolerability of a monophasic oral contraceptive containing ethynilestradiol and drospirenone. Eur J Contracept reprod Health Care 2000;5:25–34
18. Pinter B. Continuation and compliance of contraceptive use. Eur J Contracept Reprod Health Care. 2002 Sep;7(3):178–83. Review. PMID: 12428939.
19. Aubeny E. et al. Oral contraception: patterns of non–compliance. The Coraliance study. Eur J Contracept Reprod Health Care. 2002 Sep;7(3):155–61.
20. Apter D, Borsos A, Baumgartner W, Melis GB, Vexiau–Robert D, Colligs–Hakert A, Palmer M, Kelly S. Effect of an oral contraceptive containing drospirenone and ethinylestradiol on general well–being and fluid–related symptoms. Eur J Contracept Reprod Health Care. 2003 Mar;8(1):37–51.
21. Wiklund I, Dimenas E, Wahl M. Factors of importance when evaluating quality of life in clinical trials. Control Clin Trials 1990;11:169–79.
22. Borenstein J, Yu HT, Wade S, Chiou CF, Rapkin A. Effect of an oral contraceptive containing ethinyl estradiol and drospirenone on premenstrual symptomatology and health–related quality of life. J Reprod Med. 2003 Feb;48(2):79–85.
23. Boschitch E, Skarabis H, Wuttke W et al. The acceptability of a novel oral contraceptive containing drospirenone and its effect on well–being. The Eur J of Contracept and Reprod Health Care 2000;5(suppl 3):34–40.
24. Brown C, Ling F, Wan J. A new monophasic oral contraceptive containing drospirenone. Effect on premenstrual symptoms. J Reprod Med. 2002 Jan;47(1):14–22.
25. Freeman EW, Kroll R, Rapkin A, Pearlstein T, Brown C, Parsey K, Zhang P, Patel H, Foegh M; PMS/PMDD Research Group. Evaluation of a unique oral contraceptive in the treatment of premenstrual dysphoric disorder. J Womens Health Gend Based Med. 2001 Jul–Aug;10(6):561–9.
26. Freeman EW. Evaluation of a unique oral contraceptive (Yasmin) in the management of premenstrual dysphoric disorder. Eur J Contracept Reprod Health Care. 2002 Dec;7 Suppl 3:27–34; discussion 42–3.
27. Sulak P, Scow RD, Preece C, et al. Hormone withdrawal symptoms in oral contraceptive users. Obstet Gynecol 2000;95:261–6.
28. Sulak PJ, Cressman BE, Waldrop E, et al. Extending the duration of active oral contraceptive pills to manage hormone withdrawal symptoms. Obstet Gynecol 1997;89:179–83
29. Clarke AK, Miller SJ. The debate regarding continuous use of oral contraceptives. Ann Pharmacother 2001;35:1480–4.
30. Sillem M, Schneidereit R, Heithecker R, et al. Use of an oral contraceptive containing drospirenone in an extended regimen. Eur J Contracept Reprod Health Care 2003;8:162–169.
31. Mansour D Experiences with Yasmin: the acceptability of a novel oral contraceptive and its effect on well–being. Eur J Contracept reprod Health Care. 2002 Dec;7 Suppl 3:35–41.
32. Stier TC, Koenig S, Lee DY, Chawla M, Frishman W. Aldosterone and aldosterone antagonism in cardiovascular disease: focus on eplerenone (Inspra) Heart Dis 2003;5:102–118.
33. Preston RA, White WB, Pitt B, Norris PM, Foegh M, Hanes V. Drospirenone/estradiol effect on serum potassium of postmenopausal women at risk for hyperkalemia. Obstet Gynecol 2004;103:4;26S–27S.
34. White WB, Pitt B, Foegh M, Hanes V. Drospirenone with estradiol lowers blood pressure in postmenopausal women with systolic hypertension. Obstet Gynecol 2004; 4, suppl.,26S.