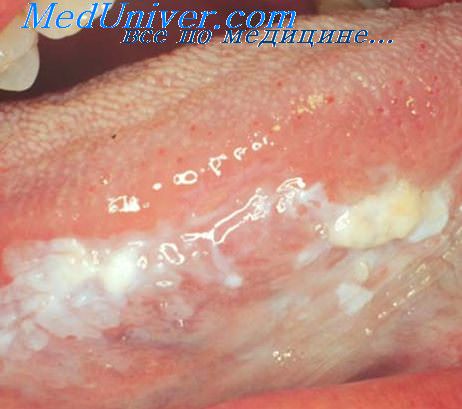
единичные митозы что значит
Митозы и митотический индекс
Дата создания: Октябрь 27, 2017
Дата изменения: Ноябрь 28, 2017
Митозы и митотический индекс
Новый показатель в гистологическом исследовании
Американский Объединенный комитет по онкологии добавил показатель частоты митозов в протокол клинической диагностики. Показатель митозов заменил другой индекс — уровень проникновения по Кларку для меланом, стадия T1.
Американские ученые (Dermatol Surg. 2011 Aug;37(8):1080-8) поставили задачу оценить необходимость биопсии сторожевых лимфоузлов на основании показателя митотической активности тонких (до 1 мм) меланом.
Что означает митотическая активность при меланоме?
Митоз — процесс деления (размножения клеток). Если в гистологическом препарате удаленной родинки (опухоли) определяются делящиеся клетки, находящиеся в процессе деления (митоза). Митотическая активность (митотический индекс) определяется под микроскопом, как процент делящихся клеток от 1000 клеток препарата (опухоли).
Наличие митозов демонстрирует рост и активность опухоли, а также дает определенный прогноз развития заболевания. Важно применить агрессивное лечение, в случаях, когда в гистологическом препарате определяются митозы. Вовремя проведенное правильное лечение спасает жизнь.
Одним из эффективных способов лечения и предотвращения метастазирования является биопсия сторожевого лимфоузла
Биопсия сторожевого лимфоузла
эффективное лечение и точный прогноз
В исследовании установлена необходимость выполнения биопсии сторожевого лимфоузла при митотическом индексе более 1, при толщине опухоли менее 1 мм. Также необходима биопсия сторожевого лимфоузла в случае изъязвления опухоли, при толщине опухоли менее 1 мм.
Митотический индекс оказался более четким прогностическим критерием, чем глубина проникновения по Кларку, в случае тонких меланом (до 1 мм). Самым точным методом, в этом случае, является биопсия сигнального лимфоузла.
При обнаружении микрометастазов в лимфоузле выполняется удалении регионарных лимфоузлов, что примерно на 20% повышает шанс на полное излечение.
Диагноз — меланома. Что делать?
Немедленно обращайтесь в клинику онкодерматологии Меланома Юнит
Вам будет составлен четкий план действий, в зависимости от предоставленных меддокументов и данных о заболевании
В данном случае промедление может привести к крайне неблагоприятным последствиям, даже в случае если Вам сказали только наблюдаться. На данный момент, в России биопсия сигнальных лимфоузлов при меланоме еще не выполняется
В большинстве случаев меланома поддается правильному лечению, на ранних стадиях практически гарантированно полное выздоровление.
Атипичные клетки – это рак или нет?
Атипичные клетки – это такие клетки, которые под воздействием различных неблагоприятных факторов из обычной нормальной клетки человеческого организма преобразовались в нехарактерную структуру, изменили свой размер и форму. Организм в свою очередь теряет контроль над такими клетками, поэтому существует риск перерождения атипических клеток, что может привести к образованию рака.
Что может повлиять на образование атипичных клеток:
Это некоторые факторы, которые могут привести к образованию атипичных клеток. К сожалению, точной причины их возникновения сказать никто не может. Даже какой-то незначительный сбой в организме может привести к возникновению не одной и даже не двух таких клеток, а тысяч.
Как происходит перерождение атипичных клеток в рак
Давно известно, что образование клеток с измененной ДНК появляются постоянно. Но появление атипичных клеток не всегда приводят к раку. В нашем организме есть защитный механизм, процесс старение и уничтожение клеток, так называемый апоптоз. Он отвечает за то, чтобы аномальные клетки исчезали из организма. Но любая система может дать сбой, и в результате атипичные клетки затаятся в организме. При таком раскладе есть вероятность их перерождения в раковые клетки.
Что делать, если обнаружили атипичные клетки во время биопсии? Рак это или нет?
В такой ситуации лучше перестраховаться, чем что-то пропустить. Ведь ранняя диагностика рака может спасти вам жизнь.
Иногда врач назначает какое-то конкретное лечение, чтобы постараться остановить образование атипичных клеток. Либо может понадобиться еще один образец ткани – дополнительная биопсия, чтобы быть уверенным в отсутствии рака или какого-то другого заболевания.
Единичные митозы что значит
В морфологической характеристике опухолевых клеток большую роль играют исследования митотического режима. Исчерпывающие сведения о митотическом режиме в нормальных клетках можно найти в фундаментальных работах И. А. Алова, а о митотическом режиме в опухолевых клетках—в работах И. А. Алова и И. А. Казанцевой.
Накопленные факты позволили определить следующие основные направления возможного использования исследования митотического режима в опухолях: 1) ранняя диагностика рака; 2) дифференциальная диагностика доброкачественных и злокачественных опухолей сходного гистогенеза; 3) разработка методов прогнозирования малигнизации предопухолевых процессов, 4) дифференциальная диагностика опухолей разного гистогенеза и уточнение гистогенетнческой принадлежности новообразования (первичного н метастатического), 5) оценка степени терапевтического повреждения опухоли.
Суммируя материалы, полученные И. А. Казанцевой, можно следующим образом охарактеризовать особенности митотического режима при гиперпластических и диспластических процессах и в опухолевых клетках.
Для многих нормальных эпителиальных тканей характерны умеренная митотическая активность, которая, однако, значительно выше в быстро обновляющихся тканях; примерно одинаковое количество клеток в стадии профазы и метафазы с преобладанием иногда первой; невысокая частота патологических митозов.
При фоновых процессах (умеренная дисплазня эпителия гортани и шейки матки, эпидермизация псевдоэрозий шейки матки, простая железисто-кистозная гиперплазия эндометрия и др. ) отмечают некоторое увеличение митотической активности, небольшое преобладание клеток в стадии метафазы, повышение количества патологических митозов, среди которых около 90% составляют колхициноподобные метафазы и отставание хромосом в метафазе.
При гиперпластических и диспластических процессах, которые могут рассматриваться как предраковые (тяжелая дисплазня шейки эпителия матки, атипическая гиперплазия эпителия гортани и др ), а также при некоторых доброкачественных опухолях может наблюдаться дальнейшее нарастание нарушений митотического режима, связанных с преобладанием метафаз, учащением числа патологических митозов и их разнообразие с появлением разновидностей, ведущих к анеуплоидин, расширение зоны, где встречаются делящиеся клетки.
Для клеток злокачественных опухолей характерно преобладание метафаз над другими стадиями митоза, резкое возрастание частоты патологических митозов, различная степень повышения митотической активности, нередко незначительная. Существуют опухоли, в которых митотическая активность ниже, чем в нормальных тканях. Мнение, что во всех опухолях клетки делятся чаше, чем в норме, неверно.
Нет, по-видимому, и прямой связи между митотической активностью и быстротой роста опухоли.
Обнаружение соответствующих нарушений митотического режима может быть дополнительным ранним диагностическим признаком наступившей малигнизации или иметь прогностическое значение при оценке предопухолевых процессов чем резче выражены нарушения митотического режима, тем неблагоприятнее прогноз.
Не исключено, что, возможно, имеют место некоторые различия в характере нарушения митотического режима в опухолях разного гистогенеза.
На основании изучения митотического режима может быть получена полезная информация для оценки степени повреждения опухолевых клеток при лучевом или лекарственном лечении новообразований. Например, снижение митотического индекса и нарастание так называемых комковатых митозов, являющихся разновидностью К-митозов и ведущих клетку к гибели, может служить одним из критериев терапевтического эффекта.
Исследование закономерностей митотического режима в новообразованиях имеет решающее значение для понимания механизмов, определяющих книети ку популяции опухолевых клеток, которая по многим параметрам оказывается весьма гетерогенной. Если рассматривать популяцию опухолевых клеток с точки зрения их деления, то следует отметить, что вышедшие из митотического цикла опухолевые клетки могут или вступить на путь диффереицировки, или вновь вступить в митоз и продолжать пролиферировать, или остаться в покоящемся состоянии. Таким образом, в популяции имеется 3 группы клеток, нахо дящихся во взаимосвязи друг с другом недифференцированные покоящиеся клетки, недифференцированные пролиферирующие клетки и дифференцирующиеся, но уже не пролифернрующие клетки.
Покоящиеся опухолевые клетки, как было показано О. И. Епифановой и соавт., сохраняют жизнеспособность и пролиферативный потенциал, они резистентны к химиотерапевтическим препаратам (цитостатикам, алкилирующим соединениям, антибиотикам), митотическим ингибиторам Сохраняя способность при каких-то условиях вновь вступать в митоз, эти клетки являются источником рецидивов, что делает их изучение крайне важным. Хотя существуют сведения о том, что в покоящихся опухолевых клетках ниже проницаемость плазматической мембраны, более резко конденсирован хроматин, возможно, в ДНК имеются участки, более прочно связанные с белком, повы шено обновление молекул, однако их практическая идентификация в опухоли пока еще невозможна, так как мы не знаем их особенностей нх обмена, ни их морфологических, гистохимических или ультраструктурных особенностей, ко торые позволили бы отличить их от других недифференцированных опухолевых клеток.
В связи с тем что недифференцированные пролиферирующие опухолевые клетки чувствительны к лучевому и химнотерапевтическому лечению, делают попытки перевести покоящиеся клетки в группу пролиферирующих путем гормональных воздействий или иных мероприятий.
Катаплазия на светооптическом уровне касается не только морфологии опухолевых клеток (их фенотипа), но еще в большей степени их морфогенетических потенций, что выражается в нарушении обычной тканевой и органной структуры новообразований. Органная и тканевая катаплазия, являющаяся, так же как инвазивный рост и метастазирование, наиболее характерным морфологическим признаком опухолевого роста, наряду с клеточной катаплазией составляют ту сумму признаков, которые позволяют на светооптическом уровне идентифицировать опухоль во всем многообразии ее строения.
Классические гистологические методы поэтому были и остаются основой морфологической диагностики новообразований человека, однако использование только их не дает возможности решать встающие перед онкологией новые задачи. Расширить методические возможности морфологической верификации новообразований можно с помощью таких современных способов исследования, как электронная микроскопия, гистохимия, иммуногистохимия. Анализ ультраструктурных, гистохимических, иммуногистохимических и биологических особенностей опухолевых клеток главным образом в плане диагностики и установления гистогенеза новообразований человека дан в последующих трех разделах.
Метастазы — как выявить раньше вторичной опухоли
Метастазы — злокачественные клетки, отделившиеся от первичного новообразования и перенесенные с током крови или лимфы в другие участки тела. Зачастую метастазы в органах и тканях обнаруживаются на поздних стадиях онкопатологии. Именно поэтому очень важно вовремя понять, является ли обнаруженная у человека опухоль первичным очагом и распространяет ли он патологические клетки за свои пределы.
Метастазы — что это такое
О том, что такое метастазы при раке и насколько они опасны, знают не только врачи — для людей с онкопатологиями этот термин особенно пугающий. Появление метастазов значит, что раковые клетки оторвались и начали перемещаться из очага, возникшего первым. Результатом их распространения становится образование опухоли в других органах, тканях.
Распротраняются патологические клетки по сосудам с током крови (гематогенные) и лимфы (лимфогенные). Метастазы попадают в кровеносное и лимфатическое русло в случае травмирования сосудов, расположенных в непосредственной близости от первичной опухоли.
В крови и лимфе обнаруживаются циркулирующие опухолевые клетки (ЦОК). Когда они прикрепляются к стенке сосуда или к органу, через который он проходит, метастазы выходят за пределы своего транспортного коридора и начинают активно делиться.
В случае, когда человек обладает крепким иммунитетом, метастазы не образуют новые опухоли. Намного опаснее ситуация, при которой иммунная защита организма ослаблена. Тогда появление аномальных клеток приводит к быстрому образованию и росту множественных очагов опухоли, которые нарушают структуру нормальных тканей, сдавливают жизненно важные органы, вызывают сильные боли и приводят к гибели человека.
Симптомы метастазов
В зависимости от того, в каком органе из-за распространения аномальных клеток сформировалась опухоль, возникают характерные симптомы. Например, метастазы в трубчатых костях, позвоночнике вызывают их хрупкость, возникают множественные переломы. Человек испытывает нестерпимые боли.
При появлении вторичных очагов опухоли в головном мозге возникают характерные симптомы:
Симптомы метастазов в легких (они возникают на фоне рака ЛОР-органов, молочной железы, прямой кишки и других органов):
Появление множественных вторичных очагов в печени сопровождается желтухой, сильной интоксикацией.
Стадии развития метастаз
Риск появления метастазов в других органах зависит от вида рака и стадии на которой выявлена первичная опухоль. Если первичное новообразование диагностировано рано, и пациент с ним получил лечение на первой стадии, то риск метастазирования сведен к минимуму.
Онкологи выделяют несколько стадий развития вторичных опухолевых очагов:
Скорость его развития и симптомы, которые испытывает больной человек, зависят от вида рака, его агрессивности, локализации вторичного новообразования.
Диагностика метастаз
Выявить метастазы удается с использованием различных диагностических методов. Наиболее эффективными для обследования больных с подозрением на метастазы являются:
Метод диагностики врачи определяют в индивидуальном порядке, ориентируясь на вид рака, предполагаемое место, где сформировалась вторичная опухоль (по симптомам) и особенностям крово- и лимфообращения в области первичного новообразования.
Диагностику с целью выявления метастазов проводят как до начала первого курса лечения, так и после удаления первичной раковой опухоли.
Лабораторные исследования также очень информативны, если нужно обнаружить вторичное новообразование и определить характер метастазов на ранних стадиях.
Один из наиболее эффективных методов — ранняя иммунологическая диагностика. Она позволяет выявить единичные циркулирующие опухолевые клетки или целые их конгломераты, вовремя начать лечение и не допустить усугубления патологического процесса.
Циркулирующие опухолевые клетки очень коварны — всего несколько их, попавших в кровоток, может перенестись в головной мозг, легкие, печень или другие органы. Там клетки могут пребывать в состоянии ожидания в течение долгих лет. В случае, если возникает достаточно сильный стимул, они начинают быстро размножаться и формируют опухоль.
ЦОК практически не реагируют на облучение и воздействие химиопрепаратами. Анализ крови на ЦОК позволяет выявить их во время лечения и по окончании полного курса. Те пациенты, у которых после терапии обнаруживаются ЦОК, причисляются к группе повышенного риска, у них могут появиться метастазы.
При каких видах рака выявляется ЦОК
Анализ крови на циркулирующие опухолевые клетки позволяет обнаружить их при большинстве раковых процессов, развивающихся из эпителиальных тканей и при меланоме. Максимально информативна диагностика по крови при новообразованиях молочной железы у женщин, предстательной — у мужчин, а также при раке прямой кишки.
Врачи делают вывод о наличии гематогенных или лимфогенных метастазов, если показатель ЦОК на 7,5 мл венозной крови превышает:
Более высокие показатели сопряжены с большой угрозой метастазирования и коротким периодом ремиссии.
Диагностика по методу ДОК
Чтобы вовремя выявить метастазы при меланоме, раке молочной железы важны и другие методы лабораторной диагностики. Так, единичные патологические клетки удается обнаружить в костном мозге при помощи анализа диссеминированных опухолевых клеток (ДОК). На основании этого исследования специалисты определяют реальную распространенность аномальных клеток и степень риска появления метастатических очагов.
Как проводится анализ на ЦОК и ДОК
Иммунологическое исследование клеток костного мозга (диссеминированые опухолевые клетки), 6 цветная проточная цитометрия;
Иммунологическое исследование опухолевых клеток периферической крови (циркулирующие опухолевые клетки), 6 цветная проточная цитометрия.
ЦОК и ДОК — диагностика относится к числу жидкостных исследований. Для выявления онкологических клеток по методике ЦОК у пациента берут порцию венозной крови, для ДОК проводится стернальная пункция (забор образца костного мозга, от 0,5 до 1 мл).
Полученный биоматериал инкубируют с добавлением специальных антител, а затем определяют количество и качество аномальных клеток, их жизнеспособность.
Диагностика по методу ЦОК и ДОК дает возможность:
Особенности лечения метастазов
Чтобы уничтожить метастазы, применяются хирургические и консервативные методы лечения.
Часто метастазы в лимфоузлах, отдельные очаги, расположенные в органах удаляют одновременно с основной опухолью. Проводится операция по удалению метастазов при помощи традиционных хирургических методов. С этой же целью применяется кибер-нож и протонно-лучевая терапия.
Чтобы остановить распространение новых очагов рака, после операции проводится курс, в котором сочетаются химио— и таргетная терапия, а также облучение.
Противоопухолевые препараты больному вводят внутривенно, в некоторых случаях применяется методика артериального введения лекарства максимально близко к пораженному органу. Комплексное лечение останавливает метастазирования и вызывает уменьшение опухоли.
Своевременно сделанные анализы позволяют выявить онкозаболевания на самых ранних этапах, провести лечение и минимизировать угрозу множественных метастазов при уже имеющихся онкообразованиях.
Пройти иммунологическую диагностику клеток костного мозга (ДОК) или исследование опухолевых клеток, циркулирующих в периферической крови (ЦОК) можно в лабораторном отделении нашего центра.
Филиалы и отделения где применяется инновационный метод диагностики метастазов
МРНЦ им. А.Ф. Цыба – филиал ФГБУ «НМИЦ радиологии» Минздрава России.
Единичные митозы что значит
ИГХ, иммуногистохимическое исследование ткани, исследование образца опухолевой ткани, исследование ткани опухоли.
Какой биоматериал можно использовать для исследования?
Локализация б/м: образец ткани (биоптат) опухолевого образования стенки матки.
Общая информация об исследовании
Миома матки является самым распространенным доброкачественным новообразованием органов женской репродуктивной системы и выявляется у 25-30 % женщин.
Самая высокая заболеваемость и большинство показаний к оперативному лечению (быстрый рост, большие размеры узла, подозрение на малигнизацию лейомиомы) приходятся на перименопаузальный возрастной период, являющийся наиболее критическим по подобным рискам в жизни женщины. Возникающие болезни адаптации и компенсации, эндокринные, метаболические и иммунологические расстройства предрасполагают к манифестации опухолевых заболеваний.
Существуют определенные трудности в тактике ведения данного контингента больных. Реальный прогресс в решении проблем морфологической диагностики опухолей достигнут с использованием иммуноцистохимических методик. Оценка пролиферативной активности опухоли стала возможной на основании анализа белков ядра, связанных с репликацией ДНК, выявленных при помощи антител к Ki-67. Полученные данные помогают определиться с методикой лечения и объемом оперативного вмешательства по поводу быстро растущей миомы. Прежде всего это касается решения вопроса о сохранении придатков матки.
Большое значение при выборе тактики лечения, прогнозе риска осложнений имеет установление гистологического типа лейомиомы матки. ВОЗ рекомендует выделять обычную, или простую, лейомиому и гистологические варианты лейомиомы (клеточная, митотически активная, эпителиоидная, миксоидная, атипическая лейомиома и липолейомиома и т. д.). В настоящее время описано три основные формы миомы матки: 1) простая лейомиома, развивающаяся по типу доброкачественной очаговой мышечной гиперплазии, 2) митозы отсутствуют вовсе либо 3) единичные. Данная методика позволяет помочь в диагностике и дифференцировании лейомиом.
Иммуногистохимия (ИГХ) – метод выявления точной локализации клеточного или тканевого компонента (антигена) с помощью иммунологических и гистохимических реакций; при этом иммунологический анализ срезов тканей или цитологического материала проводится в условиях сохранения морфологии клеток. В диагностической практике можно выделить несколько основных областей применения ИГХ: во-первых, при исследовании опухолей человека в целях определения гистогенеза недифференцированных опухолевых образований, отдаленных метастазов, для дифференцировки различных тканевых компонентов, составляющих комплексные опухоли; во-вторых, в целях прогностической оценки дальнейшего течения заболевания и, наконец, при назначении терапии.
В целях прогностической оценки заболевания, предсказания биологического поведения опухоли, появления метастазов, эффективности терапии проводят исследование пролиферативной активности (Ki-67), выраженности ангиогенеза, выявление рецепторов к стероидным гормонам, изучение степени анаплазии клеток (мутантный белок гена p53).
Антиген Ki-67 является специфичным и оптимальным для широкого использования в патологоанатомической практике маркером пролиферации. Он впервые описан Gerdes и соавторами в 1983 г., состоит из двух полипептидных цепей с молекулярной массой 345 и 395 кДа. Это основная часть нуклеарного матрикса, в течение интерфазы ассоциированная с хромосомами фазы митоза. Ki-67−димерная молекула, имеющая тесную связь с 10-й хромосомой, конкретная роль этого протеина в процессе клеточного деления до сих пор точно не выяснена. Экспрессия Кi-67 позволяет выделить опухолевые клетки, находящиеся в активной фазе клеточного цикла, на всём его протяжении (G1-, S-, G2- и M-фазы). Кi-67 отсутствует только в G0-периоде. Активно пролиферирующие опухолевые клетки представляют собой «фракцию роста» новообразования. Антиген Ki-67, выявляемый соответствующими моноклональными антителами, представляет собой короткоживущий протеин, он разрушается в течение 1,5-2 часов. Поэтому антитела к Ki-67 выявляют только делящиеся клетки, так как Ki-67 не успевает накапливаться и не остается в покоящихся клетках. Пролиферативная активность является ведущим фактором как в механизме злокачественной трансформации клеток, так и в биологическом поведении уже возникших опухолей. Это наиболее важная характеристика фенотипа опухоли, в значительной степени определяющая скорость роста новообразования, риск метастазирования, потенциальный ответ на лечебные мероприятия и исход онкологического заболевания. Многие факторы, влияющие на течение и исход онкологических заболеваний, свое патогенетическое действие на опухоль опосредуют через изменение пролиферативной активности. Оценка пролиферативной активности опухолевых клеток необходимо не только для определения биологических характеристик опухолей, но и для селективного подхода к выбору терапии.
Индекс пролиферативной активности в различных опухолях имеет разные значения, являясь при этом независимым прогностическим признаком, определяющим клиническое течение и прогноз заболевания. При Ki-67 менее 15 % опухоль считается менее агрессивной, при показателе более 30 % опухоль считается высокоагрессивной. При высоком уровне (выраженном в %) Ki-67 опухоль с более высокой вероятностью ответит на химиотерапевтическое лечение. При низком его уровне опухоль при определённых условиях лучше отреагирует на гормонотерапию. Тест проводится на образце ткани, полученном из опухоли в результате биопсии или оперативным путем.
Дополнительно проводится комплексное определением пролиферативной активности гладкомышечных актинов – сократительных белков, являющихся главными компонентами системы микрофиламентов клетки. Выявлено шесть основных изоформ актина. Антитела к альфа-актину гладких мышц являются надежными маркерами для определения гладкомышечных опухолей. SMA и α-SMA также окрашивают клетки с частичной гладкомышечной дифференцировкой: перициты, миоэпителиальные клетки и миофибробласты. Определение перицитов вокруг сосудистых структур – признак доброкачественного сосудистого процесса, тогда как в большинстве злокачественных сосудистых новообразованиях число перицитарных клеток снижено. Высокая экспрессия гладкомышечного актина отмечается при непролиферативной и умеренной степени пролиферативной формы лейомиомы. В случае пролиферативной формы изменений выраженной степени экспрессия гладкомышечного актина слабее. Маркером, определяющим благоприятное течение заболевания, является высокая экспрессия гладкомышечного актина.
Комплексное гистологическое и иммуногистохимическое исследование с определением пролиферативной активности в растущих лейомиомах по экспрессии KI-67 и гладкомышечного актина представляет ценный современный метод диагностики, позволяющий определить степень пролиферативной активности и анаплазии опухолевых клеток, охарактеризовать прогноз и предложить адекватные методы лечения. Однако не следует и преувеличивать возможности данного метода при лечении конкретного пациента. Данный вид обследования является только дополнительной методикой исследования, и его результаты должны быть интерпретированы в контексте с другими данными обследования, включая клинические.
Для чего используется исследование?
Когда назначается исследование?
Что означают результаты?
При использовании данного метода визуализации антигенов должно получиться интенсивное четко выявляемое окрашивание тканевых антигенов в исследуемом образце и позитивном контроле. Окрашивание негативного контроля также необходимо принимать во внимание при оценке специфичного расположения исследуемых антигенов. Интерпретация полученных результатов ИГХ-реакции включает такие термины, как «выраженная позитивная реакция», «ложно-позитивная реакция», «негативная реакция», «ложно-негативное окрашивание».
Кто назначает исследование?