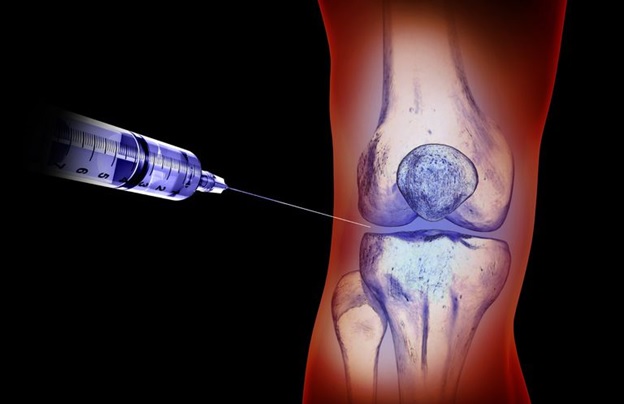
Экстраартикулярное введение препарата что это
Околосуставное введение лекарственных препаратов
Околосуставные инъекции: показания для проведения и особенности процедуры
Околосуставное или периартикулярное введение лекарств – инъекции препаратов в мягкие ткани вокруг сустава – сухожилия, фасции, связки, апоневрозы и мышцы. Их назначают при различных патологиях опорно-двигательного аппарата, чаще всего воспалительного и дегенеративно-дистрофического характера.
Преимущества околосуставных инъекций
Показания для проведения инъекций
Основными показаниями для выполнения околосуставных инъекций являются выраженный болевой синдром и воспаление, которое не получается снять другими препаратами. В зависимости от очага поражения уколы назначают при таких заболеваниях:
Также околосуставные инъекции назначают при травмах, если долго не спадает отек, а боль и воспаление продолжат нарастать.
Препараты для околосуставного введения

Но следует знать, что при дегенеративно-дистрофических процессах глюкокортикостероиды малоэффективны. Они способны только уменьшить ответную реакцию организма, купировав симптомы болезни, но не остановить разрушение хрящевой ткани сустава. Поэтому околосуставные инъекции практически не применяются в качестве основного лечения, а всегда входят в комплексную терапию.
Особенности проведения процедуры
Перед инъекцией кожа обрабатывается антисептиком. Препарат вводят вместе с анестетиком в одном шприце. По просьбе пациента перед уколом может быть сделана местная аппликационная анестезия.
Для поиска места для инъекции проводят УЗИ сустава. После уточнения локализации патологического процесса опытный ревматолог без труда выполнит околосуставное введение препарата. Курс и частоту уколов врач подбирает в зависимости от диагноза, состояния сустава и реакции организма на инъекции. При положительной динамике процедуру повторяют несколько раз с интервалов в 7-12 дней.
Периартикулярная блокада
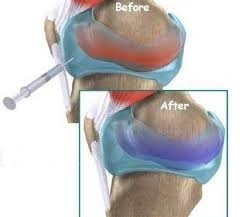
Блокадой называют процедуру, во время которой в пораженный сустав вводят лекарство для купирования болевого синдрома. При прогрессировании дегенеративных процессов блокада входит в состав комплексной терапии.
При проведении периартикулярной блокады инъекцию делают в околосуставные ткани (мышцы, сухожилия, связки). Поэтому ее также называют околосуставной.
Преимущества околосуставных инъекций
Периартикулярная блокада максимально быстро (за 2-3 минуты) устраняет боль и избавляет от дискомфорта, что объясняется несколькими факторами:
Процедура проводится в амбулаторных условиях и не требует госпитализации, не вызывает побочных действий.
Препараты, которые используются для блокады, обладают пролонгированным действием – действуют на протяжении длительного времени.
Во время инъекции пациент не ощущает боли, благодаря чему нет необходимости в дополнительной анестезии.
Показания и противопоказания
Периартикулярную блокаду делают при невыносимых болях и резком обострении болевого синдрома, а также перед проведением курса лечения.
Околосуставные инъекции рекомендованы при:
Противопоказана процедура при:
Препараты для блокады
Для периартикулярной блокады используют несколько групп препаратов:
Как делают блокаду?
Для инъекций используют шприц с тонкой иглой. Если вводится несколько лекарств, то их предварительно смешивают.
Есть 2 вида уколов в околосуставную область: наружный и двусторонний. При наружном делают одну инъекцию, а при двустороннем – 2 (с внутренней и наружной стороны).
Препарат и количество инъекций подбирает специалист в зависимости от заболевания, размеров сустава, выраженности болевого синдрома и состояния пациента. На тазобедренном и коленном суставах блокаду обычно проводят раз в 3 месяца, а на меньших сочленениях – раз в 2-3 недели.
Результаты блокады
Процедура ослабляет либо полностью снимает боль, устраняет отечность, расслабляет мышечные спазмы, нормализует состав внутрисуставной жидкости, затормаживает дегенеративные процессы, восстанавливает двигательную амплитуду.
Но все же основное предназначение блокады – купирование симптоматики. Поэтому ни в коем случае при исчезновении боли не стоит отказываться от основной терапии.
Также для успешного выздоровления необходимо заниматься лечебной физкультурой, соблюдать диету, вести здоровый образ жизни.
Где сделать в Лобне?
В медицинском центре «Гармония» вам окажут квалифицированную помощь и моментально снимут боль.
Для инъекций мы используем самые эффективные и безопасные препараты, не вызывающие побочных действий.
Все манипуляции выполняют опытные специалисты.
Стоимость услуг
| Код | Наименование услуги | Стоимость |
|---|---|---|
| 1212 | Периартикулярная блокада | 1500 руб |
| 1213 | Препарат клиники (дипроспан) для проведения блокады | 1000 руб |
Примечание
ООО «Гармония» предоставляет скидки в размере 10%:
Периартикулярное введение лекарственного препарата
Периартикулярное введение препарата – это инъекции в периартикулярные ткани. Периартикулярные ткани – это мягкие ткани, окружающие сустав.
К ним относятся:
Периартикулярные патологии развиваются при многих ревматических заболеваниях, но чаще являются самостоятельным воспалительным или дегенеративным процессом и могут возникать в любой из околосуставных структур.
В зависимости от очага воспаления выделяют следующие заболевания, при которых показаны периартикулярные инъекции:
Для точной диагностики локализации патологического процесса используется УЗИ суставов. Если очаг проблемы выявлен точно, то квалифицированному ревматологу не составит труда выполнить адресное периартикулярное введение препарата. Точное попадание в цель позволяет не только снять воспаление и убрать болевой синдром, но и позволяет избежать хронизации заболевания. Кроме того, патологические изменения, возникшие в одной структуре, довольно быстро распространяются и на прилежащие ткани. Поэтому важно своевременно диагностировать нарушения и уделить должное внимание лечению.
Какие препараты вводят периартикулярно?
В лечении патологий околосуставных тканей используются глюкокортикоиды – синтетические аналоги гормонов надпочечников. Они наиболее эффективны при воспалительных патологиях, менее эффективны – при дегенетивно-дистофических. Их назначают при длительных, не поддающихся терапии другими препаратами воспалительных заболеваниях, сопряженных с болями и нарушениями функций суставов.
Эффект наблюдается уже после первой инъекции и сохраняется длительно (в зависимости от препарата до нескольких месяцев).
Как это делается?
Кожа обрабатывается йодом, затем спиртом. Препарат вводится в одном шприце с анестетиком. Для особо чувствительных пациентов может быть выполнена аппликационная местная анестезия.
Врач выбирает, какой препарат, в какой дозировке и сколько раз будет вводиться для достижения оптимального эффекта.
Время – хороший врач, но только если речь не идет о болезнях суставов. Долгое время оставаясь без наблюдения, патология только усугубляется. Периартикулярное введение препарата поможет блокировать процесс и избавит от боли. Для того чтобы получить консультацию ревматолога по подбору препарата, запишитесь на прием по телефонам клиники: +7(495)949-96-80, +7(499)493-24-00, +7(909)974-33-88 или через форму заявок в верху страницы.
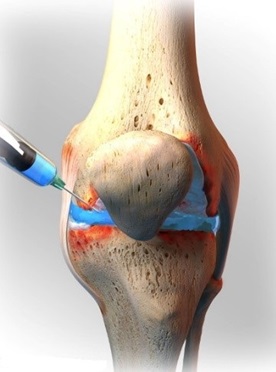
Внутрисуставное введение гилауроновой кислоты
Внутрисуставная инъекция обычно назначается, когда боль в суставе не удается снизить с помощью других консервативных методов лечения, включая болеутоляющие средства, пероральные противовоспалительные препараты и физическую терапию.
Типы внутрисуставных инъекций
Цель внутрисуставных инъекций может варьироваться в зависимости от используемого препарата. Хотя обезболивание является наиболее распространенной целью инъекций в сустав, их также можно использовать для доставки химиотерапевтических препаратов, таких как Доксил (доксорубицин), непосредственно в сустав, пораженный раком. Они также могут быть эффективным средством ликвидации грибковой инфекции в суставах (грибковый артрит).
При использовании для облегчения боли различные внутрисуставные инъекции действуют по-разному:
Внутрисуставные инъекции гиалуроновой кислоты при остеоартрите
Гиалуроновая кислота вырабатывается организмом человека. Это естественная часть жидкости, которая помогает смазывать суставы и обеспечивает их бесперебойную работу.
Когда у пациента остеоартрит, количество гиалуроновой кислоты в пораженном суставе уменьшается. Инъекции гиалуроновой кислоты компенсируют дефицит этого вещества.
Препараты с гиалуроновой кислотой называют эндопротезами синовиальной жидкости, так как они берут на себя роль лубрикантов в суставах.
Кому показаны внутрисуставные инъекции гиалуроновой кислоты?
Врачи не могут точно предсказать, кому из пациентов в большей степени помогут инъекции гиалуроновой кислоты. Но многие врачи назначают эти инъекции пациентам с остеоартрозом, у которых стандартные методы лечения не дают эффекта.
Внутрисуставные инъекции гиалуроновой кислоты также часто назначают пациентам, которые по тем или иным причинам не могут принимать НПВС.
Насколько эффективны внутрисуставные инъекции гиалуроновой кислоты при остеоартрите?
Исследования показывают, что инъекции гиалуроновой кислоты у некоторых пациентов с ОА могут действовать более эффективно, чем болеутоляющие средства. Другие исследования показали, что по эффективности они не уступают кортикостероидам.
Что ожидать при инъекциях гиалуроновой кислоты?
В зависимости от того, какой тип эндопротеза синовиальной жидкости использует врач, количество инъекций может варьироваться – это может быть одна инъекция или от трех до пяти инъекций, с промежутками в одну неделю между процедурами. Облегчение боли обычно достигается через 4-12 недель, и эффект, как было показано, длится до нескольких месяцев. Лечение можно повторить по мере необходимости.
Инъекция проводится одинаково для всех типов препаратов. Сначала врач очищает область. Если колено опухло от избыточной жидкости, врач может ввести местный болеутоляющий препарат, а затем вставить иглу в сустав для удаления жидкости. С помощью той же иглы в суставе, врач может ввести гиалуроновую кислоту в коленный сустав.
После инъекции пациент должен исключить тяжелые нагрузки в течение одного или двух дней. В противном случае эффективность инъекций снижается.
Побочные эффекты
Наиболее распространенными кратковременными побочными эффектами являются незначительная боль в месте инъекции и небольшое увеличение объема суставной жидкости. Эти симптомы, как правило, снижаются в течение нескольких дней.
Иногда при использовании некоторых форм гиалуроновой кислоты может возникать серьезная реакция с отеком, покраснением и болью, называемая псевдосептической реакцией. Достаточно редко инъекция может обострить воспалительный процесс.
Препараты гиалуроновой кислоты для инъекций в суставы
Существует несколько вариантов инъекций гиалуронана, также называемых viscosupplementation, которые используются для лечения остеартрита. Они вводятся непосредственно в сустав. Они включают:
Как действует внутрисуставная инъекция гиалуроновой кислоты?
Нормальная суставная жидкость содержит вещество, называемое гиалуронан. Она действует как амортизатор и смазка в суставе и необходима для нормальной функции сустава. Гиалуронан очень вязкий и позволяет хрящевым поверхностям костей плавно скользить друг по другу. Это приводит к снижению симптомов остеоартрита.
Какие суставы, пораженные остеоартритом, можно лечить с помощью этих инъекций?
В настоящее время препараты доказали свою эффективность только для лечения умеренно выраженного остеоартрита коленного сустава. Тем не менее, возможно введение этих препаратов и в другие суставы.
Противопоказания для внутрисуставных инъекций
Противопоказания для любой внутрисуставной инъекции будут включать:
Относительные противопоказания включают кристаллические инъекции стероидов вблизи критических артерий или суставов. Большие кристаллы стероидов потенциально могут оказывать механическое эрозионное действие при нагрузке сразу после инъекции кортикостероидов. При введении гиалуроновой кислоты также не рекомендуются значительные нагрузки на сустав в течение нескольких дней.
Факторы риска, которые необходимо учитывать до проведения процедуры:
Каждый врач, выполняющий внутрисуставные инъекции на регулярной основе, в конечном итоге должен столкнуться с решением, следует ли вводить внутрь внутрисуставного пространства препарат после суставной артропластики. Инфекционное осложнение после суставной артропластики может быть катастрофическим, включая удаление аппаратного обеспечения, введение устройств с антибиотиками, длительный прием антибиотиков и пересмотр процедуры артропластики. Однако могут быть моменты, когда эффект перевешивает риск, и врач может выполнить эту процедуру. Следует обратить внимание на потенциальную активацию латентных инфекций, таких как Mycobacterium tuberculosis, Nocardia, Cryptococcus, Pneumocystis, Borrelia burgdorferi, токсоплазмоз и т. д. при использовании кортикостероидов.
Инъекции под контролем УЗИ
Ультразвуковые методики вмешательства быстро становятся популярной новой технологией. С улучшением разрешения изображения и переносимостью новой ультразвуковой технологии, а также с отсутствием радиационного воздействия ожидается, что использовании УЗИ для инъекций будет приобретать популярность. Изображения подтвержденного начального размещения иглы, а также положения после инъекции должны быть сохранены.
ЛОКАЛЬНАЯ ТЕРАПИЯ ОСТЕОАРТРОЗА
Остеоартроз (ОА) — хроническое дегенеративно-дистрофическое заболевание суставов, характеризующееся прогрессирующей деструкцией суставного хряща, пролиферативной реакцией хрящевой и костной ткани и часто сопутствующим вторичным синовитом. Терапия боль
Остеоартроз (ОА) — хроническое дегенеративно-дистрофическое заболевание суставов, характеризующееся прогрессирующей деструкцией суставного хряща, пролиферативной реакцией хрящевой и костной ткани и часто сопутствующим вторичным синовитом.
Терапия больных ОА должна проводиться с использованием системно назначаемых лекарственных препаратов. Однако при этом возникают проблемы с их переносимостью, взаимодействием, противопоказаниями. Это обусловливает применение локальной терапии (ЛТ), которая при ОА патогенетически показана и клинически эффективна.
Преимущества локальной терапии:
Необходимо отметить, что ЛТ не исключает, а, наоборот, часто проводится в сочетании с лечением, воздействующим на организм в целом.
Различают несколько видов локальной терапии:
Аппликационная терапия
Один из наиболее широко распространенных методов ЛТ — аппликационное применение лекарственных препаратов, что обусловлено простотой и безболезненностью процедур, при которых не повреждаются кожные покровы.
Разработаны специальные требования для локально назначаемых средств. Местно применяемый препарат должен быть эффективен при подлежащей лечению патологии; не должен вызывать местных токсических и аллергических реакций; должен достигать органа-«мишени»; концентрация препарата в сыворотке не должна достигать уровня, при котором возникают зависимые от дозы побочные эффекты; метаболизм и выведение препарата должны быть такими же, как при системном применении. При аппликационном применении предполагается создание терапевтической концентрации препарата в тканях в месте нанесения, при этом в общий кровоток поступает лишь незначительное количество вещества, что позволяет практически свести на нет системные побочные эффекты [12].
Широкое распространение в аппликационной терапии ОА нашли мази согревающего и отвлекающего характера как синтетические, так и на основе пчелиного и змеиного ядов: финалгон, апизартрон, випратокс.
В лечении мышечных и суставных болей традиционно применяются мазевые препараты, содержащие:
Патогенетически обусловленным представляется использование мазевых средств, содержащих нестероидные противовоспалительные препараты (НПВП) (бутадионовая, индометациновая, вольтареновая мази, крем долгит, фастум гель и многие другие). Для получения клинического эффекта при использовании мазей, содержащих НПВП, необходимо применять их достаточно длительно, соблюдать кратность аппликаций, наносить на кожу достаточное количество препарата. Местные НПВП эффективны при острой и хронической боли и часто применяются при ОА как препараты, не вызывающие побочных действий со стороны желудочно-кишечного тракта. Тем не менее исследований, посвященных сравнению эффективности локальных НПВП и оральных НПВП при ОА [20, 21, 25], пока не проводилось.
В лечении артрита хорошо зарекомендовал себя диметилсульфоксид (димексид), 50%-ный водный раствор которого в виде аппликаций на пораженный сустав обладает противовоспалительным и обезболивающим эффектом. Кроме того, димексид как хороший растворитель является проводником для пенетрации в мягкие ткани других медикаментов (новокаина, анальгина, но-шпы, гидрокортизона). Это средство используется как в аппликационной ЛТ остеоартроза, так и для улучшения введения лекарств при электрофорезе методом электродрегинга [1, 10, 13].
Недостатком аппликационного метода ЛТ является невысокая концентрация лекарственного средства, проникающего в ткани (в среднем до 5% используемого количества). Лекарственный препарат резорбцируется в мягкие ткани сквозь выводные протоки потовых и сальных желез, волосяные фолликулы, межклеточные пространства. Степень проникновения препарата зависит от его липофильности и правильного увлажнения рогового слоя эпидермиса. Затрудняют проникновение лекарства в глубь тканей барьерные функции кожных покровов, в том числе перепад градиентов рН.
Физиотерапевтическое лечение
Широко применяемые физиотерапевтические методы лечения ОА уменьшают болевой синдром, мышечный спазм, воспалительные процессы, улучшают микроциркуляцию и трофику, благоприятно воздействуют на метаболические процессы в тканях сустава.
В период обострения ОА, обусловленного реактивным синовитом, используют ультрафиолетовое облучение, электрическое поле УВЧ, переменные магнитные поля низкой частоты, электрофорез анальгина, новокаина, тримекаина, димексида на область пораженного сустава.
В период стихания обострения, а также в начальной стадии заболевания, когда явления синовита слабо выражены или отсутствуют, показаны воздействия электромагнитными полями высоких и сверхвысоких частот (индуктотермия, дециметровая и сантиметровая волновая терапия), импульсные токи низкой частоты — синусоидальные модулированные и диадинамические, магнитотерапия, лазерное воздействие, фонофорез гидрокортизона. Для стимуляции трофики суставного хряща проводят электрофорез лития, кальция, серы, цинка, гумизоля. Для потенциирования обезболивающего действия применяют СМТ-форез новокаина, анальгина, салициловой кислоты [2, 4, 8].
Из различных физиотерапевтических методов хорошо зарекомендовал себя лекарственный электрофорез, сочетающий терапевтическое воздействие постоянного электрического тока и медикаментозного средства, вводимого с его помощью.
Среди механизмов биологического действия постоянного электрического тока можно выделить следующие физико-химические эффекты:
Под действием электрического тока в подлежащих тканях активируются системы регуляции локального кровотока и повышается содержание биологически активных веществ (брадикинина, калликреина, простагландинов) и вазоактивных медиаторов (ацетилхолина, гистамина). В результате происходят расширение просвета сосудов кожи и ее гиперемия.
Расширение капилляров и повышение проницаемости их стенок вследствие местных нейрогуморальных процессов возникает не только в месте приложения электродов, но и в глубоко расположенных тканях, через которые проходит постоянный электрический ток. Наряду с усилением крово- и лимфообращения, повышением резорбционной способности тканей наблюдаются ослабление мышечного тонуса, усиление выделительной функции кожи и уменьшение отека в очаге воспаления. Кроме того, вследствие электроосмоса снижается компрессия болевых проводников, более выраженная под анодом.
Постоянный электрический ток усиливает синтез макроэргов в клетках, стимулирует обменно-трофические процессы в тканях, увеличивает фагоцитарную активность макрофагов, ускоряет процессы регенерации, стимулирует ретикулоэндотелиальную систему, повышает активность факторов неспецифического иммунитета.
Таким образом, постоянный электрический ток обладает следующими лечебными эффектами: противовоспалительным, метаболическим, вазодилятирующим, санирующим (дренирующе-дегидратирующим), анальгетическим, миорелаксирующим, седативным (на аноде) [2, 8].
При ОА с болевым синдромом без клиники синовита, пролиферативных явлениях, вазотрофических расстройствах, контрактурах показаны тепловые процедуры, включая аппликации парафина, озокерита, иловой, торфяной грязи. В стадии ремиссии эффективны морские, радоновые, сульфидные, йодобромные, бишофитные ванны.
В последнее время для лечения ОА с успехом применяются бишофитные ванны. Бишофит — естественный минерал в виде твердых солей и сверхкрепких рассолов, распространен в ряде регионов нашей страны. Наиболее известно Волгоградское месторождение бишофита. Бишофит включает в себя редкий и специфический хлоридно-магниево-натриевый комплекс, не имеющий аналогов в курортной практике. Основу его составляют следующие компоненты: хлорид магния — 415-460 г, бромид магния — 4-9 г, хлорид натрия — 5 г, хлорид калия — до 5 г, хлорид кальция — до 4 г, сульфат кальция — до 1 г, гидрокарбонат кальция — до 0,5 г. Кроме того, в бишофите содержится много микроэлементов (йод, бор, медь, железо, кремний и др.). Экспериментальным путем доказаны низкая токсичность бишофита, отсутствие в его среде патогенной флоры, аллергенных, канцерогенных свойств и, что особенно важно, наличие анальгетического и противовоспалительного эффектов [14].
С целью укрепления мышц возможно применение электромиостимуляции.
Лечебный массаж уменьшает мышечный спазм, повышает тонус ослабленных мышц, стимулирует трофику пораженных суставов, улучшает функциональные способности больного. Массаж, проводящийся вне обострения ОА, должен быть щадящим по отношению к пораженным суставам; необходимо избегать механического раздражения суставной капсулы; особое внимание следует обращать на работу с прилегающими к суставу мышцами.
Локальная инъекционная терапия
Аналогами инъекционного введения различных веществ в природе могут служить укусы змей, пчел, ос и т. д. Примером первого сознательного использования инъекционного введения препаратов человеком является, по всей видимости, применение различных ядов для стрел. Классическим стал пример применения индейцами Южной Америки кураре во время охоты, и только значительно позднее парентеральный способ начал использоваться в лечебных целях. Для введения лекарственных препаратов в организм Гиппократ 2400 лет назад применил полую трубку, к концу которой был прикреплен мочевой пузырь свиньи. В 1836 году во Франции La Farque изобрел шприц — ланцет-троакар — для введения веществ под кожу, а впоследствии Wood (1855) усовершенствовал этот шприц, добавив к нему полую иглу. Современнй шприц был предложен Aneli в 1857 году. В 1894-1897 годах Luer ввел в практику цельные стеклянные шприцы всевозможных размеров. В 1906 году был сконструирован шприц типа «Рекорд» со стеклянным цилиндром, металлическим поршнем и металлической иглой.
Коленный сустав наиболее удобен в техническом отношении для инъекций, и поэтому он чаще всего используется для локальной терапии. При выполнении пункции больной лежит на спине с выпрямленными ногами. Точка вкола находится на латеральной стороне на 1-1,5 см проксимальнее верхнего края надколенника. Игла, вводимая по направлению к щели между надколенником и бедренной костью, попадает в широкую супрапателлярную сумку, при этом врач испытывает ощущение провала иглы в полость. Техника проведения пункций других суставов описывалась как в первых отечественных руководствах по артрологии, так и во многих зарубежных пособиях по ревматологии [3, 19].
Самая длительная история в плане инъекционного введения в сустав у новокаина, который как местно-анестезирующее вещество для ЛТ в настоящее время используется наиболее широко. Новокаин низкотоксичен, обладает достаточно большим временем действия, не вызывает местного раздражения. Обезболивающий эффект препарата не усиливается при концентрации выше 0,5%. Местные анестетики действуют на тонкие, безмякотные (немиелинизированные) волокна и, следовательно, снижают только ощущения, а не управление произвольными движениями, тогда как новокаин блокирует проводимость нерва, замещая по конкурентному типу ионы кальция на мембране. Это создает препятствие потоку ионов натрия и предотвращает деполяризацию и распространение потенциала действия.
Новокаин, представляющий собой гидрохлорид 2-диметиламинэтилового эфира парааминобензойной кислоты, в сыворотке крови быстро гидролизуется, образуя парааминобензойную кислоту и диметиламиноэтанол. Диметиламиноэтанол — эффективный антиконвульсант, хотя конвульсии и являются одним из побочных эффектов новокаина. Другой продукт гидролиза — парааминобензойная кислота, калиевая соль которой обладает антифиброзным действием. Таким образом, продукты гидролиза новокаина сами обладают потенциальным положительным воздействием. Из неанальгетических реакций новокаина, как и других местно-анестезирующих веществ, отмечают локальное расширение артериол, значительное усиление микроциркуляции крови. Внутримышечная инъекция новокаина вызывает в течение 24-72 часов умеренную местную инфильтрацию нейтрофилами, лимфоцитами, макрофагами. Дж. Г. Травел (1989) считает желательным при инфильтрации болевых точек добавлять в раствор новокаина глюкокортикоиды в двух случаях: при наличии у больного симптомов воспаления соединительной ткани и при развитии постинъекционной болезненности и аллергических реакций как ответа на введение новокаина [27].
Значительное распространение новокаиновые блокады пораженного сустава получили со времен Payr, который вводил 0,5%-ный раствор новокаина с адреналином в сустав и достигал таким образом хорошего болеутоляющего эффекта. М. О. Фридланд в 1955 году писал об эффективности спирто-новокаиновых блокад сустава в период обострения артроза. P. F. Matzen (1961) рекомендовал применять блокады болевых точек 0,5-1%-ным раствором новокаина.
Целая эпоха в локальной терапии заболеваний суставов связана с глюкокортикоидами. Новая эра началась в 1948 году. 21 сентября в клинике Мейо Hench сделал больному ревматоидным артритом первую внутримышечную инъекцию кристаллов кортизона и добился того ярко выраженного эффекта, который всем хорошо известен. Сегодня результаты его исследований подтверждены сотнями исследований, в которых приняли участие тысячи пациентов. Глюкокортикоиды стали называть «улучшенным аспирином» или «эликсиром жизни».
За полвека применения в медицине глюкокортикоиды зарекомендовали себя как наиболее эффективные противовоспалительные средства. Это единственная группа лекарств, сочетающих быстро проявляющиеся противовоспалительные и иммунодепрессивные свойства [3, 11, 18, 19, 27].
Впервые больному с ревматоидным синовитом в коленный сустав 10 мл гидрокортизона ввел Y. W. Thorn (Бостон, 1950). Полученный положительный эффект автор приписал общему резорбтивному действию лекарства и поэтому прекратил дальнейшие исследования в этом направлении. Выраженный положительный эффект от интраартикулярных инъекций глюкокортикоидов отметил в 1951 году J. L. Hollander (Филадельфия), вводивший ацетат гидрокортизона в коленные суставы больным ревматоидным артритом и остеоартрозом, что вызывало подавление синовита в первые 24 часа после инъекции в 90% случаев. Продолжительность благоприятного действия составляла около 8 дней, а последующие инъекции оказались столь же эффективными, как и первая. Наиболее полно и обстоятельно автор изложил результаты проведенных исследований в 1966 году, когда опубликовал итоги 15-летнего опыта локальной кортикотерапии. За этот период J. L. Hollander оценил результаты 150 000 инъекций глюкокортикоидов, сделанных более 5000 больных различными артритами, бурситами, тендовагинитами, и подтвердил их противовоспалительный и анальгетический эффекты [11, 19].
Внедрение в клиническую практику локальной глюкокортикоидной терапии (ЛГТ) при лечении как пораженных суставов, так и мягких околосуставных тканей (при ревматических заболеваниях и, в частности, при ОА) стало одним из крупнейших достижений медицины середины XX века [11].
Выраженного противовоспалительного и обезболивающего эффекта можно добиться при внутрисуставном введении гидрокортизона, метипреда, кеналога, дипроспана. Последние характеризуются более мощным и пролонгированным лечебным воздействием. Высоким клиническим эффектом обладает дипроспан, 1 мл которого включает 2 мг бетаметазона динатрия фосфата, действующего в первые часы после введения, и 5 мг бетаметазона дипропионата, действующего в течение 4-6 недель. Глюкокортикоиды снижают уровень клеточного метаболизма, подавляют пролиферативные процессы, продукцию металлопротеиназ и интерлейкина-1, участвующих в деструкции хряща. Возможно одновременное введение анестетиков (новокаина, лидокаина), действие которых на фоне глюкокортикоидов потенциируется. Необходимо отметить, что частота интраартикулярного введения глюкокортикоидов ограничена из-за возможного усиления остеопороза и отрицательного влияния на хрящ. Отсутствие эффекта при однократном (максимум двукратном) введении глюкокортикоида является противопоказанием для дальнейших внутрисуставных инъекций препарата. Это связано с тем, что причиной болей может быть не обострение синовита, а, например, повреждение хряща. Если в течение одного года глюкокортикоиды вводятся в сустав более 4 раз, необходимо пересмотреть тактику лечения данного больного [11, 18].
Обезболивающий эффект оказывает параартикулярное введение глюкокортикоидов в так называемые болевые точки, часто сопутствующие ОА, такие, как область большого вертела бедренной кости, область «гусиной лапки» коленного сустава. Предпочтительно при этом вводить меньшее количество глюкокортикоида с увеличенной дозой анестетика [3, 4, 5, 16, 19].
В. Младенович делит осложнения ЛГТ на внутрисуставные и внесуставные [9].
Способы контроля за важнейшими нежелательными последствиями ЛГТ представлены в табл. 1.
На основании 10-летнего наблюдения над больными ОА, получавшими ЛГТ, мы пришли к следующим заключениям.
Таким образом, у пациентов с ОА коленных суставов при условии учета показаний (стадии болезни, оценки сопутствующих заболеваний, анализа проведенного предшествующего лечения), соблюдения техники выполнения ЛГТ, количества и кратности процедур, правильного выбора доз вводимых препаратов локальная терапия инъекциями глюкокортикоидов может быть признана эффективной и рекомендоваться для лечения обострений ОА (табл. 2).
К патогенетическому лечению ОА относится введение в полость сустава препаратов, обладающих хондропротекторными свойствами. К ним относятся артепарон; полусинтетический хондроитинсульфат; гиалуроновая кислота, принимающая участие в формировании эластических свойств хряща; альфлутоп, обладающий антигиалуронидазной активностью. Их справедливо считают средствами базисной терапии ОА. Эти препараты благодаря биологическому сродству с суставным хрящом легко проникают в него, подавляют активность протеолитических ферментов, стимулируют обмен хрящевой ткани, задерживают развитие дегенетаривного процесса [7, 22, 23, 24, 26].
Не так давно удалось установить роль токсических дериватов кислорода (супероксидного аниона кислорода и гидроксильного радикала ОН) в развитии воспалительных изменений в суставе. Супероксидный анион кислорода нейтрализуется ферментом супероксиддисмутазой, который в настоящее время выделен в чистом виде и применяется в клинической практике под названием орготеин. Введение 8 мг орготеина один раз в неделю в коленные суставы 3-5 инъекций на курс приводит к заметному клиническому улучшению у 76% больных ОА [6].
Определенные надежды возлагаются и на внутрисуставное введение димексида [10].
Выраженный синовит является показанием для пункции сустава, удаления синовиальной жидкости и введения препаратов — ингибиторов медиаторов воспаления: контрикала (трасилола), гордокса. Для усиления противовоспалительного эффекта желательно также вводить глюкокортикоиды.
При некупируемом синовите показано внутрисуставное введение активных реагентов, вызывающих поверхностный некроз синовиальной оболочки, что влечет за собой так называемую химическую или физическую консервативную синовэктомию (синовиортез). Для химической редукции синовита используются эндоксан, осмиевая кислота, для физической — радиоактивные изотопы: золото-198, иттрий-90, излучающие бета- и гамма-лучи. Несмотря на то что положительный эффект данной терапии при ревматоидном артрите можно считать доказанным, тем не менее она не нашла широкого применения при ОА.
Способы интра- и периартикулярного введения лекарственного препарата могут быть различными: традиционные игольно-шприцевые инъекции; безыгольные инъекции; игольно-струйные инъекции.
В 1956 году в Нью-Йорке M. Ziff, V. Contreras, F. R. Schmid применили струйный инъектор Hyposprey для внутрисуставных инъекций гидрокортизона. Препарат вводился 71 больному в межфаланговые, пястнофаланговые, локтевые, лучезапястные, коленные суставы из стандартных доступов (всего в 178 суставов). Клиническое улучшение или полная ремиссия были получены у 76,5-94,3% больных. В качестве одного из преимуществ безыгольных инъекций следует отметить безболезненность процедуры.
Добавим, что часть инъекций исследователи провели на себе, а больные, ранее получавшие игольно-шприцевые инъекции, предпочли в дальнейшем введение препаратов инъектором Hyposprey.
Авторы для лечения больных ОА коленных суставов использовали отечественный полуавтоматический комбинированный игольно-струйный инъектор «ИСИ-1», предложенный М. В. Провоторовым и И. А. Ханиным (Воронеж, 1982) для трансторакального интрапульмонального введения препаратов. Интра- и периартикулярные игольно-струйные инъекции кеналога с новокаином в коленный сустав, проведенные больным с ОА с помощью инъектора «ИСИ-1», обладали выраженным клиническим эффектом [17].
Лекарственный электрофорез с перифокальным депонированием препаратов
При лекарственном электрофорезе основными путями пенетрации лекарств в ткани являются выводные протоки потовых и сальных желез, волосяные фолликулы и, в меньшей степени, межклеточные пространства. Лекарственные вещества в основном накапливаются в эпидермисе и дерме, образуя так называемое кожное депо ионов, где могут находиться от 3 часов до 15-20 суток. Лекарство постепенно диффундирует в лимфатические и кровеносные сосуды, проникая в воспаленные очаги.
Введение препаратов с помощью электрофореза проходит безболезненно и не сопровождается повреждением кожи. Действие лекарств усиливается вследствие введения их в ионизированном виде. Тем не менее при электрофорезе количество вводимого в ткани лекарственного вещества невелико и колеблется от 2 до 10% исходного количества (нанесенного на прокладку). В ткани лекарства проникают на небольшую глубину [2, 8].
В большинстве случаев лечение ОА с помощью физических факторов проводится в отсроченный период обострения, в стадии стихающего синовита — на «сухой, холодный» сустав. В целях купирования острого синовита широко используется (нередко в стационарных условиях) интраартикулярное введение глюкокортикоидов, зарекомендовавшее себя как достаточно эффективный способ.
Интраартикулярное введение препаратов наряду с множеством преимуществ имеет и ряд недостатков: процедура достаточно сложна в выполнении; возможны осложнения, к которым прежде всего относятся инфицирование полости сустава и повреждение хряща. Особенно сложно осуществлять внутрисуставные инъекции больным с ОА, так как у них сужены и деформированы суставные щели, склерозирована фиброзная капсула сустава, невысок объем синовиального выпота.
Для лечения ОА, учитывая достоинства и недостатки обоих методов ЛТ, мы использовали их сочетание, применив лекарственный электрофорез с инъекционным перифокальным депонированием препаратов в мягкие околосуставные ткани.
В последние десятилетия в практике физиотерапии применяется внутритканевый лекарственный электрофорез, представляющий собой модификацию электрофореза, предполагающего не нанесение медикаментозного средства на кожу, а введение его в ткани и полости с последующей гальванизацией данной области. В зависимости от способа введения различают собственно внутритканевый и внутриполостной лекарственный электрофорезы [15].
В целях повышения клинической эффективности ЛТ при перифокальном депонировании лекарственных препаратов мы заменили гальванизацию области сустава лекарственным электрофорезом, тем самым добившись двойного депонирования фармакологических средств.
Для инъекционного перифокального депонирования желательно использовать новокаин и гидрокортизон, руководствуясь накопленным опытом их применения при электрофорезе.
Инъекционное перифокальное депонирование лекарственных препаратов осуществлялось в мягкие ткани медиальной поверхности коленного сустава ниже уровня суставной щели, где к большеберцовой кости прикрепляются объединенное сухожилие полусухожильной, портняжной и стройной мышц, а также сухожилие полумембранозной мышцы и образуется так называемая «гусиная лапка». Часто встречающаяся патология этой области — анзериновая энтезопатия — может протекать как самостоятельное заболевание, а также развиваться на фоне ОА коленного сустава. Клинически эффективные и широко применяемые локальные инъекции анестетика с глюкокортикоидом при анзериновой энтезопатии способствовали выбору данной области сустава для создания перифокального депо препаратов [5, 16, 19].
Техника выполнения лекарственного электрофореза с перифокальным депонированием препаратов состоит в следующем. В первый день пациенту параартикулярно в мягкие ткани внутренней поверхности коленного сустава, ниже уровня суставной щели шприцем вводится от 5 до 10 мл 0,5%-ного раствора новокаина с 50 мг суспензии гидрокортизона — создается перифокальное депо препаратов. Далее с первого дня и на протяжении 10 последующих ежедневно выполняется электрофорез новокаина по следующей методике. Электроды прямоугольной формы накладываются поперечно на коленный сустав. Сила тока составляет 15-20 мА, продолжительность воздействия — 20 минут. Раствор новокаина вводится с прокладки положительного электрода (анода).
При лечении необходимо учитывать противопоказания как для инъекционной терапии (прежде всего соблюдение правил асептики), так и для выполнения электрофореза (состояние коронарных и миокардиальных резервов пациента, наличие пролиферативных заболеваний, болезней органов кроветворения и других, а также переносимость электрического тока).
В результате лечения отмечен положительный эффект, характеризующийся снижением болевого синдрома, уменьшением окружности сустава и увеличением объема движений в нем. Лекарственный электрофорез с перифокальным депонированием препаратов зарекомендовал себя как эффективный, технически безопасный, отличающийся хорошей переносимостью и минимальным числом побочных явлений способ. Авторы надеются, что данный метод получит широкое распространение в лечении остеоартроза.