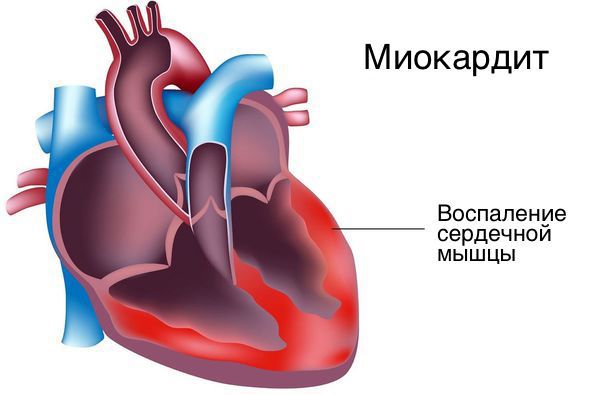
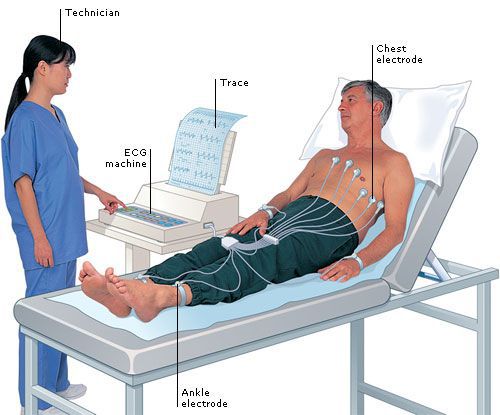
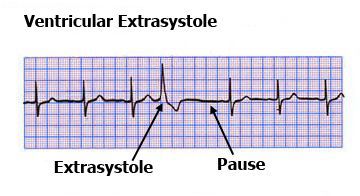
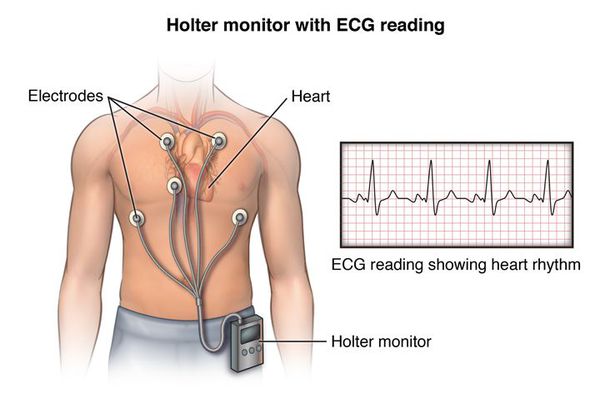
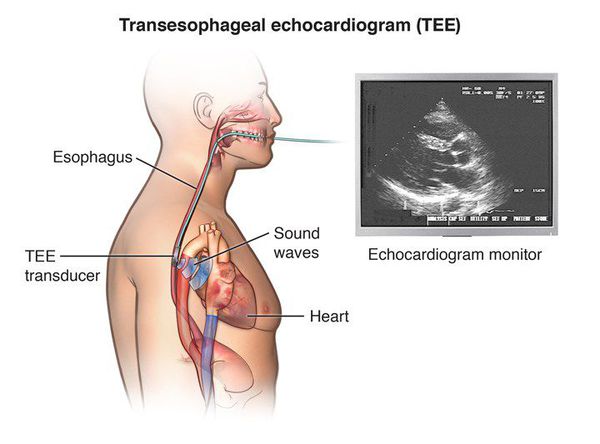
Экстрасистолия что это такое симптомы и лечение у взрослых
Экстрасистолия – самый распространенный вид аритмии
Андрей Леонидович
Провизор
Экстрасистолия – один из самых распространенных вариантов аритмии, сопровождающихся внеочередными сокращениями всей мышцы миокарда или ее отдельных частей экстрасистол. Патология является следствием нарушения механизма прохождения электрического импульса от синусового узла к желудочкам сердца. Характерные симптомы расстройства: ощущение интенсивных сердечных ударов, чувство замирания сердца, страх, тревожность, одышка. При наличии подозрительной симптоматики необходимо записаться на консультацию к кардиологу, который будет заниматься диагностикой и лечением заболевания.
Общая информация
Считается, что с этой разновидностью аритмии в некоторые периоды жизни сталкивается практически каждый человек. Единичные, нерегулярные экстрасистолы могут возникать у абсолютно здоровых мужчин и женщин. В возрасте 50-55 лет нарушение регистрируется у 70-85% пациентов.
Экстрасистолия: группы риска
При отсутствии органических патологий мышцы миокарда экстрасистолы не представляют угрозы для здоровья и жизни человека. Любые органические повреждения существенно увеличивают риски летального исхода от опасных желудочных аритмий.
Причины развития
Функциональные экстрасистолии, периодически беспокоящие практически здоровых людей без каких-либо причин, считаются идиопатическими. В основе функциональных расстройств лежат сбои нейро- и психогенного характера, основные причины которых:
Нарушения и состояния, на фоне которых может возникнуть функциональная экстрасистолия:
Экстрасистолия может возникать в период критических дней у женщин. Расстройство сердечного ритма в таких ситуациях может быть обусловлено следующими факторами:
Патологическая экстрасистолия возникает в результате поражения миокарда при таких болезнях:
Токсические экстрасистолии могут быть следствием:
Симптомы
Клиника заболевания, как правило, основывается на субъективных ощущениях и характеризуется следующими симптомами:
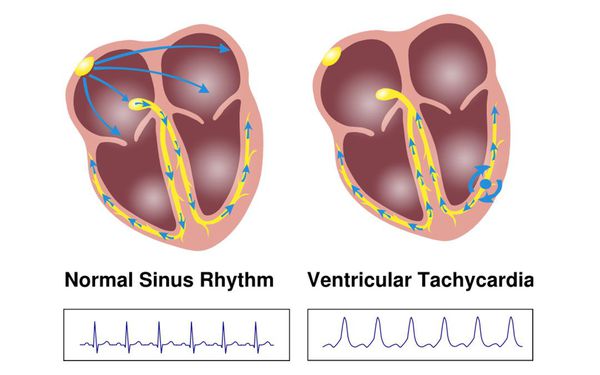
Главная опасность экстрасистолии заключается в том, что она может трансформироваться в более опасные нарушения ритма, такие как:
Частые приступы экстрасистолии становятся причиной развития хронической недостаточности коронарного, церебрального, почечного кровообращения. Поэтому при наличии подозрительных симптомов необходимо как можно скорее попасть на консультацию к кардиологу.
Диагностика
Пациентам с подозрением на экстрасистолию дается направление на следующие диагностические процедуры:
Лечение экстрасистолии
Экстрасистолы, не связанные с кардиальными патологиями и не влияющие на качество жизни пациента, не требуют специального лечения. Пациент остается под наблюдением врача-кардиолога, периодически проходит профилактический осмотр.
Если экстрасистолия возникла на фоне заболеваний сердечной мышцы, эндокринной, пищеварительной системы, в первую очередь приступают к лечению основной патологии. Лечение экстрасистолии нейрогенной природы осуществляется под совместным наблюдением врача кардиолога и невролога. Назначаются препараты, обладающие седативным эффектом и способствующие нормализации работы ЦНС:
Экстрасистолии, возникшие на фоне неконтролируемого употребления некоторых групп лекарственных средств требуют их немедленной отмены.
Если суточное количество экстрасистол превышает 200, а также у пациентов присутствуют кардиальные патологии и субъективные жалобы, назначаются антиаритмические препараты:
Если в течение 2-х месяцев зафиксировано урежение или полное исчезновение экстрасистол, доза препарата постепенно снижается до полной отмены. В остальных случаях антиаритмики придется принимать пожизненно.
Все лекарства, доступные к продаже в аптеках Вашего города, а также цены на них, Вы можете увидеть на нашем сайте, введя в поисковой строке название лекарства и запустив поиск.
Что такое желудочковая экстрасистолия? Причины возникновения, диагностику и методы лечения разберем в статье доктора Колесниченко Ирины Вячеславовны, кардиолога со стажем в 24 года.
Определение болезни. Причины заболевания
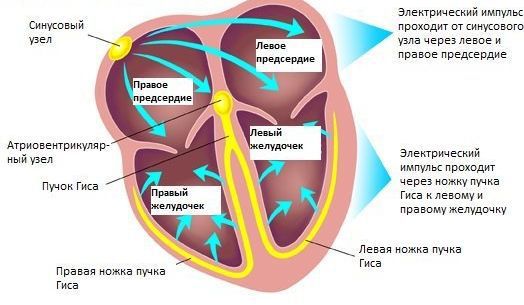
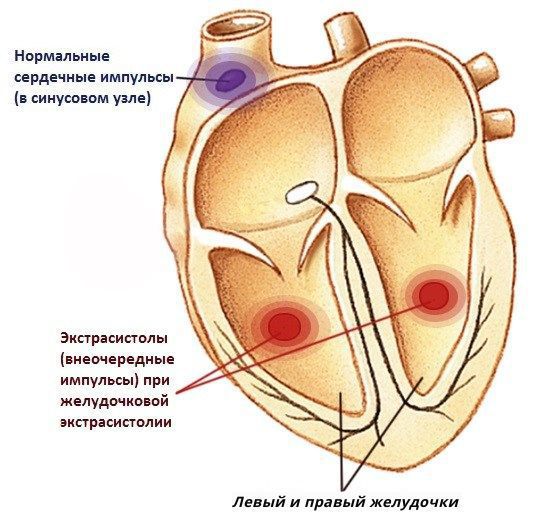
В норме сердце работает упорядоченно благодаря главному водителю ритма, который называется синусовым узлом. Иногда в сердце возникает неправильная (эктопическая) активность не из синусового узла, а из нижележащих отделов проводящей системы сердца, способных самостоятельно создавать электрические импульсы. Такая активность нарушает правильный сердечный ритм, именно это явление названо экстрасистолией.
В зависимости от того, откуда исходит неправильная электрическая активность, внеочередные импульсы (экстрасистолы) бывают наджелудочковыми и желудочковыми. Желудочковая экстрасистолия (ЖЭС) — нарушение сердечного ритма, при котором дополнительный очаг или очаги возбуждения расположены в левом или правом желудочках сердца (ствол пучка Гиса, его разветвление, правая и левая ножки пучка Гиса, волокна Пуркинье).
Причины ЖЭС можно разделись на четыре группы.
2. Некардиальные, связанные с внесердечными заболеваниями.
3. Функциональные, связанные с курением, стрессом, употреблением большого количества кофеина или спиртных напитков. Эти факторы повышают активность симпатико-адреналовой системы и приводят к накоплению катехоламинов (адреналина, норадреналина и др.), которые резко повышают возбудимость миокарда. В данном случае прослеживается чёткая связь с провоцирующим фактором, но органических изменений в сердечной мышце не выявляется.
4. Выделяют также идиопатическую ЖЭС, когда нет связи данной аритмии с заболеваниями или другими факторами.
Симптомы желудочковой экстрасистолии
При желудочковой экстрасистолии пациент обычно жалуется на замирание сердца, перебои в его работе, бултыхания и толчки в области сердца. Могут возникать боли в грудной клетке в атипичном месте, слабость, головокружения. Однако в ряде случаев человек не ощущает аритмию и не предъявляет жалоб.
В зависимости от течения ЖЭС, её причин и сопутствующих заболеваний симптомы могут быть различными.
Кроме этого, нарушение сердечного ритма может вызвать у пациента чувство тревоги, боязнь умереть, а в более тяжёлых случаях — панику.
Жалобы на перебои в работе сердца при экстрасистолии могут быть связаны с действием провоцирующих факторов (курение, алкоголь, чрезмерная физическая нагрузка и пр.) и/или обострением заболевания, ставшего причиной экстрасистолии. Однако симптомы аритмии могут появляться и вне связи с какими-либо провоцирующими факторами.
Патогенез желудочковой экстрасистолии
Формирование экстрасистол (а точнее раз витие активного эктопического очага, вырабатывающего экстрасистолы), происходит из-за разности потенциалов между соседними миокардиальными волокнами или их группами. Разность потенциалов в свою очередь вызвана разбалансированным соотношением симпатических и парасимпатических влияний на миокард (например, при ВСД, возникновении участков некроза сердечной мышцы при инфаркте миокарда, появлении электрической нестабильности в миокарде при его ишемии на фоне хронических форм ИБС).
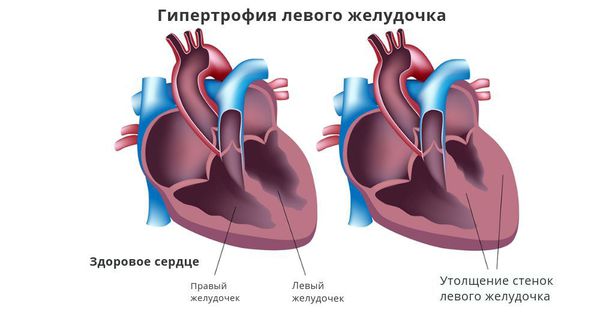
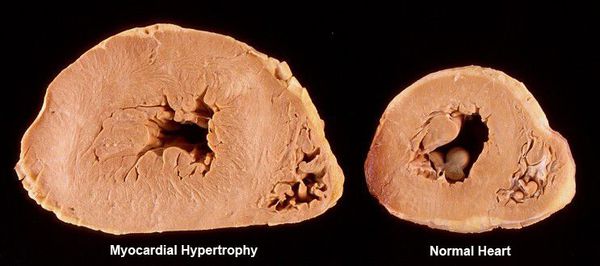
При артериальной гипертензии возникновение и тяжесть желудочковой экстрасистолии обычно чётко взаимосвязано со степенью гипертрофии (утолщением стенок) левого желудочка. Провоцирующим фактором при наличии гипертрофии может стать приём калийсберегающих диуретиков (мочегонных препаратов) без контроля уровня калия в крови.
Если у пациента хроническое лёгочное сердце, экстрасистолия преимущественно будет правожелудочковой. Она отражает хроническую перегрузку правых отделов сердца.
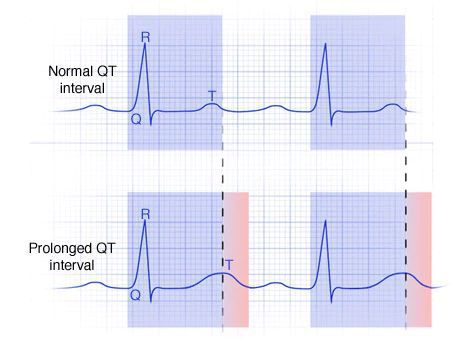
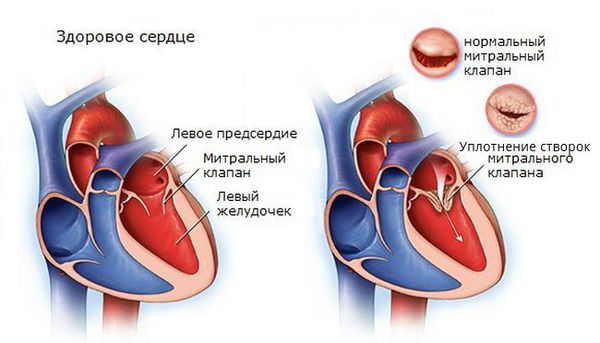
При пролапсе митрального клапана (обычно при наличии удлинённого интервала QT и/или дополнительных хорд) желудочковая экстрасистолия чаще встречается на фоне миксоматозной дегенерации клапана (уплотнения створок митрального клапана) и митральной регургитации (обратного тока крови из левого желудочка в левое предсердие).
Аритмогенное действие лекарств (в первую очередь антиаритмиков IА, IC и III классов) и гипокалиемии реализуется в основном через удлинение интервала QT.
Генетически детерминированные заболевания относят к разряду каналопатий — болезней, обусловленных патологией белка ионных калиевых, реже натриевых каналов (врождённое удлинение интервала QT). Предполагается, что при аритмогенной дисплазии правого желудочка у гетерозиготных детей первичное поражение миокарда происходит в результате воздействия вирусов. В дальнейшем наблюдается прогрессирующее его замещение жировой и фиброзно-жировой тканью. В связи с неблагоприятным прогнозом, связанным с развитием резистентных к лечению аритмий и правожелудочковой недостаточности, таким больным показана трансплантация сердца.
Среди генетических заболеваний выделяют также катехоламининдуцированную триггерную полиморфную желудочковую тахикардию. Её относят к патологиям с первичной электрической нестабильностью миокарда у молодых пациентов без структурного нарушения сердца. Изучаются генетические маркеры заболевания.
Классификация и стадии развития желудочковой экстрасистолии
Классификация желудочковой экстрасистолии очень важна для выбора тактики лечения и определения прогноза заболевания. Экстрасистолы различают по следующим признакам:
По частоте возникновения:
По плотности:
По ритмичности появления одиночные экстрасистолы могут быть по типу бигеминии (каждое второе сокращение является экстрасистолой), тригеминии и квадригеминии (каждый третий и четвертый комплекс является внеочередным).
По расположению в желудочках:
По локализации эктопического очага возбуждения:
J.T. Bigger (1984) предложил прогностическую классификацию аритмий. По степени опасности и риску внезапной смерти он выделил три категории.
Классификация Лауна — Вольфа (она была создана для больных с инфарктом миокарда) построена по морфологическому принципу и отражает нарастание клинической значимости желудочковых экстрасистол:
0 — отсутствие желудочковых экстрасистол;
1 — редкие, монотопные (до 30 в час);
2 — частые, монотопные (более 30 в час);
4А — спаренные; 4Б — залповые (пробежки желудочковой тахикардии из трёх комплексов и более);
Осложнения желудочковой экстрасистолии
Желудочковая экстрасистолия может усугублять основное заболевание сердца, на фоне которого она возникла. Также встречаются и другие осложнения и последствия ЖЭС.
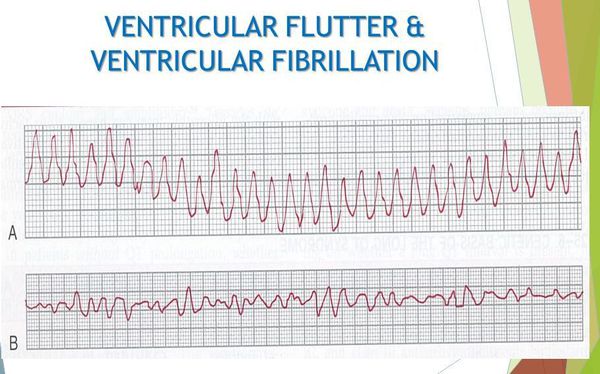
Важно отметить, что у пациентов с желудочковыми экстрасистолиями высоких градаций по классификации Лауна — Вольфа (преимущественно классов 4 и 5), с устойчивыми (более 30 секунд) пароксизмами желудочковой тахикардии возможны такие осложнения, как трепетание и фибрилляция желудочков, которые опасны высоким риском смертельного исхода.
При трепетании желудочки начинают сокращаться с частотой 230-310 ударов в минуту, при фибрилляции сокращение желудочков происходит с частотой 460 ударов в минуту в хаотичном порядке. В этот момент камеры сердца не способны перекачивать кровь, что приводит к недостатку кислорода в головном мозге.
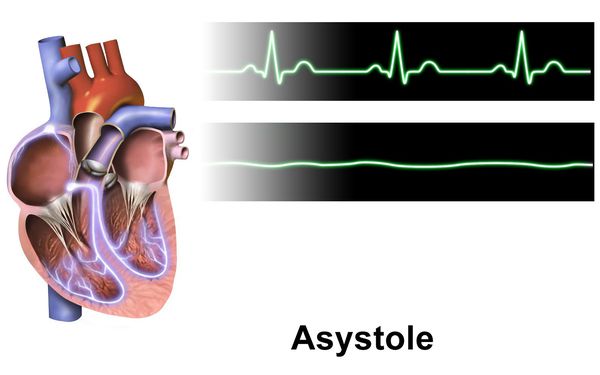
Есть вероятность развития асистолии (остановки сердца), которая может привести к смерти, если вовремя не провести реанимационные действия. Опасность заключается ещё и в том, что асистолия иногда возникает внезапно.
Прогноз жизни этих пациентов крайне неблагоприятен, а их лечение должно ставить своими целями не только устранение тяжёлых пароксизмов, но и продление жизни (вторичная профилактика).
Диагностика желудочковой экстрасистолии
Диагноз желудочковой экстрасистолии подтверждается на основании объективного обследования, данных аускультации (выслушивания) сердца, проведения электрокардиографии (ЭКГ), суточного ЭКГ-мониторирования по Холтеру.
При объективном обследовании обращает на себя внимание выраженная пульсация вен шеи, возникающая при преждевременном сокращении желудочков. Характерной чертой является неравномерный пульс с длинной паузой после внеочередного сокращения сердца. При аускультации можно услышать аритмичные сердечные тоны с изменением звучности I тона (обусловлен звуком закрытия митрального и трикуспидального клапанов и появляется во время сокращения желудочков ), расщеплением II тона ( появляется через короткий промежуток времени после первого во время расслабления сердца, обусловлен закрытием клапанов аорты и лёгочной артерии ). Подтвердить диагноз желудочковой экстрасистолии можно только с помощью инструментальных исследований.
При подозрении на ЖЭС пациенту в первую очередь проводится ЭКГ-исследование, которое позволяет зафиксировать внеочередной комплекс QRS.
Характерные признаки желудочковой экстрасистолы: отсутствие предсердного зубца Р, расширение и деформация самого желудочкового комплекса, противоположное (дискордантное) направление зубца T по отношению к QRS-комплексу, а после него идёт полная компенсаторная пауза (изолиния).
Нужно отметить, что ЭКГ проводится в короткий промежуток времени и не всегда в этот момент возникает внеочередное возбуждение, поэтому данный метод не позволяет выявить проблему в 100 % случаев. Для установления диагноза обязательно должно применяться суточное или более длительное (например, в течение двух суток) мониторирование ЭКГ, которое называется холтеровским (по фамилии автора Нормана Холтера, предложившего эту методику).
После записи и расшифровки специалистом данных ЭКГ-мониторирования становится возможным:
Показанием к проведению чреспищеводной стимуляции сердца (ЧПСС) или электрофизиологического исследования (ЭФИ) может стать необходимость установления механизма и места возникновения экстрастимула (при частой монотопной желудочковой экстрасистолии).
Лечение желудочковой экстрасистолии
После обнаружения у пациента желудочковой экстрасистолии лечение должно быть выбрано с учётом симптомов и наличия опасных видов экстрасистол.
Тактика ведения пациентов с желудочковой экстрасистолией залючается в следующем:
Выделяют несколько основных направлений лечения в зависимости от течения, формы и выраженности ЖЭС.
1. Если у человека нет жалоб, а при исследовании выявляются редкие одиночные мономорфные преждевременные желудочковые комплексы, не вызывающие нарушения гемодинамики, особой терапии не требуется. В этом случае пациенту стоит отказаться от кофеинсодержащих и спиртных напитков, исключить курение, наладить режим дня, обеспечить полноценный сон и отдых. Если есть какие-либо нарушения функций организма, связанные с недостаточной подвижностью, нужно увеличить физическую активность в соответствии с возможностями организма. В то же время необходимо исключить чрезмерные физические нагрузки (поднятие тяжестей, занятия тяжёлой атлетикой). В рацион питания необходимо включать продукты, богатые калием и магнием: они оказывают благоприятное влияние на сердечно-сосудистую систему.
2. При выявлении приступов экстрасистолии, которые со провождаются клинической симптоматикой, но не нарушают гемодинамику и имеют доброкачественное течение, в первую очередь назначают бета-адреноблокаторы («Бисопролол», «Метопролол»). Иногда, особенно при функциональной желудочковой аритмии на фоне вегето-сосудистой дистонии и стрессовых состояний, в комплексном лечении помогают препараты с седативным («Валемидин», «Валериана») и противотревожным действием («Стрезам», «Адаптол»), препараты магния («Магнерот», «Магне В6 форте»). Необходимо подчеркнуть, что количество ЖЭС учитывается при определении степени её злокачественности. Частая (до 1000 и более в сутки) желудочковая экстрасистолия сама по себе, даже при отсутствии очевидного заболевания сердца, является показанием к проведению антиаритмической терапии.
3. При ЖЭС злокачественного характера необходимо назначение высокоэффективных препаратов, таких как «Амиодарон» и «Соталол». Иногда их сочетают с поддерживающими дозами бета-адреноблокаторов. Лечение обычно проводится в условиях стационара, под контролем ЭКГ. В стационаре больше возможностей, чтобы скорректировать гемодинамику и значительно уменьшить риск летального исхода у больных с нарушениями ритма сердца.
Антиаритмики I класса не следует принимать, если у больного имеются следующие патологии:
Практически важным является вопрос о длительности антиаритмической терапии. У пациентов со злокачественными желудочковыми аритмиями терапия антиаритмиками должна проводится неопределённо долго, в большинстве случаев пожизненно. При менее злокачественных нарушениях ритма лечение должно продолжаться до нескольких месяцев с возможностью постепенной (ввиду опасности синдрома «рикошета») его отмены. После прекращения постоянной терапии больному даются рекомендации всегда носить с собой успешно использованный антиаритмик и принимать его в случае возобновления перебоев в работе сердца.
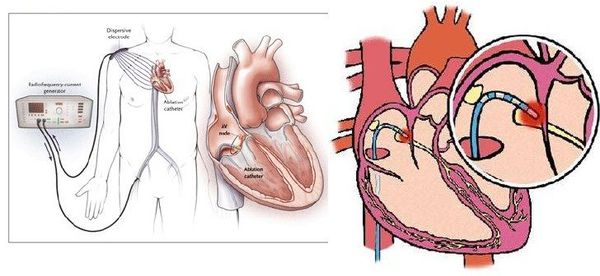
4. При желудочковой экстрасистолии возможно хирургическое лечение. Показанием к оперативному вмешательству являются:
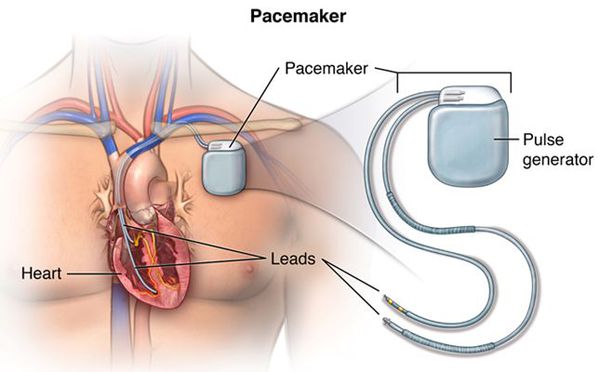
Возможна также установка элктрокардиостимулятора (ЭКС). ЭКС представляет собой устройство с электродами, которые в ходе операции крепятся к желудочку и предсердию. Электроды создают электронные импульсы, заставляющие миокард сокращаться. Кардиостимулятор, по сути, заменяет синусовый узел, отвечающий за ритмичность. Он избавляет человека от экстрасистолии и позволяет вернуться к полноценной жизни.
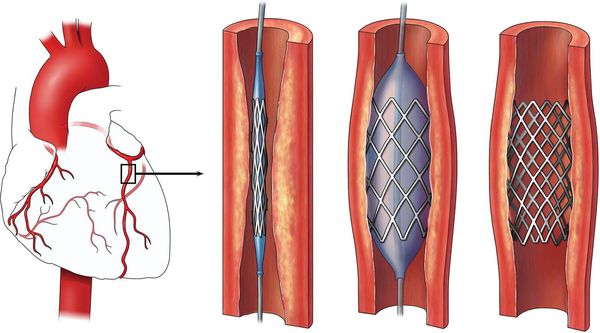
При острой и хронической ишемической болезни сердца развитие желудочковой аритмии напрямую связано с ишемией миокарда. В связи с этим хирургическая реваскуляризация миокарда (стентирование, аорто-коронарное шунтирование) может улучшить электрическую стабильность и снизить вероятность развития желудочковых нарушений ритма.
У больных с высокой вероятностью внезапной смерти и застойной сердечной недостаточностью главным методом лечения остается пересадка сердца.
Прогноз. Профилактика
На прогноз течения желудочковой экстрасистолии влияет её форма, наличие морфологической патологии тканей сердца и нарушений гемодинамики.
Функциональные и идиопатические единичные несвоевременные сокращения миокарда не угрожают здоровью и жизни человека. Как правило, больные с доброкачественным течением желудочковой экстрасистолии без органических патологий сердца живут долго.
Частая полиморфная ЖЭС, которая развивается на фоне органического поражения сердца, при отсутствии лечения может вызвать сердечную недостаточность и привести к внезапному летальному исходу. Этот вид желудочковой экстрасистолии представляет угрозу для жизни человека. Именно поэтому всем пациентам с признаками нарушения сердечного ритма необходимо вовремя прийти к специалисту. Также важно периодически проходить профилактический осмотр у кардиолога с целью выявления заболевания на ранней стадии.
Для профилактики желудочковой экстрасистолии рекомендуется проводить следующие мероприятия:
ЭКСТРАСИСТОЛИЯ: клиническое значение, диагностика и лечение
Экстрасистолами называют преждевременные комплексы (преждевременные сокращения), выявляемые на ЭКГ. По механизму возникновения преждевременные комплексы подразделяются на экстрасистолы и парасистолы. Различия между экстрасистолией и парасистолией являютс
Экстрасистолами называют преждевременные комплексы (преждевременные сокращения), выявляемые на ЭКГ. По механизму возникновения преждевременные комплексы подразделяются на экстрасистолы и парасистолы. Различия между экстрасистолией и парасистолией являются чисто электрокардиографическими или электрофизиологическими. Клиническое значение и лечебные мероприятия при экстрасистолии и парасистолии абсолютно одинаковы. По локализации источника аритмии электросистолы разделяют на наджелудочковые и желудочковые.
Экстрасистолы, несомненно, являются самым распространенным нарушением ритма сердца. Они часто регистрируются и у здоровых лиц. При проведении суточного мониторирования ЭКГ статистической «нормой» экстрасистол считается примерно до 200 наджелудочковых экстрасистол и до 200 желудочковых экстрасистол в сутки. Экстрасистолы могут быть одиночными или парными. Три и более экстрасистолы подряд принято называть тахикардией («пробежки» тахикардии, «короткие эпизоды неустойчивой тахикардии»). Неустойчивой тахикардией называют эпизоды тахикардии продолжительностью менее 30 с. Иногда для обозначения 3–5 экстрасистол подряд используют определение «групповые», или «залповые», экстрасистолы. Очень частые экстрасистолы, особенно парные и рецидивирующие «пробежки» неустойчивой тахикардии, могут достигать степени непрерывно-рецидивирующей тахикардии, при которой от 50 до 90% сокращений в течение суток составляют эктопические комплексы, а синусовые сокращения регистрируются в виде единичных комплексов или коротких кратковременных эпизодов синусового ритма.
В практической работе и научных исследованиях основное внимание уделяют желудочковой экстрасистолии. Одной из наиболее известных классификаций желудочковых аритмий является классификация B. Lown и M. Wolf (1971).
Предполагалось, что высокие градации экстрасистол (классы 3–5) являются наиболее опасными. Однако в дальнейших исследованиях было установлено, что клиническое и прогностическое значение экстрасистолии (и парасистолии) практически целиком определяется характером основного заболевания, степенью органического поражения сердца и функциональным состоянием миокарда. У лиц без признаков поражения миокарда с нормальной сократительной функцией левого желудочка (фракция выброса больше 50%) экстрасистолия, включая эпизоды неустойчивой желудочковой тахикардии и даже непрерывно-рецидивирующей тахикардии, не влияет на прогноз и не представляет опасности для жизни. Аритмии у лиц без признаков органического поражения сердца называют идиопатическими. У больных с органическим поражением миокарда (постинфарктный кардиосклероз, дилатация и/или гипертрофия левого желудочка) наличие экстрасистолии считается дополнительным прогностически неблагоприятным признаком. Но даже в этих случаях экстрасистолы не имеют самостоятельного прогностического значения, а являются отражением поражения миокарда и дисфункции левого желудочка.
В 1983 г J. T. Bigger предложил прогностическую классификацию желудочковых аритмий.
Однако, как было отмечено, независимого прогностического значения желудочковая экстрасистолия не имеет. Сами по себе экстрасистолы в большинстве случаев безопасны. Экстрасистолию даже называют «косметической» аритмией, подчеркивая этим ее безопасность. Даже «пробежки» неустойчивой желудочковой тахикардии тоже относят к «косметическим» аритмиям и называют «энтузиастическими выскальзывающими ритмами» (R. W. Campbell, K. Nimkhedar, 1990). В любом случае лечение экстрасистолии с помощью антиаритмических препаратов (ААП) не улучшает прогноз. В нескольких крупных контролируемых клинических исследованиях было выявлено заметное повышение общей смертности и частоты внезапной смерти (в 2–3 раза и более) у больных с органическим поражением сердца на фоне приема ААП класса I, несмотря на эффективное устранение экстрасистол и эпизодов желудочковой тахикардии. Наиболее известным исследованием, в котором впервые было выявлено несоответствие клинической эффективности препаратов и их влияния на прогноз, является исследование CAST. В исследовании CAST («исследование подавления аритмий сердца») у больных, перенесших инфаркт миокарда, на фоне эффективного устранения желудочковой экстрасистолии препаратами класса I С (флекаинид, энкаинид и морицизин) выявлено достоверное увеличение общей смертности в 2,5 раза и частоты внезапной смерти в 3,6 раза по сравнению с больными, принимавшими плацебо. Результаты исследования заставили пересмотреть тактику лечения не только пациентов с нарушениями ритма, но и кардиологических больных вообще. Исследование CAST является одним из основных в становлении «медицины, основанной на доказательствах». Только на фоне приема β- адреноблокаторов и амиодарона отмечено снижение смертности больных с постинфарктным кардиосклерозом, сердечной недостаточностью или реанимированных пациентов. Однако положительное влияние амиодарона и особенно β-адреноблокаторов не зависело от антиаритмического действия этих препаратов.
Выявление экстрасистолии (как и любого другого варианта нарушений ритма) является поводом для обследования, направленного прежде всего на выявление возможной причины аритмии, заболевания сердца или экстракардиальной патологии и определения функционального состояния миокарда.
ААП не излечивают от аритмии, а только устраняют ее на период приема препаратов. При этом побочные реакции и осложнения, связанные с приемом практически всех препаратов, могут быть гораздо более неприятными и опасными, чем экстрасистолия. Таким образом, само по себе наличие экстрасистолии (независимо от частоты и «градации») не является показанием для назначения ААП. Бессимптомные или малосимптомные экстрасистолы не требуют проведения специального лечения. Таким больным показано диспансерное наблюдение с проведением эхокардиографии примерно 2 раза в год для выявления возможных структурных изменений и ухудшения функционального состояния левого желудочка. Л. М. Макаров и О. В. Горлицкая (2003) при длительном наблюдении за 540 больными с идиопатической частой экстрасистолией (более 350 экстрасистол в час и более 5000 в сутки) выявили у 20% больных увеличение полостей сердца («аритмогенная кардиомиопатия»). Причем более часто увеличение полостей сердца отмечалось при наличии предсердной экстрасистолии.
Показания для лечения экстрасистолии:
Лечение экстрасистолии
Необходимо объяснить больному, что малосимптомная экстрасистолия безопасна, а прием антиаритмических препаратов может сопровождаться неприятными побочными эффектами или даже вызвать опасные осложнения. Прежде всего необходимо устранить все потенциально аритмогенные факторы: алкоголь, курение, крепкий чай, кофе, прием симпатомиметических препаратов, психоэмоциональное напряжение. Следует немедленно приступить к соблюдению всех правил здорового образа жизни.
При наличии показаний для назначения ААП у больных с органическим поражением сердца используют β-адреноблокаторы, амиодарон и соталол. У больных без признаков органического поражения сердца, кроме этих препаратов, применяют ААП класса I: Этацизин, Аллапинин, Пропафенон, Кинидин Дурулес. Этацизин назначают по 50 мг 3 раза в день, Аллапинин — по 25 мг 3 раза в день, Пропафенон — по 150 мг 3 раза в день, Кинидин Дурулес — по 200 мг 2–3 раза в день.
Лечение экстрасистолии проводят методом проб и ошибок, последовательно (по 3–4 дня) оценивая эффект приема антиаритмических препаратов в средних суточных дозах (с учетом противопоказаний), выбирая наиболее подходящий для данного больного. Для оценки антиаритмического эффекта амиодарона может потребоваться несколько недель или даже месяцев (применение более высоких доз амиодарона, например по 1200 мг/сут, может сократить этот период до нескольких дней).
Эффективность амиодарона в подавлении желудочковых экстрасистол составляет 90–95%, соталола — 75%, препаратов класса I C — от 75 до 80% (B. N. Singh, 1993).
Критерий эффективности ААП — исчезновение ощущения перебоев, улучшение самочувствия. Многие кардиологи предпочитают начинать подбор препаратов с назначения β-адреноблокаторов. У больных с органическим поражением сердца при отсутствии эффекта от β-адреноблокаторов применяют Амиодарон, в том числе в комбинации с первыми. У больных с экстрасистолией на фоне брадикардии подбор лечения начинают с назначения препаратов, ускоряющих ЧСС: можно попробовать прием пиндолола (Вискен), эуфиллина (Теопек) или препаратов класса I (Этацизин, Аллапинин, Кинидин Дурулес). Назначение холинолитических препаратов типа белладонны или симпатомиметиков менее эффективно и сопровождается многочисленными побочными явлениями.
В случае неэффективности монотерапии оценивают эффект комбинаций различных ААП в уменьшенных дозах. Особенно популярны комбинации ААП с β-адреноблокаторами или амиодароном.
Есть данные, что одновременное назначение β-адреноблокаторов (и амиодарона) нейтрализует повышенный риск от приема любых антиаритмических средств. В исследовании CAST у больных, перенесших инфаркт миокарда, которые наряду с препаратами класса I C принимали β-адреноблокаторы не было отмечено увеличения смертности. Более того, было выявлено снижение частоты аритмической смерти на 33%!
Особенно эффективна комбинация β-адреноблокаторов и амиодарона. На фоне приема такой комбинации наблюдалось еще большее снижение смертности, чем от каждого препарата в отдельности. Если ЧСС превышает 70–80 уд./мин в покое и интервал P–Q в пределах 0,2 с, то проблемы с одновременным назначением амиодарона и β-адреноблокаторов нет. В случае брадикардии или АВ-блокады I–II степени для назначения амиодарона, β-адреноблокаторов и их комбинации необходима имплантация кардиостимулятора, функционирующего в режиме DDD (DDDR). Есть сообщения о повышении эффективности антиаритмической терапии при сочетании ААП с ингибиторами АПФ, блокаторами рецепторов ангиотензина, статинами и препаратами омега-3-ненасыщенных жирных кислот.
Некоторые противоречия существуют в отношении применения амиодарона. С одной стороны, некоторые кардиологи назначают амиодарон в последнюю очередь — только при отсутствии эффекта от других препаратов (считая, что амиодарон довольно часто вызывает побочные явления и требует длительного «периода насыщения»). С другой стороны, возможно, более рационально начинать подбор терапии именно с амиодарона как наиболее эффективного и удобного для приема препарата. Амиодарон в малых поддерживающих дозах (100–200 мг в день) редко вызывает серьезные побочные явления или осложнения и является скорее даже более безопасным и лучше переносимым, чем большинство других антиаритмических препаратов. В любом случае при наличии органического поражения сердца выбор небольшой: β-адреноблокаторы, амиодарон или соталол. При отсутствии эффекта от приема амиодарона (после «периода насыщения» — как минимум по 600–1000 мг/сут в течение 10 дней) можно продолжить его прием в поддерживающей дозе — 0,2 г/сут и, при необходимости, оценить эффект последовательного добавления препаратов класса I С (Этацизин, Пропафенон, Аллапинин) в половинных дозах.
У больных с сердечной недостаточностью заметное уменьшение количества экстрасистол может отмечаться на фоне приема ингибиторов АПФ и Верошпирона.
Следует отметить, что проведение суточного мониторирования ЭКГ для оценки эффективности антиаритмической терапии утратило свое значение, так как степень подавления экстрасистол не влияет на прогноз. В исследовании CAST выраженное увеличение смертности отмечено на фоне достижения всех критериев полного антиаритмического эффекта: уменьшения общего количества экстрасистол более чем на 50%, парных экстрасистол — не менее чем на 90% и полное устранение эпизодов желудочковой тахикардии. Основным критерием эффективности лечения является улучшение самочувствия. Это обычно совпадает с уменьшением количества экстрасистол, а определение степени подавления экстрасистолии не имеет значения.
В целом последовательность подбора ААП у больных с органическим заболеванием сердца, при лечении рецидивирующих аритмий, включая экстрасистолию, можно представить в следующем виде.
У больных без признаков органического поражения сердца можно использовать любые препараты, в любой последовательности или использовать схему, предложенную для больных с органическим заболеванием сердца.
Краткая характеристика ААП
β-адреноблокаторы. После исследования CAST и опубликования результатов метаанализа исследований по применению ААП класса I, в котором было показано, что практически все ААП класса I способны увеличивать смертность у больных с органическим поражением сердца, β-адреноблокаторы стали самыми популярными антиаритмическими препаратами.
Антиаритмический эффект β-адреноблокаторов обусловлен именно блокадой β-адренергических рецепторов, т. е. уменьшением симпатико-адреналовых влияний на сердце. Поэтому β-адреноблокаторы наиболее эффективны при аритмиях, связанных с симпатико-адреналовыми влияниями — так называемые «катехоламинзависимые» или «адренергические аритмии». Возникновение таких аритмий, как правило, связано с физической нагрузкой или психоэмоциональным напряжением.
Катехоламинзависимые аритмии в большинстве случаев одновременно являются «тахизависимыми», т. е. возникают при достижении определенной критической частоты сердечных сокращений, например во время физической нагрузки частая желудочковая экстрасистолия или желудочковая тахикардия возникают только при достижении частоты синусового ритма 130 сокращений в минуту. На фоне приема достаточной дозы β-адреноблокаторов больной не сможет достичь частоты 130 уд./мин при любом уровне физической нагрузки, таким образом предотвращается возникновение желудочковых аритмий.
β-адреноблокаторы являются препаратами выбора для лечения аритмий при врожденных синдромах удлинения интервала Q–T.
При аритмиях, не связанных с активацией симпатической нервной системы β-адреноблокаторы гораздо менее эффективны, но добавление β-адреноблокаторов нередко значительно увеличивает эффективность других антиаритмических препаратов и снижает риск аритмогенного эффекта ААП класса I. Препараты класса I в сочетании с β-адреноблокаторами не увеличивают смертность у больных с им поражением сердца (исследование CAST).
При так называемых «вагусных» аритмиях β-адреноблокаторы оказывают аритмогенное действие. «Вагусные» аритмии возникают в состоянии покоя, после еды, во время сна, на фоне урежения ЧСС («брадизависимые» аритмии). Вместе с тем в некоторых случаях при брадизависимых аритмиях эффективно применение пиндолола (Вискен) — β-адреноблокатора с внутренней симпатомиметической активностью (ВСА). Кроме пиндолола к β-адреноблокаторам с ВСА относятся окспренолол (Тразикор) и ацебутолол (Сектраль), однако в максимальной степени внутренняя симпатомиметическая активность выражена именно у пиндолола.
Дозы β-адреноблокаторов регулируют в соответствии с антиаритмическим эффектом. Дополнительным критерием достаточной β-блокады является снижение ЧСС до 50 уд./мин в состоянии покоя. В прежние годы, когда основным β-адреноблокатором был пропранолол (Анаприлин, Обзидан), известны случаи эффективного применения пропранолола при желудочковых аритмиях в дозах до 960 мг/сут и более, например до 4 г в день! (R. L. Woosley et al., 1979).
Амиодарон. Амиодарон таблетки 0,2 г. (оригинальным препаратом является Кордарон) обладает свойствами всех четырех классов ААП и, кроме того, оказывает умеренное a-блокирующее действие. Амиодарон, несомненно, является самым эффективным из существующих антиаритмических препаратов. Его даже называют «аритмолитическим препаратом».
Основным недостатком амиодарона является высокая частота экстракардиальных побочных эффектов, которые при длительном приеме наблюдаются у 10–75% больных. Однако необходимость в отмене амиодарона возникает у 5–25% (J. A. Johus et al., 1984; J. F. Best et al., 1986; W. M. Smith et al., 1986). К основным побочным эффектам амиодарона относятся: фотосенсибилизация, изменение цвета кожи, нарушение функции щитовидной железы (как гипотиреоз, так и гипертиреоз), повышение активности печеночных трансаминаз, периферические нейропатии, мышечная слабость, тремор, атаксия, нарушения зрения. Большинство этих побочных эффектов обратимы и исчезают после отмены или при уменьшении дозы амиодарона. Гипотиреоз можно контролировать с помощью приема левотироксина. Наиболее опасным побочным эффектом амиодарона является поражение легких («амиодароновое поражение легких») — возникновение интерстициального пневмонита или, реже, легочного фиброза. У большинства больных поражение легких развивается только при длительном приеме сравнительно больших поддерживающих доз амиодарона — более 400 мг/сут. Такие дозы крайне редко применяют в России. Поддерживающая доза амиодарона в России обычно составляет 200 мг/сут или даже меньше (по 200 мг в день 5 дней в неделю). B. Clarke и соавторы (1985) сообщают лишь о трех случаях из 48 наблюдений возникновения этого осложнения на фоне приема амиодарона в дозе 200 мг в сутки.
В настоящее время изучается эффективность дронедарона, деривата амиодарона без йода. Предварительные данные свидетельствуют об отсутствии экстракардиальных побочных эффектов у дронедарона.
Соталол. Соталол (Соталекс, Сотагексал) таблетки 160 мг применяется в средней суточной дозе 240–320 мг. Начинают с назначения 80 мг 2 раза в день. При рефрактерных аритмиях иногда используют прием соталола до 640 мг/сут. β-адреноблокирующее действие соталола проявляется начиная с дозы 25 мг.
На фоне приема соталола имеется повышенный риск развития желудочковой тахикардии типа «пируэт». Поэтому прием соталола желательно начинать в стационаре. При назначении соталола необходимо тщательно контролировать величину интервала Q–T, особенно в первые 3 дня. Корригированный интервал Q–T не должен превышать 0,5 с. В этих случаях риск развития тахикардии типа «пируэт» менее 2%. С увеличением дозы соталола и степени удлинения интервала Q–T значительно увеличивается риск развития тахикардии типа «пируэт». Если корригированный интервал Q–T превышает 0,55 с — риск тахикардии типа «пируэт» достигает 11%. Поэтому при удлинении интервала Q–T до 0,5 с необходимо уменьшить дозу соталола или отменить препарат.
Побочные эффекты соталола соответствуют типичным побочным эффектам β-адреноблокаторов.
Этацизин. Этацизин таблетки 50 мг. Наиболее изученный отечественный препарат (создан в СССР). Для лечения аритмий применяется с 1982 г. Быстрое достижение клинического эффекта позволяет с успехом использовать Этацизин у лиц без органического поражения сердца для лечения желудочковых и наджелудочковых нарушений ритма: экстрасистолии, всех вариантов пароксизмальных и хронических тахиаритмий, в том числе мерцательной аритмии, при синдроме Вольфа–Паркинсона–Уайта. Наиболее эффективен Этацизин у пациентов с ночными аритмиями, а также при желудочковой экстрасистолии.Средняя суточная доза Этацизина составляет 150 мг (по 50 мг 3 раза в день). Максимальная суточная доза — 250 мг. При назначении этацизина для предупреждения рецидивирования мерцательной аритмии, наджелудочковых и желудочковых тахикардий его эффективность, как правило, превосходит эффективность других АПП класса I. Препарат хорошо переносится, необходимость в отмене возникает примерно у 4% больных. Основные побочные эффекты: головокружение, головная боль, «онемение» языка, нарушение фиксации взора. Обычно побочные реакции наблюдаются сравнительно редко, и их выраженность уменьшается после первой недели приема Этацизина.
Аллапинин. Отечественный препарат Аллапинин, таблетки 25 мг (создан также в СССР) применяется в клинической практике с 1986 г. Назначают по 25–50 мг 3 раза в день. Максимальная суточная доза составляет 300 мг. Аллапинин довольно эффективен при наджелудочковых и желудочковых аритмиях. Основные побочные явления — головокружение, головная боль, нарушение фиксации взора. Необходимость в отмене возникает примерно у 6% больных. Одной из особенностей аллапинина и теоретически его недостатком является наличие β-адреностимулирующего действия.
Пропафенон (Ритмонорм, Пропанорм), таблетки 150 мг, ампулы 10 мл (35 мг). Назначают по 150–300 мг 3 раза в день. При необходимости дозу увеличивают до 1200 мг/сут. Пропафенон, кроме замедления проведения, слегка удлиняет рефрактерные периоды во всех отделах сердца. Кроме того, пропафенон обладает небольшим β-адреноблокирующим действием и свойствами антагонистов кальция.
К основным побочным эффектам пропафенона относятся головокружение, нарушение фиксации взора, атаксия, тошнота, металлический вкус во рту.
Хинидин. В настоящее время в России используют в основном Кинидин Дурулес, табл. по 0,2 г. Разовая доза составляет 0,2–0,4 г, средняя суточная доза — от 0,6 до 1,0 г. Максимальная суточная доза хинидина в прежние годы (когда хинидин был основным антиаритмическим препаратом) достигала 4,0 г! В настоящее время такие дозы не используются и примерной максимальной суточной дозой хинидина можно считать 1,6 г.
В небольших дозах (600–800 мг/сут) хинидин хорошо переносится. Побочные явления возникают обычно при более высоких дозах. К наиболее частым побочным эффектам при приеме хинидина относятся нарушения функции желудочно-кишечного тракта: тошнота, рвота, понос. Реже отмечаются головная боль, головокружения, ортостатическая гипотония. Самое опасное осложнение от приема хинидина — возникновение желудочковой тахикардии типа «пируэт». По данным литературы, это осложнение наблюдается у 1–3% больных, принимающих хинидин.
П. Х. Джанашия, доктор медицинских наук, профессор
С. В. Шлык, доктор медицинских наук, профессор
Н. М. Шевченко, доктор медицинских наук, профессор
РГМУ, Москва