Экзогенная гипертриглицеридемия что это такое
Гипертриглицеридемия: этиология, патогенез, диагностика
Т.В. Чепетова, А.Н. Мешков.
ФГУ Российский кардиологический научно-производственный комплекс Росздрава, Москва
Цель обзора – дать современные представления об этиологии и патогенезе гипертриглицеридемии, а так же ее причинной роли в развитии ряда заболеваний. В обзоре приведены данные об обмене триглицеридов в норме, об основных причинах гипертриглицеридемии, ее клиническом значении и диагностических подходах у пациентов с этим нарушением. Гипертриглицеридемия, несмотря на важную роль в развитии атеросклероза, панкреатита, болезни Альцгеймера, преэклампсии, остается мало освещенной проблемой для практикующего врача.
Ключевые слова: гипертриглицеридемия, гиперхолестеринемия, диагностика, атеросклероз, ИБС.
Key words: hypertriglyceridemia, hypercholesterolemia, diagnostica, atherosclerosis,CHD.
Введение
Помимо этого, гипертриглицеридемия (ГТГ) ассоциируется с рядом других заболеваний, таких как болезнь Альцгеймера, артериальная гипертония, панкреатит, преэклампсия [7,8,9].
В повседневной клинической практике врачи (кардиологи, терапевты, хирурги и др.) сталкиваются с тем или иным видом нарушений липидного обмена. Однако, если гиперхолестеринемия довольно хорошо освещена в литературе, то теме гипертриглицеридемии уделено меньше внимания. Настоящий обзор ставит своей целью дать современные представления об этиологии, патогенезе и клинической диагностике различных форм гипертриглицеридемии.
Метаболизм триглицеридов
В метаболизме триглицеридов можно условно выделить два пути: экзогенный и эндогенный [1,3]. Экзогенный путь: На начальном этапе жир, поступающий с пищей и подвергщийся процессам пищеварения в кишечнике, поступает в виде b-моноглицеридов, a-моноглицеридов, глицерина и жирных кислот в энтероциты посредством мицеллярной диффузии. В энтероцитах происходит ресинтез из этих компонентов эндогенных триглицеридов и фосфолипидов. Холестерин попадает в энтероцит путем как простой диффузии, так и активным транспортом с участием белков транспортеров семейства АВС. В энтероцитах также синтезируются апобелки (апо В48, апо АI, апо АII, апо АIV). Все эти компоненты, соединяясь в цистернах ГЭР (гладкоэндоплазиатического ретикулума), образуют хиломикроны [3,10,11].
Хилимикроны секретируются в кровоток, где транспортируют жирные кислоты, триглицериды, фосфолипиды к периферическим тканям (преимущественно сердечная и скелетная мускулатура, жировая ткань, молочные железы) [12]. В результате контакта хилимикрон со стенкой капилляров периферических тканей и гидролиза под действием липопротеинлипазы, находящейся на эндотелии сосудов, происходит образование ремнант хиломикрон с освобождением свободных жирных кислот, которые в свою очередь захватываются CD36 рецепторами периферических тканей [13]. Следует отметить, что для активации ЛПЛ необходимо участие апо СII, в то время как апо СIII выступает в качестве ингибитора липопротеинлипазы [14].
Эндогенный путь условно начинается с трансформации метаболитов в печени и ресинтезе из триглицеридов, фосфолипидов, холестерина, а также апо В 100, апо Е, апо СII ЛПОНП, которые секретируются в кровоток [1,3]. В кровеном русле в результате контакта с эндотелием сосудов под действием CETP-cholesteryl ester transfer protein(фермента, переносящего эфиры холестерина), PLTP- phospholipid transfer protein (фермента, переносящего фосфолипиды) и частичного действия липопротеинлипазы ЛПОНП превращаются в ЛППП, а затем под действием печеночной липазы в малой плотности ЛПНП. ЛППП и ЛПНП, богатые ХС, подвергаются захвату периферическими тканями через ЛПНП-рецептор [13].
Поверхностные фосфолипиды и протеины, которые образуются в результате гидролиза ХМ и ЛПОНП, переходят в антиатерогенный пул ЛПВП, бедный липидами и обогащенный апо АI, синтезирующийся печенью и слизистой кишечника [16]. ЛПВП забирают свободный ХС из тканей и макрофагов с помощью АВС-А1 транспортера, а плазменный ЛХАТ (лецитин-холестерол-ацилтрансфераза) превращает свободный ХС в эстерифицированный. ЛПВП захватываются SR-BI рецепторами печени [17].
Помимо основного участия в катаболизме триглицеридов ЛПЛ обладает некоторыми другими функциями, в частности, она способствует взаимодействию липопротеинов с эндотелиальной поверхностью, тем самым увеличивая захват атерогенных ремнантных частиц в печени [18]. Кроме того, показано, что увеличение уровней апо-С III—ингибитора активности как ЛПЛ, так и гидролиза хиломикрон и ЛПОНП, связано с повышением ЛПОНП и уменьшением их фракционного катаболизма, что приводит к развитию гипертриглицеридемии [14].
Патофизиологическая основа атерогенной природы триглицеридов.
Гипертриглицеридемия может влиять на развитие ИБС несколькими путями. Во-первых, ХМ, ЛПОНП и их ремнанты могут играть прямую роль в атерогенном процессе: связывание липопротеинов, обогащенных триглицеридами, с эндотелием стенок артерий происходит одновременно с их гидролизом под действием ЛПЛ с образованием ремнант, которые могут пенетрировать сосудистую стенку и поглощаться макрофагами и гладкомышечными клетками, а высвобождающиеся из них СЖК имеют прямое повреждающее действие на эндотелий [10,11,13].Важно, что ЛПЛ, которая в норме усиливает метаболизм триглицеридов в мышцах и жировой ткани, может также обладать проатерогенным действием. Кроме того, сами макрофаги продуцируют ЛПЛ, которая может увеличивать их эндоцитоз сосудистой стенкой, однако, точные механизмы остаются неясными [18]. Во-вторых, увеличение ХМ и/или ЛПОНП стимулирует CETP-опосредованную эстерификацию ХС, в связи с чем ЛППП и ЛПНП будут больше доставлять ХС в сосудистую стенку[16,17].Кроме того, показано, что увеличение ЛПОНП сопровождается повышением секреции в плазму апоВ и может приводить к повышению ЛПНП и уменьшению ЛПВП [3]. В-третьих, связь между повышенным уровнем триглицеридов и риском ИБС основана на присутствии так называемого «атерогенного липидного профиля», представляющего собою повышение триглицеридов, малых плотных ЛПНП и снижение ХС ЛПВП. Малые плотные ЛПНП отличаются повышенной способностью к окислению и пенетрации сосудистой стенки [13]. Уменьшение уровней ЛПВП может ограничивать анти-атерогенные функции этого класса липопротеинов, включающие обратный транспорт холестерина, антиоксидантные эффекты, антипролиферативную активность [16].
Роль гипертриглицеридемии в генезе других заболеваний.
Классификация гипертриглицеридемий
В зависимости от уровня повышения ТГ принято выделять три степени гипертриглицеридемии— пограничное повышение ТГ, высокий уровень ТГ и очень высокий уровень ТГ (Таблица 1).
Что касается приобретённых факторов, провоцирующих развитие дислипидемии вообще, проведено несколько исследований, оценивавших связь образа жизни и вредных привычек с развитием дислипидемии. Показано, что курение повышает уровень ТГ на 0,15 ммоль/л и снижает уровень ХС ЛПВП на 0,09 ммоль/л с каждыми 20 выкуренными сигаретами, а избыточное потребление алкоголя связано со значительным повышением липопротеинов, богатых ТГ, и признано одной из наиболее частых причин ГТГ; так прием алкоголя увеличивает уровень ТГ в среднем на 0,11 ммоль/л и повышает уровень ХС ЛПВП на 0,06 ммоль/л на каждые 23 г алкоголях [20,21]. В той же работе оценивались эффекты физической нагрузки. Показано, что степень влияния на липиды зависит от характера нагрузки; так, прогулка длительностью более 6000 шагов в день снижает уровень ТГ на 0,11 ммоль/л и повышает уровень ХС ЛПВП на 0,08 ммоль/л, тяжелая физическая нагрузка (бег или плавание) – на 0,11 и 0,13 ммоль/л, соответственно, на каждые 300 ккал нагрузки. Наконец, диета со сниженным потреблением насыщенных жиров и ХС приводит к снижению уровня общего ХС на 0,52 ммоль/л, ТГ на 0,45 ммоль/л и повышению уровня ХС ЛПВП на 0,13 ммоль/л [21].
Часто повышение ТГ крови обусловлено сахарным диабетом [22,23]. Показано, что количественненные и качественные изменения инсулина при диабете приводят к нарушению его взаимодействия с адипоцитами, что сопровождается усилением внутриклеточного гидролиза ТГ и высвобождением неэстерифицированных ЖК (НЭЖК). Избыток НЭЖК в условиях относительного дефицита инсулина и сниженной его активности приводит к сложным изменениям метаболизма липидов плазмы. Во-первых, повышается уровень ЛПОНП плазмы. Повышенный уровень ЛПОНП ассоциируется с постпрандиальной гиперлипидемией, которая усиливается в условиях нарушенной активности ЛПЛ. Последняя прямо коррелирует с ИБС. С другой стороны, известно, что ремнантные частицы могут переносить большее количество ХС к макрофагам, чем ЛПНП-частицы. Во-вторых, снижается уровень ХС ЛПВП плазмы. Снижение уровня ХС ЛПВП означает уменьшение выхода ХС из периферических тканей в печень. Когда уровень ХС ЛПВП снижается, антиоксидантная и антиатерогенная активность ЛПВП уменьшается. ЛПНП-частицы становятся меньшей плотности и размеров, что усиливает их окисляемость и способность пенетрировать сосудистую стенку. Кроме того, ГТГ вызывает тромбогенные сдвиги в системе коагуляции, что может способствовать развитию тромбоза. В результате отмеченных механизмов диабетическая дислипидемия высоко коррелирует с риском развития ИБС [24,25]. Подводя итог, следует сказать, что пограничное повышение ТГ часто является компонентом атерогенной дислипидемии, включающей повышенное содержание мелких плотных ЛПНП и сниженный ХС ЛПВП, и метаболического синдрома.
«Высокий уровень триглицеридов» (до 2,3- 5,5 ммоль/л). В большинстве случаев высокая ГТГ обусловлена комбинацией генетических и не генетических факторов. У многих пациентов отмечается инсулинорезистентность и метаболический синдром, а также абдоминальный тип ожирения. Однако преобладающее значение имеют генетические факторы. Во многих семьях частота этой дислипидемии значительно повышена, что свидетельствует о её наследственной природе. Выделяют три формы генетически обусловленного повышения ТГ плазмы крови.
При семейной комбинированной гиперлипидемии (СКГЛ) повышается уровень как ХС, так и ТГ. Характерной биохимической особенностью заболевания является повышенный синтез ЛПОНП в печени. СКГЛ ассоциируется с повышенным риском ИБС. Эта дислипидемия – одна из самых частых форм ГТГ, встречается у 1-3% лиц взрослой популяции и её частота возрастает до 20% у пациентов с первичным ИМ. К сожалению, какие-либо специфические клинические особенности заболевания отсутствуют. Диагноз СКГЛ обычно ставят на основании наличия у пациента повышенных уровней ХС (6 ммоль/л и более), ТГ (1,7-10 ммоль/л), апо В-100 (более 1200 мг/л), и разнообразных фенотипов ГЛП у родственников. Патогенез метаболических нарушений при СКГЛ характеризуется аномальным увеличением продукции апоВ-100 при нормальном или нарушенном клиренсе ТГ. Предполагают, что увеличение синтеза апоВ в печени связано с повышенным притоком периферических свободных жирных кислот (СЖК) вследствие дефекта метаболизма СЖК в адипоцитах. Кроме того, СЖК активируют глюконеогенез в печени. Повышение синтеза глюкозы сопровождается усилением секреции инсулина поджелудочной железой для поддержания нормогликемии и, таким образом, повышенной концентрацией инсулина плазмы, что ассоциируется с синдромом инсулинорезистентности. Нарушение гормонального влияния на уровне адипоцитов уменьшает захват ими СЖК, в результате чего напрямую повышается концентрация СЖК в плазме. Наконец, повышение СЖК в плазме и инсулинорезистентность ингибируют активность этого фермента, повышают высвобождение из эндотелиальных клеток и усиливают захват ЛПЛ печенью. Таким образом, нарушенный метаболизм СЖК патофизиологически связан с гиперпродукцией апоВ в печени, частичным дефицитом ЛПЛ и инсулинорезистентностью [26,27].
Что касается генетической основы СКГЛ, то остается неясной природа генетического дефекта. Показано, что наследование фенотипа СКГЛ сложное. Сегрегационный анализ свидетельствует о том, что уровни апоВ, ТГ, ЛПНП регулируются многими генами. Проведённые исследования определили несколько хромосомных регионов, ответственных за профиль липидных нарушений при СКГЛ, и которые значительно варьировали в разных популяциях: 1q21, 2q31, 2p25.1, 10p11.2, 11p14.1-q12.1, 16q24.1, 21q21 [26, 27].
Случаи повышения ТГ без сопутствующего повышения ХС плазмы крови у членов одной семьи относят к семейной гипертриглицеридемии (СГТГ). У многих пациентов с СГТГ также отмечается ожирение или другие проявления метаболического синдрома. Биохимические особенности этой формы дислипидемии – повышенное содержание ЛПОНП и хиломикрон, при нормальном уровне ХС плазмы крови, что фенотепически проявляется IV или V типом гиперлипидемии, так же, отмечается сниженный уровень ХС ЛПВП [28].
Причиной данного заболевания является умеренное снижение активности ЛПЛ, в результате мутаций гена ЛПЛ, причем для развития заболевания достаточно повреждения одного аллеля данного гена. В тоже время, если мутации происходят в двух аллелях гена ЛПЛ это приводит к более существенному повышению ТГ, в основном за счет хиломикрон, и проявляется I типом гиперлипидемии [28,29]. Более подробно о гомозиготной форме дефицита ЛПЛ будет сказано позднее.
К третей форме генетически обусловленного высокого уровня ТГ относиться семейная дисбеталипопротеинемия или ГЛП III типа. Как правило, причиной данного заболевания является сочетание генотипа апо Е2/Е2 и дополнительного генетического или метаболического фактора. Эти дополнительные факторы приводят к: 1) повышению синтеза липопротеинов, 2) нарушению липолиза липопротеинов, или 3) снижению захвата ремнантных частиц печенью. Наиболее известные факторы, способствующие развитию ГЛП III типа, включают гипотиреоз, ожирение, сахарный диабет и чрезмерное употребление алкоголя [20,21].
Пациенты с III типом ГЛП обычно очень хорошо отвечают на терапию. В некоторых случаях только диета и лечение сопутствующей патологии (ожирения, гипотиреоза, диабета) нормализуют уровень липидов плазмы. Однако, большинству пациентов с III типом ГЛП в дополнение к диете требуется липидснижающая терапия.
«Очень высокий уровень триглицеридов» подразумевает повышение концентрации ТГ плазмы крови более 5,6 ммоль/л [19] вследствие хиломикронемии и повышения уровня ЛПОНП. При наиболее тяжёлых формах уровень ТГ обычно превышает 11 ммоль/л. При выраженной хиломикронемии содержание ТГ в плазме может даже превышать 100 ммоль/л. В связи с повышением ХМ, содержащих как ХС пищи, так и синтезируемый кишечником, а также из-за повышенного уровня ЛПОНП, которые тоже содержат ХС, может наблюдаться сопутствующее повышение уровня общего ХС до 30 ммоль/л и более без увеличения концентрации ХС ЛПНП. Случаи тяжелой ГТГ могут носить семейный (генетический), вторичный (индуцированный) или смешанный характер. При этом наблюдается как повышение синтеза ЛПОНП печенью (семейные формы, диабет, ожирение, употребление алкоголя, прием эстрогенов), так и снижение липолиза ЛПОНП и ХМ (генетические факторы, гипотиреоз, применение β-адреноблокаторов, сахарный диабет) Частота тяжелой ГТГ (более 10 ммоль/л) оценивается как 1 случай на 1000 среди взрослых [12].
В некоторых случаях тяжелая ГТГ может быть обусловлена наследственным дефицитом ЛПЛ. Это заболевание имеет аутосомно-рециссивный тип наследования и проявляется ГЛП I (в гомозиготном состоянии) или V (в гетерозиготном состоянии) типа [28]. Большинство мутаций в гомозиготном состоянии гена ЛПЛ приводит к полной утрате активности фермента, однако гомозиготная форма заболевания встречается чрезвычайно редко – 1 случай на миллион в общей популяции. У гетерозигот отмечается умеренное уменьшение активности ЛПЛ и повышение уровня ТГ плазмы, сочетающееся со снижением ХС ЛПВП [29]. У носителей разных типов мутаций гена ЛПЛ, приведших к снижению постгепариновой плазменной активности липопротеинлипазы от 22 до 53 % и уменьшению ХС ЛПВП на 0.08-0.25 ммоль/л выявлено повышение риска ишемической болезни сердца в 1.2-4.9 раза по данным мета-анализа 29 исследований [2,31,32]. Так же показано, что курение в дополнение к мутации ЛПЛ приводило к увеличению риска ИБС [33].
Тактика обследования лиц с выраженной гипертриглицеридемии основана на:
1) измерении уровня плазменных триглицеридов в сопоставлении с уровнями холестерина, ХС ЛПВП стандартными биохимическими методами;
2) проведение типирования гипертриглицеридемии с помощью электрофореза липопротеидов;
3) исключение вторичного (индуцированного сопутствующими заболеваниями и состояниями) генеза заболевания: определение уровня глюкозы крови, маркеров функции печени и почек.
3) для исключения либо подтверждения дефекта на уровне липопротеинлипазы желательно определение уровней постгепариновой активности липопротеинлипазы и ее массы.
И наконец, наиболее достоверным в идентификации типа гипертриглицеридемии является генетическое исследование на предмет выявления мутаций генов, ответственных за вышеуказанные ключевые регуляторы метаболизма триглицеридов [10,11,28]. Сравнение различных наследственных форм гипертриглицеридемии представлено в Таблице 2.
В заключение нашего обзора, в котором мы попытались рассказать читателям о причинах возникновения гипертриглицеридемии, ее клиническом значении в развитии ряда заболеваний и о подходах применяемых в дифференциальной диагностики различных форм гипертриглицеридемии, хотелось бы подчеркнуть важность выявления причины гипертриглицеридемии в каждом случае повышения уровня ТГ у пациентов, так как от этого может зависеть выбор медикаментозной терапии, а также оценка прогноза и степени тяжести гипертриглицеридемии.
1. Ginsberg H.N. New perspectives on atherogenesis. Role of abnormal triglycerid-rich lipoprotein metabolism. Circulation 2002; 106:2137-2142.
2. Wittrup H.H., Tybjaerg-Hansen A., Nordestgaard B.G. Lipoprotein lipase mutations, plasma lipids and lipoproteins, and risk of ischemic heart disease. Circulation 1999; 99: 2901-2907.
3. Ginsberg H.N. Hypertriglyceridemia: new insights and new approaches to treatment. Am.J.Cardiol.2001;87:1174-1180.
4. Manninen V., Tenkanen L., Koskinen P., et el. Helsinki Heart Study. Circulation, 1992;85:37-45.
5. Jeppesen J., Hein H.O., Suadicani P., and el. Triglyceride concentration and ischemic heart disease: an eight-year follow-up in the Copenhagen Male Study. Circulation 1998;97:1029-1036.
6. Hokanson J.E., Austin M.A. Plasma triglyceride is a risk factor for cardiovascular disease independent of high-density lipoprotein cholesterol: a meta-analysis of population-based prospective studies. J Cardiovasc risk 1996;3:213-219.
7. Sprecher D.L., Harris B.V. Higher triglycerides, lower high-density lipoprotein cholesterol and higher systolic blood pressure in lipoprotein lipase-deficient heterozygotes. Circulation 1996; 94:3239-3245.
8. Okura Y., Hayashi K. Diagnostic evaluation of acute pancreatitis in two patients with hypertriglyceridemia. World J Gastroenterol 2004;10(24): 3691-3695.
9. Stojakovic T., Scharnagl H., Marz W. Apo E: crossroads between Alzheimers disease and atherosclerosis. Seminars in vascular medicine, V4, N3 2004, 279-285.
10. Evans V., Kastelein J.J.P. Lipoprotein lipase deficiency-rare or common? Cardiovascular drugs and therapy 2002; 16:283-287.
11. Merkel M., Eckel R.H., Goldberg I.J. Lipoprotein lipase: genetics, lipid uptake, and regylation. Journal of lipid research V43, 2002:1997-2006.
12. Durrington P. Dyslipidaemia. Lancet 2003; 362:717-31.
13. Lusis AL.J., Fogelman Al.M. Genetic Basis of Atherosclerosis. Clinical Implications. Circulation 2004;110:2066-2071.
14. Le N-A, Cibson J.C. Independent regulation of plasma apolipoproteins CII and CIII concentrations in very low density and high density lipoproteins: implications for the regulation of the catabolism of these Lipoproteins. J Lipid Res 1988;29:669-677.
16. Ansell B.J., Watson K.E. High-density lipoprotein function.J Am Coll Cardiol 2005;46:1792-8.
17. Ashen M.D., Blumenthal R.S. Low HDL Cholesterol levels. N Engl J Med 2005;353:1252-60.
18. Bahaev V.R. Macrophage LPL promotes foam cell formation and atherosclerosis in low density lipoprotein receptor-deficient wice. J Biol. Chem 2000;275:26293-26299
19. Third Report of the National Cholesterol Education Program Expert Panel on Detection, Evaluation, and Treatment of High Blood Cholesterol in Adults, final report. Circulation 2002; V106,25, p 3157-3373.
20. Hata Y., Nakajima K. Life-style and serum lipids and lipoproteins. J Atheroscler Thromb. 2000;7(4):177-97
21. Lee W.Y., Jung C.H., Park J.S., Rhee E.J., Kim S.W. Effects of smoking, alcohol, exercise, education, and family history on the metabolic syndrome as defined by the ATP III. Diabetes Res Clin Pract. 2005 Jan;67(1):70-7.
22. Grundy S. M. Hypertriglyceridemia, insulin resistance, and the metabolic syndrome. Am J Cardiol.1999;83:25F-29F.
23. Erkelens D.W. Diabetic dyslipidaemia. Eur Heart J 1998;19(suppl):H27-H30.
24. Horward B.V. Insulin resistance and lipid metabolism. Am. J Cardiol 1999;84;28j-32j.
25. Krentz A.J. Lipoprotein abnormalities and their consequences for patients with type 2 diabetes. Diabetes Obes Metab. 2003 Nov;5 Suppl 1:S19-27.
26. De Graaf J., van der Vleuten G., Stalenhoef A.F. Diagnostic criteria in relation to the pathogenesis of familial combined hyperlipidemia. Seminars in vascular medicine, V4, N3 2004,229-239.
27. Shoulders C.C., Jones E.L., Naoumova R.P. Genetics of familial hyperlipidemia and risk of coronary heart disease. Human molecular genetics, 2004, V 13, R 149-R160.
28. Tompson G.P. A handbook of hyperlipidaemia.p 118-124. Current Science, ltd. London 1990.
29.Talmud P.J. Genetic determinants of plasma triglycerides: impact of rare and common mutations. Curr Atheroscler Rep 2001;3:191-199.
30. Smelt A.H.M., de Beer F. Apolipoprotein E and Familial Dysbetalipoproteinemia: clinical, biochemical and genetic aspects. Seminars in vascular medicine, V4, N3 2004,249-257.
31. Wittrup H.H., Nordestgaard B.J. A common mutation in lipoprotein lipase confers a 2-fold increase in risk of ischemic cerebrovascular disease in women but not in men. Circulation 2000; 101: 2393-2397.
32. Jukema J.W. The Asp 9 Asn mutation in the Lpl gene is associated with increased progression of coronary atherosclerosis. Circulation 1996;94:1913-1918.
33. Talmud P.J., Dujac S. Substitution of D9N of LPL markedly augment risk of coronary heart disease in man smokes. Atherosclerosis 2000;149:75-81.
34. Murase T., Ymada N. Decline of postheparin plasma lipoprotein lipase in acromegalic patients. Metabolism 1980;29: 666-72.
Что такое гиперлипопротеинемия? Причины возникновения, диагностику и методы лечения разберем в статье доктора Колесниченко Ирины Вячеславовны, кардиолога со стажем в 24 года.
Определение болезни. Причины заболевания
Это состояние является частным случаем дислипидемии.
Заболевание может долго протекать без симптомов и выявляться случайно после сдачи анализов. При длительном течении болезни развивается атеросклероз, который приводит к сужению сосудов. Симптомы зависят от того, какие артерии поражены:
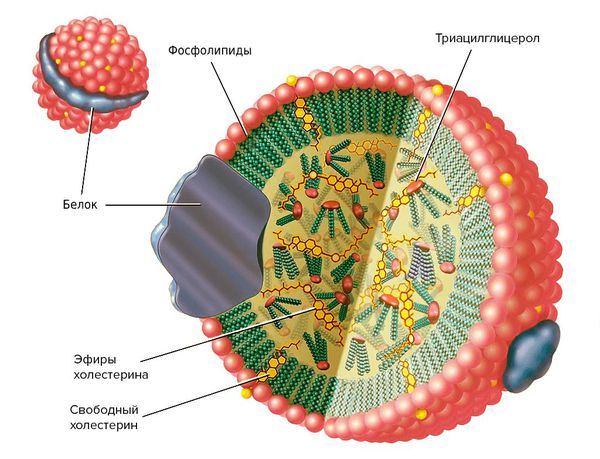
Липопротеины — это растворимые в воде частицы, состоящие из жиров (липидов) и белков (апопротеинов). Они очень важны для организма, поскольку переносят витамины, гормоны и жиры, которые поступают с пищей и синтезируются в печени.
Распространённость
Причины гиперлипопротеинемии
Гиперлипопротеинемии бывают первичными и вторичными. Первичные формы имеют врождённую природу, но встречаются довольно редко: ими страдают 0,25 % населения.
К врождённым гиперлипидемиям относятся:
Вторичные гиперлипопротеинемии обусловлены различными заболеваниями, приёмом некоторых лекарств и неправильным образом жизни.
Наиболее часто заболевание развивается при сахарном диабете, хронической почечной недостаточности, нефротическом синдроме, гипотиреозе, ожирении, желчнокаменной болезни, холестазе, анорексии, частичной или полной потере жировой ткани (липодистрофии), болезнях накопления гликогена, сильном стрессе, сепсисе, беременности, остром гепатите, системной красной волчанке и лимфоме.
Лекарства, которые могут привести к гиперлипопротеинемии:
К развитию гиперлипопротеинемии часто приводит неправильный образ жизни на фоне хронических заболеваний. К неблагоприятным факторам относятся:
Также важно отметить причины, из-за которых снижается уровень ЛПВП. Помимо курения, к ним относятся недостаточное питание и ожирение. Концентрация защитных липопротеинов может уменьшаться при приёме бета-блокаторов и анаболических стероидов.
Уровень общего холестерина может быть выше нормы и у здоровых людей, например при неправильной подготовке к анализу крови и во время беременности.
Гиперлипопротеинемия при беременности
У беременных женщин уровень общего холестерина повышается в 1,5–2 раза. Он резко возрастает в начале II триместра, когда активно формируется плацента. Холестерин — это основа для её клеток, поэтому чем больше срок беременности, тем выше его уровень.
Симптомы гиперлипопротеинемии
Гиперлипопротеинемия может длительное время протекать бессимптомно. Повышенный уровень вредных липидов выявляется при анализах, но клинические симптомы долго не возникают.
При врождённых гиперлипопротеинемиях, вызванных генетическими факторами, симптомы появляются рано. Уровень холестерина при врождённых формах болезни всегда выше 6,5 ммоль/л. Он колеблется от 7 до 13 ммоль/л и выше.
Симптомы первичной гиперлипопротеинемии
К характерным проявлениям гомозиготной семейной гиперхолестеринемии, при которой человек наследует дефектный ген от обоих родителей, относятся:
При семейной гипертриглицеридемии в крови повышается уровень триглицеридов (до 2,8–8,5 ммоль/л) и липопротеинов очень низкой плотности.
Симптомы вторичной гиперлипопротеинемии
При вторичных гиперлипопротеинемиях симптомы зависят от расположения поражённых атеросклерозом артерий, степени и количества вовлечённых сосудов.
Долгое время уровень вредных липопротеинов растёт, а содержание защитных липопротеинов снижается, но симптомы отсутствуют. Они появляются по мере развития атеросклероза.
К таким признакам относятся:
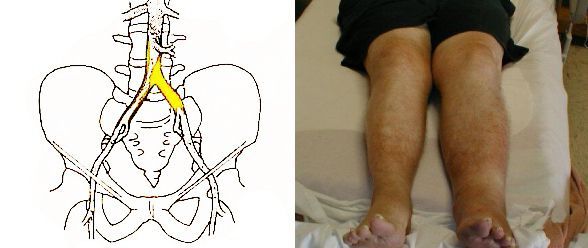
В зависимости от того, какие артерии повреждены атеросклерозом, возникают следующие симптомы:
Патогенез гиперлипопротеинемии
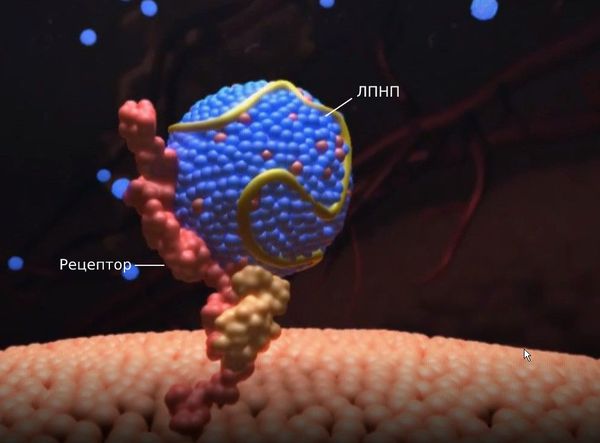
Первичные гиперлипопротеинемии вызваны мутациями в генах, которые ответственны за образование и работу рецепторов к липопротеинам низкой плотности. При гетерозиготной форме семейной гиперхолестеринемии ЛПНП-рецепторы могут быть наполовину полноценными, а при гомозиготной форме — практически полностью отсутствовать. Из-за этого дефекта рецепторы не захватывают липопротеины, они хуже распадаются и не выводятся из организма, поэтому их уровень в крови растёт.
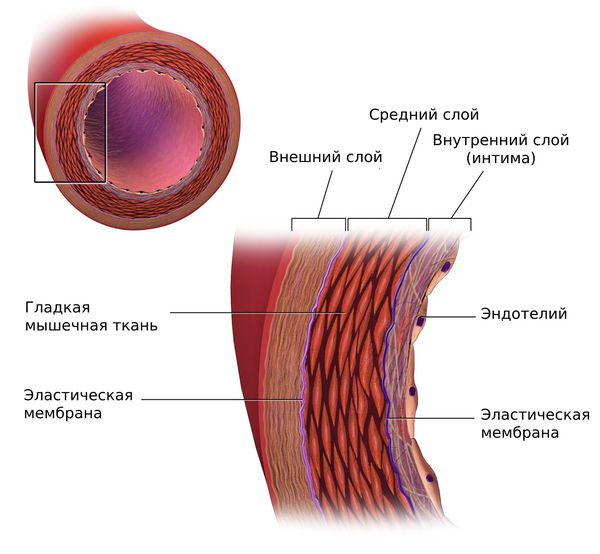
При вторичных гиперлипопротеинемиях повреждается внутренняя оболочка артерий и в неё активно проникают липопротеины.
Липопротеины подразделяются на два вида:
Атерогенность зависит от размеров и физико-химических свойств липопротеиновых частиц.
Липопротеины очень низкой плотности и липопротеины низкой плотности (ЛПОНП и ЛПНП) являются атерогенными и проникают во внутреннюю оболочку артерий (интиму) при повреждении эндотелия.
Дисфункцию эндотелия артерий вызывают:
Под влиянием этих факторов эндотелий разрыхляется и истончается. Расширяются щели между клетками, возникает отёк, клетки и волокнистые структуры внутренней оболочки артерий разъединяются, и частицы атерогенных липопротеинов проникают в интиму артерий.
Затем к этим частицам присоединяется глюкоза. Процесс модификации липопротеинов называется гликозилированием, или гликированием. Он особенно интенсивен при сахарном диабете и избытке глюкозы в крови. В результате нарушается взаимодействие ЛПНП с рецепторами клеток, замедляется распад липопротеинов и, следовательно, развивается гиперлипопротеинемия. Гликирование защитных ЛПВП ускоряет их распад.
Второй путь модификации липопротеинов низкой плотности — пероксидация, или перекисное окисление. Это важнейший фактор развития атеросклероза. В организме постоянно образуются свободные радикалы: ионы, атомы или молекулы с одним неспаренным электроном на своей орбите. Поскольку у них есть свободное место для электрона, они стремятся отнять его у других молекул. Так окисляются любые соединения, с которыми они соприкасаются. Пероксидация ЛПНП делает их высокоатерогенными.
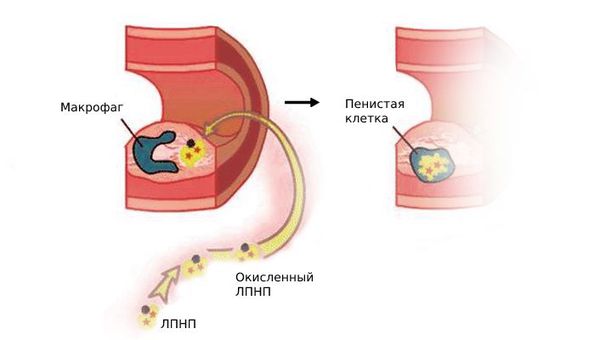
Следующий этап атерогенеза — пропитывание интимы артерий циркулирующими лейкоцитами (моноцитами), которые трансформируются в макрофаги. Они захватывают модифицированные ЛПНП, содержание холестерина в макрофагах быстро нарастает, и они превращаются в пенистые клетки.
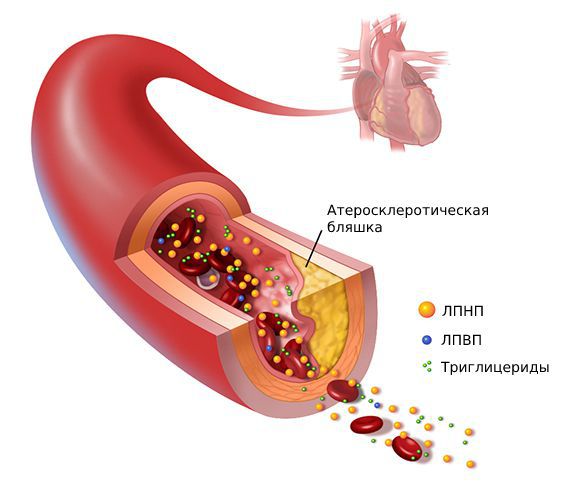
Пенистые клетки остаются в интиме артерий и погибают. При этом они выделяют накопленный холестерин, который образует липидные пятна и полоски, а затем атеросклеротические бляшки.
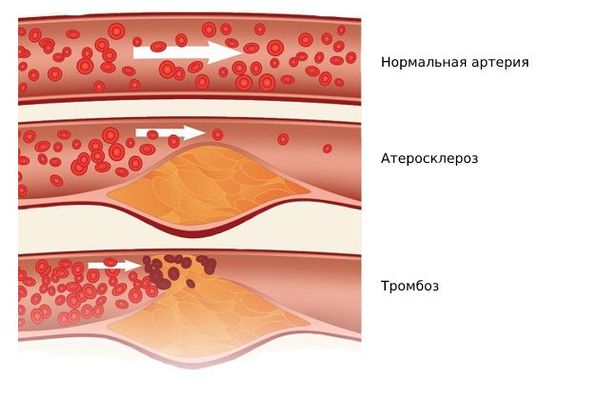
Одним из наиболее серьёзных осложнений атеросклероза является тромбоз в области бляшки — частичная или полная закупорка артерии тромбом. Образованию тромба предшествуют надрывы и разрывы фиброзной покрышки бляшки, а также повреждение эндотелия самой бляшкой. Иногда атеросклеротическая бляшка становится источником эмболий, при которых её оторвавшийся кусочек закупоривает какой-либо сосуд.
Осложнением атеросклеротической бляшки также является атерокальциноз — отложение солей кальция в стенке сосудов.
Классификация и стадии развития гиперлипопротеинемии
Наиболее распространена классификация липопротеинов в зависимости от плотности:
По участию в развитии атеросклероза липопротеины подразделяются на три класса:
Типы гиперлипопротеинемии
Гиперлипопротеинемии подразделяются на следующие типы:
Также широко применяется классификация гиперлипопротеинемий, предложенная Фредриксоном и соавторами в 1967 году:
Осложнения гиперлипопротеинемии
Диагностика гиперлипопротеинемии
Диагностика гиперлипопротеинемий состоит из осмотра, лабораторных исследований и инструментальных методов.
Осмотр
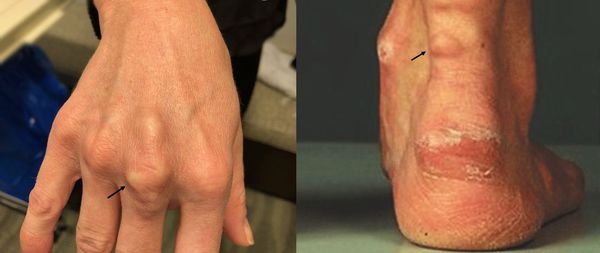
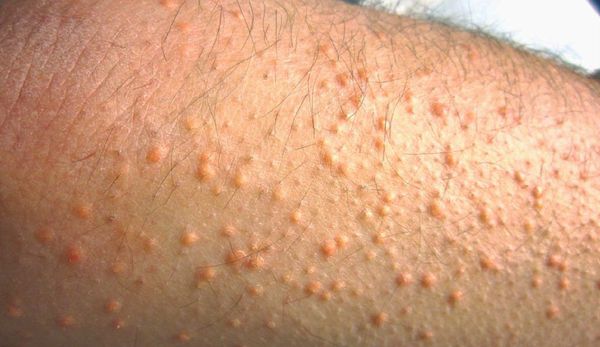
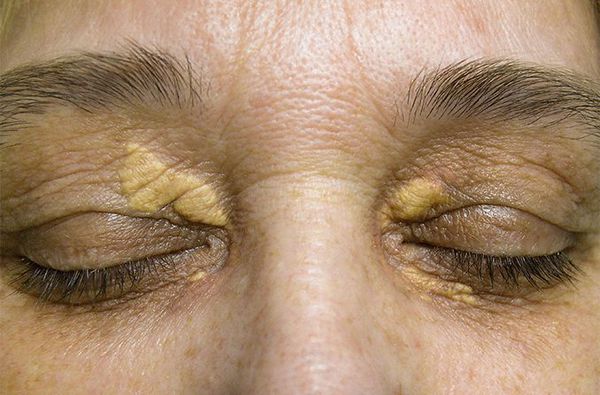
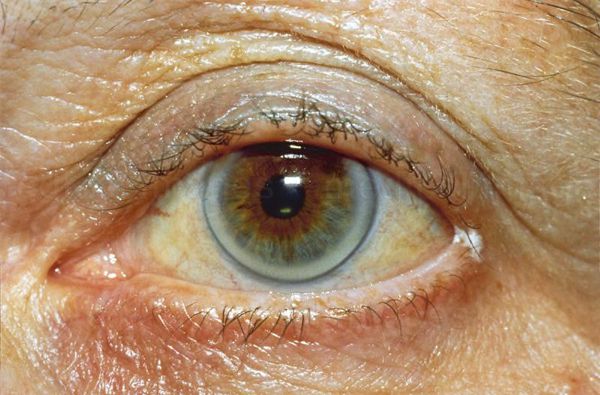
При осмотре врач обращает внимание на признаки, указывающие на нарушение обмена липидов:
Измерение артериального давления
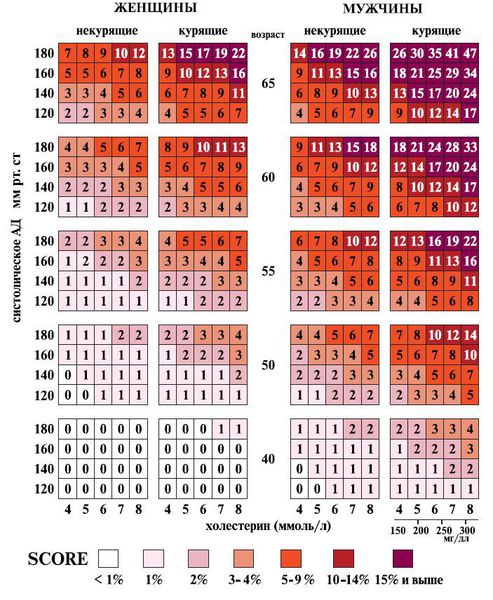
Шкала SCORE — это тест-калькулятор для оценки сердечно-сосудистого риска.
Сердечно-сосудистый риск зависит от сочетания следующих факторов:
По шкале SCORE пациенты попадают в категории низкого, умеренного, высокого и очень высокого риска.
Полученное значение показывает вероятность смерти от сердечно-сосудистого заболевания в ближайшие 10 лет.
Также всем пациентам необходимо проверить состояние печени. Для этого исследуется уровень печёночных ферментов (АСАТ, АЛАТ). Анализ позволяет определить, можно ли назначать статины — препараты для снижения уровня липопротеинов.
Не менее важно проверить состояние щитовидной железы. Для этого исследуется уровень тиреотропного гормона (ТТГ), так как гипотиреоз может быть причиной нарушений липидного обмена и требует коррекции.
Также при гиперлипопротеинемии необходимо определить уровень глюкозы в крови, поскольку сахарный диабет способствует быстрому развитию атеросклероза.
Инструментальные методы диагностики
Для выявления атеросклероза используются:
Лечение гиперлипопротеинемии
Диета
Если у пациента нет симптомов, то лечение начинают со специальной диеты. Коррекция питания позволяет уменьшить уровень холестерина на 5–10 %.
Важно помнить, что холестерин не только поступает извне, но и образуется в организме. Поэтому полностью отказываться от продуктов, содержащих жиры, не стоит.
Медикаментозное лечение
При сердечно-сосудистых заболеваниях, сахарном диабете, хронической болезни почек и высоком риске по шкале SCORE показан приём препаратов, снижающих холестерин. Однако в ряде случаев пациентам даже с умеренным риском может потребоваться медикаментозная терапия. Она поможет уменьшить вероятность развития атеросклероза.
Группы препаратов для лечения гиперлипопротеинемии:
Статины
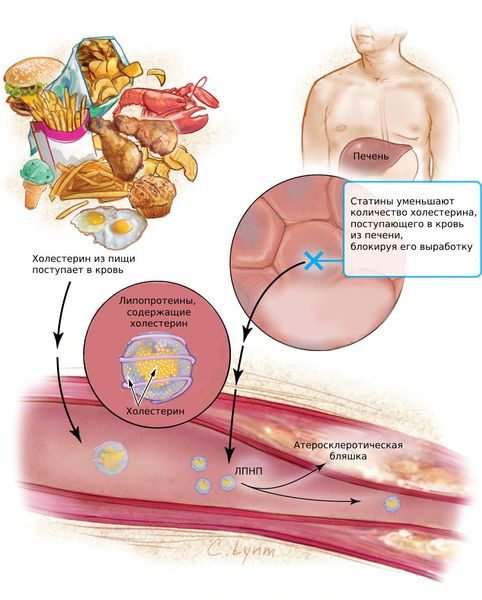
Статины (Аторвастатин, Розувастатин, Питавастатин) — это наиболее эффективные средства для снижения холестерина. Они блокируют фермент, который участвует в его образовании и тем самым подавляет выработку холестерина в печени. Статины снижают содержание липопротеинов низкой плотности (ЛПНП) и триглицеридов (ТГ).
Статины предотвращают развитие атеросклероза коронарных и церебральных артерий, а при длительном приёме уменьшают размер бляшек в сосудах. Эти препараты необходимы пациентам с гиперлипопротеинемией и атеросклерозом для профилактики инфаркта миокарда и инсульта.
Перед тем, как начать принимать статины, необходимо определить липидный профиль, а также проверить состояние печени по содержанию в крови печёночных ферментов (АСАТ, АЛАТ). Статины применяют в безопасных дозировках до достижения целевых уровней ЛПНП. Дозировка зависит от кардиоваскулярного риска пациента.
Для оценки безопасности и эффективности назначенной дозы через месяц после начала приёма необходимо повторно провести анализы на липидный профиль, АСАТ и АЛАТ. Эффект проявляется в течение первой недели от начала лечения. Через две недели он составляет 90 % от максимального действия. Наибольший эффект достигается к четвёртой неделе и затем остаётся постоянным.
Если целевой уровень ЛПНП достигнут и препарат не влияет отрицательно на печень, то статин в данной дозировке применяют длительно. Липидный профиль, АСАТ и АЛАТ контролируют через каждые 3–6 месяцев. При повышении печёночных ферментов выше трёх норм препарат перестают применять.
Помимо снижения холестерина, статины положительно влияют на состояние внутренней оболочки артерий, стабилизируют атеросклеротические бляшки и улучшают текучесть крови.
Статины обычно хорошо переносятся, но у некоторых пациентов возникают побочные эффекты, например боль в мышцах. Принимать препараты следует под постоянным контролем врача, вовремя корректировать их дозу или использовать в комбинации с другими лекарствами.
Фибраты
Фибраты (Фенофибрат) стимулируют активность фермента липопротеинлипазы и тем самым ускоряют распад липопротеинов. Они снижают не только холестерин, но и триглицериды (ТГ). Это препараты выбора у больных с сахарным диабетом, у которых чаще всего повышены ТГ.
Ингибиторы всасывания холестерина в кишечнике
Секвестранты желчных кислот
Секвестранты (Холестирамин, Колестипол) — ионообменные смолы, которые не дают желчным кислотам всасываться в кишечнике. Истощение запасов этих кислот активирует их синтез из холестерина в печени. Применяются у пациентов с холестазом.
Приём препаратов данной группы часто вызывает побочные эффекты: метеоризм, задержку стула, тошноту, боль или дискомфорт в верхнем отделе живота, что ограничивает их применение.
Моноклональные антитела
N-3 жирные кислоты
Гиполипидемическую терапию важно назначать вовремя, чтобы предотвратить развитие атеросклероза и его осложнений.
Прогноз. Профилактика
При ранней диагностике гиперлипопротеинемии и своевременном снижении уровня атерогенных липопротеинов прогноз благоприятный.
Заболевание может долго протекать без симптомов и выявиться только при профилактическом исследовании, поэтому необходимо регулярно определять липидный профиль. Это поможет избежать атеросклероза и его серьёзных осложнений: инфаркта миокарда, инсульта и т. д.
Если дислипидемия диагностирована при развившемся атеросклерозе, то следует изменить питание и начать медикаментозное лечение. Если удаётся добиться целевых уровней липидов в крови, то прогноз благоприятный. В таком случае сердечно-сосудистый риск значительно снижается. Пациенту необходимо следовать рекомендациям врача и регулярно делать липидограмму.
Прогноз неблагоприятный при значительном повышении уровня липидов в крови, сопутствующих заболеваниях, таких как артериальная гипертензия, сахарный диабет, хроническая болезнь почек и осложнения атеросклероза. Такие пациенты находятся в группах высокого и очень высокого риска с большой смертностью.
Профилактика гиперлипопротеинемии
Цель первичной профилактики — уменьшить влияние возможных причин гиперлипопротеинемии. Для этого нужно правильно питаться, не курить, больше двигаться и по возможности исключить препараты, нарушающие обмен липидов.
Также для профилактики атеросклероза следует: