диагноз реконвалесцент орви что это
Диагноз реконвалесцент орви что это
К настоящему времени не разработано эффективных методов этиотропного лечения COVID-19. Применение плазмы, содержащей специфические антитела к возбудителю, является эффективным методом лечения многих вирусных заболеваний. Такое лечение является достаточно безопасным. К сожалению, введение плазмы тяжелым пациентам на поздних сроках заболевания оказалось неэффективным. Представляется, что применение антител-содержащих препаратов может быть эффективным при максимально раннем введении. Также целесообразным представляется использование плазмы с высоким титром антител.
Наиболее уязвимой категорией в отношении COVID-19 оказались пожилые пациенты, среди которых смертность от данного заболевания максимальна.
В NEJM опубликованы результаты небольшого рандомизированного плацебо-контролируемого исследования, в котором оценивалась эффективность и безопасность введения плазмы с высоким титром антител к SARS-CoV2 у пациентов старшей возрастной категории в течение 72 часов от момента манифестации COVID-19 легкой степени тяжести. Включались лица старше 75 лет или 65-74 лет хотя бы с одним сопутствующим заболеванием, ассоциирующимся с ухудшением прогноза на фоне COVID-19. В качестве критериев эффективности оценивалась частота прогрессирования заболевания до развития тяжелой дыхательной недостаточности (снижение сатурации менее 93% на атмосферном воздухе, ЧДД более 30). В качестве плацебо использовался изотонический раствор.
Существенных побочных эффектов зарегистрировано не было.
Умерло 2 пациента в группе плазмы и 4 в группе плацебо.
Т.о., раннее введение плазмы реконвалесцентов с высоким титром антител на ранних сроках заболевания способно предотвратить прогрессирование COVID-19 у пациентов высокого риска.
Libster R, Pérez Marc G, Wappner D, et al. Early High-Titer Plasma Therapy to Prevent Severe Covid-19 in Older Adults. N Engl J Med. 2021 Jan 6. doi: 10.1056/NEJMoa2033700.
РЕКОНВАЛЕСЦЕНТ
Полезное
Смотреть что такое «РЕКОНВАЛЕСЦЕНТ» в других словарях:
реконвалесцент — (ре + лат. convalescens, convalescentis выздоравливающий) больной в стадии выздоровления … Большой медицинский словарь
реконвалесцент — а, ч., мед. Людина, яка ще не одужала остаточно, але вже не має яскраво виявлених клінічних ознак хвороби … Український тлумачний словник
реконвалесцент — (лат. reconvalescens) мед. тој што закрепнува, што оздравува, што е на патот на целосното оздравување … Macedonian dictionary
реконвалесцент — Реконвалесцент: видужуючий [21] … Толковый украинский словарь
реконвалесцент — іменник чоловічого роду … Орфографічний словник української мови
Инфекцио́нные боле́зни — (позднелат. infectio заражение) группа болезней, которые вызываются специфическими возбудителями, характеризуются заразительностью, циклическим течением и формированием постинфекционного иммунитета. Термин «инфекционные болезни» был введен… … Медицинская энциклопедия
Аденови́русные боле́зни — (греч. adēn железа + Вирусы) группа инфекционных болезней, вызываемых аденовирусами и характеризующихся симптомами поражения слизистой оболочки дыхательных путей, глаз, кишечника, а также лимфоидной ткани. Относится к острым респираторным… … Медицинская энциклопедия
Амёбиа́з — (amoebiasis) протозойная болезнь, характеризующаяся хроническим рецидивирующим течением с язвенным поражением толстой кишки и нередко осложняющаяся абсцессами печени и других органов. Этиология. Возбудитель Entamoeba histolytica; в жизненном… … Медицинская энциклопедия
Сыпной тиф — Не следует путать с брюшным тифом. Сыпной тиф … Википедия
БРЮШНОЙ ТИФ — – инфекционная болезнь из группы кишечных инфекций, характеризующаяся язвенным поражением лимфатического аппарата тонкой кишки, циклическим течением, бактериемией, симптомами интоксикации, сыпью на коже. Возбудитель – Salmonella typhi,… … Энциклопедический словарь по психологии и педагогике
Восстановление легких после коронавируса
Восстанавливаются ли легкие после COVID-19? Да. Но нужно не пропустить сроки реабилитации и серьёзно отнестись к рекомендациям врача.
Новая коронавирусная инфекция, вызванная SARS-CoV-2, недостаточно изучена, однако ясно, что она наносит вред всем органам и тканям человека. Вирус проникает в организм через слизистые оболочки носа, глаз, глотки. Первые симптомы появляются на 2-14 день. Обычно это повышение температуры выше 37.5 градусов Цельсия, насморк, потеря обоняния, сухой кашель, послабление стула, слабость и головная боль. На 6–10 сутки от момента появления первых симптомов могут начать беспокоить одышка, боль в груди, усиление кашля. Это тревожные симптомы, говорящие о поражении легких и требующие проведения дополнительного обследования: компьютерной томографии легких, измерения насыщения крови кислородом (сатурации).
Легкие после COVID-19
Попадая в организм человека через слизистые оболочки дыхательных путей SARS-CoV-2 вызывает мощнейшую воспалительную реакцию. Активируются иммунные клетки, вырабатывается колоссальное количество воспалительных веществ (воспалительных цитокинов). Интенсивность этой реакции скорее всего обусловлена генетически. Именно интенсивностью воспалительной реакции и определяется тяжесть поражения легочной ткани по данным исследований. В легочной ткани поражение при COVID-19 обусловлено как поражением самих альвеол (в которых происходит газообмен и кровь насыщается кислородом из воздуха) нашими собственными иммунными клетками так и поражением легочных сосудов, оплетающих альвеолы. Степень поражения легких можно определить при помощи КТ (компьютерной томографии).
Таблица 1. Поражение лёгких при COVID-19
Процент поражения легочной ткани
Поражена часть лёгкого. Небольшое затруднение дыхания.
Особенности организации рекрутирования доноров-реконвалесцентов инфекции COVID-19 и производства иммунной антиковидной, обедненной лейкоцитами, патогенредуцированной, свежезамороженной плазмы
Журнал «Гематология и трансфузиология. Восточная Европа». – 2020. – Т. 6, № 3.
УДК 615.382+615.37
Гольдинберг Б.М., Климович О.В., Махина О.Ю., Автухова Т.Е., Ефремова К.С., Сущиц Ю.П., Полкова Е.В., Мацкевич Т.М., Сухобокова Н.В.
6-я городская клиническая больница, Минск, Беларусь
Особенности организации рекрутирования доноров-реконвалесцентов инфекции COVID-19 и производства иммунной антиковидной, обедненной лейкоцитами, патогенредуцированной, свежезамороженной плазмы
Features of organization of recruitment of reconvalescent donors with COVID-19 infection and production of immune anticovid, leucocyte-depleted, pathogen-induced and fresh-frozen plasma
Резюме
В статье анализируется собственный опыт селекции 624 реконвалесцентов инфекции COVID-19 и сравниваются результаты качества иммунной антиковидной плазмы, полученной от 88 доноров, с литературными данными.
Авторы подчеркивают, что при отсутствии специфической вакцинации и ограниченного медикаментозного арсенала иммунная донорская плазма, заготовленная от реконвалесцентов, может применяться взрослым для лечения инфекции COVID-19 в качестве дополнительного средства иммунной терапии.
Ключевые слова: инфекция COVID-19, реконвалесцент, донор, иммунная плазма.
Abstract
The article analyzes our own experience in selecting 624 convalescents with COVID-19 infection and compares the quality results of the obtained immune anticovid plasma from 88 donors with the literature data.
The authors emphasize that in the absence of specific vaccination and a limited medical arsenal, immune donor plasma prepared from reconvalescents can be used both for adults and children for the treatment of COVID-19 infection as an additional means of immune therapy.
Keywords: COVID-19 infection, reconvalescence, donor, immune plasma.
ВВЕДЕНИЕ
Пандемия инфекции COVID-19 («coronavirus disease 2019») стала тяжелым испытанием для здравоохранения практически во всех странах мира. Информация как о самом коронавирусе, так и о методах противостояния ему, постепенно накапливается. Так, к решению проблемы лечения коронавирусной инфекции одной из первых приступила группа иммунологов под руководством Артуро Касадевалла из университета Джонса Хопкинса – старейшего исследовательского университета в Западном полушарии, известного подготовкой высококлассных специалистов в области медицины, химии, биологии и права. Из-за отсутствия специфической вакцинации и ограниченного медикаментозного арсенала против коронавируса SARS—CoV-2 в качестве срочного средства иммунологами университета была предложена иммунная донорская плазма, заготовленная от реконвалесцентов.
Идея проведения пассивной иммунизации не нова. Она впервые была реализована в 1890 году немецким иммунологом Э.фон Берингом, разработавшим способы лечения дифтерии. В XIX веке это была очень опасная инфекционная болезнь, уносившая жизни тысяч детей. В 1901 году фон Беринг получил первую Нобелевскую премию в области медицины. В последующем данный метод широко использовался в ХХ веке при борьбе со столбняком, распространением кори, полиомиелита, эпидемического паротита и гриппа. Потом эту технологию вытеснили появившиеся антибиотики и другие современные лекарства. Вернуться к старому средству пришлось, когда появились «братья» нынешнего коронавируса,– SARS (атипичная пневмония) в 2002–2003 годах и MERS (Ближневосточный респираторный синдром) в 2013-2015 годах. У пациентов наблюдались тяжелые поражения легких, а попытки использовать существующие лекарства плохо помогали. И тогда в некоторых случаях стали применять реконвалесцентную плазму.
После начала эпидемии новой коронавирусной инфекции, вызванной SARS-CoV-2, китайские исследователи сообщили о применении плазмы людей, переболевших COVID-19, для тяжелобольных пациентов, когда другие средства были неэффективными [7].
Французский банк крови и Национальный институт здравоохранения и медицинских исследований с апреля 2020 года начали заготовку крови примерно у 200 пациентов, которые вылечились от коронавирусной инфекции [8].
Крупная фармацевтическая компания Takeda Pharmaceutical (Япония) при участии китайской фирмы WuXiBiologicsра рассматривает возможность разработки препарата TAK-888 на основе антител для временной профилактики поражения коронавирусом [9].
Похожую схему предлагает и калифорнийский производитель фармацевтической продукции VirPharmaceuticals. Американский фармаконцерн в настоящее время тестирует антитела, полученные в 2003 году из сыворотки крови пациентов, инфицированных SARS, на возможность их нейтрализовать коронавирус SARS-CoV-2.
Первым в России способ лечения иммунной плазмой анти-COVID-19 начинает применять НИИ скорой помощи им.Н.В. Склифосовского. У переболевших добровольцев-доноров берут с интервалом в две недели по 600 мл плазмы с антителами к коронавирусу и обрабатывают ультрафиолетовыми лучами в присутствии светочувствительных химических веществ для уничтожения различных патогенов, в том числе и COVID-19 [10].
Введение антител не панацея и не вакцинация. Разработки лекарственных средств и вакцин против коронавируса проводят параллельно. Донорские антитела не смогут выработать пожизненный иммунитет к новому вирусу, но могут обеспечить еще не болевшим людям с врожденным или приобретенным иммунным дефицитом кратковременную защиту, а находящимся в тяжелом состоянии пациентам – дать шанс выжить [6, 9, 11].
Первый случай коронавируса в Беларуси официально зарегистрирован в г.Минске 28 февраля 2020 года [12]. В республике изданы приказы Министерства здравоохранения по рекрутированию реконвалесцентов COVID-19 в доноры иммунной плазмы [2,3]. Аналогичный приказ издан комитетом по здравоохранению Мингорисполкома [4].
В процессе организации производства иммунной антиковидной свежезамороженной плазмы появились собственные технологические наработки, особенности которых, по нашему мнению, необходимо учитывать специалистам службы крови.
Актуальность темы состоит в том, что ожидается вторая волна пандемии, которую следует встретить с учетом приобретенного опыта, анализа уязвимых мест и потенциальных рисков.
ЦЕЛЬ ИССЛЕДОВАНИЯ
Показать особенности рекрутирования доноров-реконвалесцентов коронавирусной инфекции, а также определить специфические требования к качеству и инфекционной безопасности иммунной плазмы анти-COVID-19 для ее клинического применения.
МАТЕРИАЛЫ И МЕТОДЫ
Нами изучены учетные данные поликлиник и стационаров г.Минска о 624 реконвалесцентах инфекции COVID-19, статистические данные Городского центра трансфузиологии учреждения здравоохранения «6-я городская клиническая больница» (ГЦТ).
ГЦТ по отдельно созданному информационному каналу, обеспеченному защитой от несанкционированного доступа, ежедневно получал сведения по г.Минску о каждом потенциальном доноре-реконвалесценте COVID-19 после выписки из стационара или за 2-3 дня до прекращения амбулаторного наблюдения. В перечень анкетных данных вошли следующие сведения о пациентах, перенесших легкую или средней степени тяжести инфекцию COVID-19 в возрасте от 18 до 55 лет:
ФИО, дата и год рождения, адрес проживания, идентификационный номер;
результаты тестирования на SARS-CoV-2 и/или на этиологические антитела к нему.
Дополнительно в ГЦТ была создана группа медицинских работников (врачей, медсестер и медрегистраторов) для непосредственной работы с реконвалесцентами, изъявившими желание стать донорами иммунной плазмы. Ежедневное число обращений составило 15-20 в смену. После первичного отбора информация о потенциальных иммунных донорах передается группе консультантов, состоящей из врачей-трансфузиологов, рекрутирующих потенциальных доноров-реконвалесцентов COVID-19.
Материал для проведения теста полимеразной цепной реакции (ПЦР) забирали комбинированным мазком из носоглотки. Мазки немедленно помещали в стерильную транспортную пробирку, содержащую 2-3 мл транспортной среды для сохранения вирусов, и в течение 2-х часов доставляли в диагностическую лабораторию.
Выявление SARS-CoV-2 осуществлялось на амплификаторе с детекцией в режиме реального времени DT—Prime производства компании «ДНК-Технология». Для диагностики применяли следующие тест-системы: реагенты для очистки РНК «АРТ РНК экстракт» и «АРТ тест COVID-19» производства АртБиоТех ООО, Беларусь; наборы реагентов для выделения ДНК/РНК из биологического материала методом селективной преципитации «АLPREP» (форма выпуска 3) и набор реагентов для качественного выявления SARS-CoV-2 (форма выпуска 5) производства Альгимед Техно, Беларусь.
Обнаружение антител IgM и IgG к SARS-CoV-2 осуществляли тест-набором ichroma TM COVID-19 Ab, который представляет собой устройство, позволяющее их диагностировать in vitro полуколичественным методом по принципу сэндвич-иммунодетекции. Материалом исследования являлась человеческая цельная кровь, сыворотка или плазма, которые отделялись путем центрифугирования не позже 3-х часов после забора цельной крови.
Прибор для измерения тестов ichroma TM автоматически рассчитывает результат тестирования и отражает «положительный», «отрицательный» или «неопределенный» с дополнительным индексом cut-off (COI). Результаты испытаний интерпретировали в соответствии с рекомендациями производителя (табл.1).
Иммунный ответ на коронавирус SARS-CoV‑2 у больных COVID‑19
Академик Российской академии наук, д.м. н., президент
ФБГУ «НМИЦ ДГОИ им. Дмитрия Рогачева» Минздрава России
В статье представлен анализ результатов исследований иммунного ответа и памяти к SARS-CoV‑2, включая все ветви адаптивного иммунитета, иммуноглобулины, В-клетки памяти, CD8+- и CD4+-T-клетки у больных в динамике в течение 6–8 месяцев после начала заболевания.
Гуморальное звено
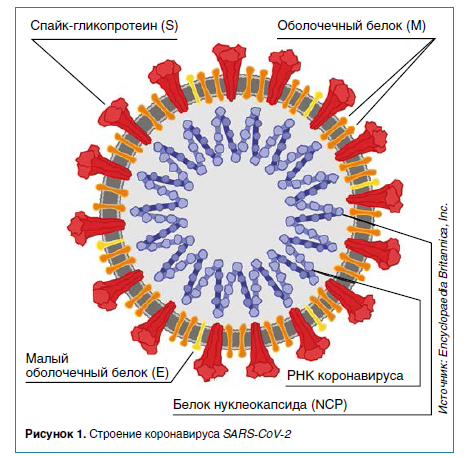
Факт первичного иммунного ответа слизистых на COVID‑19 необычен и требует объяснения. Обсуждаются две гипотезы.
Первая: вирусы контаминируют слизистые дыхательных путей и ЖКТ за 7–14 дней до появления системного ответа и клинических проявлений инфекции, поражая клетки микробиоты — используют их для репродукции вируса.
Вторая: кросс-реактивная продукция антител, предпосылкой которой являются Spike-реактивные CD4+-Т-клетки, обнаруженные у большинства пациентов с COVID‑19 и более чем у 34 % неинфицированных людей. Это подтверждает существование общих эпитопов эндемичных коронавирусов, вызывающих банальные ОРВИ и COVID‑19.
Важно, что изотипы иммуноглобулинов (либо IgG, либо IgA) конкурировали за нейтрализующую активность по отношению к SARS-CoV‑2 в зависимости от локализации. Сывороточные антитела IgG сильно коррелировали с величиной IgG-ответа и тяжестью заболевания. У пациентов, например, с IgA-назальным ответом определялась высокая активность нейтрализации вирусов. Инфекция у таких больных протекала бессимптомно.
Это, с одной стороны, предполагает возможность нейтрализации вируса с помощью IgA слизистых без системного ответа, что имеет отношение к исходам заболевания. А с другой стороны, из-за множества корреляций, наблюдаемых между типами антител и их активностью в разных анатомических участках, клиническая интерпретация гуморального ответа существенно затруднена.
Кроме того, эти данные имеют важное значение для нашего понимания защиты вакцинации, индуцирующей системный ответ на вакцинные гены или белки коронавируса по классическому пути и обеспечивающей иммунный ответ слизистых оболочек на 3–6‑й неделе после вакцинации. В идеале вакцина должна не только защитить реципиента от неизбежной болезни, но и предотвратить бессимптомное носительство, что закрыло бы проблему бессимптомных носителей в популяции.
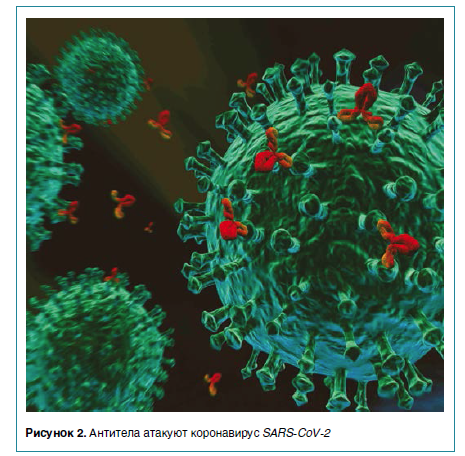
Титры Spike IgА и RBD IgА сохранялись на стабильном уровне на протяжении всего периода наблюдения t1/2— 210 дней, но у отдельных пациентов уровень специфических IgА-антител достоверно снижался через 90 дней.
Нельзя дать однозначный ответ в отношении серонегативных случаев COVID‑19. По-видимому, кроме протективного эффекта иммунитета слизистых, ответ напрямую связан с уровнем вирусной нагрузки SARS-CoV‑2. С одной стороны, высокие вирусные нагрузки связаны с более ранним ответом антител, в то время как у пациентов с низкой вирусной нагрузкой не может быть сероконверсии. С другой стороны, кинетика иммунного ответа может быть показателем скорости элиминации вируса у больного.
Идентификация специфичных В-клеток памяти к Spike, RBD и NCP с использованием флюоресцентно окрашенных зондов на IgD– и (или) CD27+ c последующей дифференцировкой по изотипам поверхностных IgM, IgG или IgA показала следующее. Количество специфических В-клеток увеличивалось в течение 120 дней после начала заболевания с последующим выходом на плато, в то время как Spike-специфические В-клетки памяти у людей, не заболевших COVID‑19, практически не встречались. RBD-специфические В-клетки появлялись на 16‑й день, и их количество увеличивалось в течение последующих 4–5 месяцев. Интересно, что только 10–30 % Spike-специфических В-клеток памяти было специфично для домена RBD через 6 месяцев после выздоровления больных.
NCP-специфичные В-клетки памяти также стабильно увеличивались в те же сроки и определялись спустя 5–6 месяцев после заболевания. Представленность изотипов иммуноглобулинов Spike-специфических В-клеток имела следующую динамику. В ранней фазе (20–60 дней) после заболевания IgM+ и IgG+ на В-клетках были представлены одинаково. В период после 60 дней до 240‑х суток преобладали IgG+ Spike-специфические В-клетки. Частота IgА+ Spike-специфических клеток составляла примерно 5 %, и они равномерно распределялись в течение всего периода наблюдения в 8 месяцев. Корреляция между сывороточным IgA и IgA слизистых оболочек не проводилась.
Сходная картина динамики наблюдалась и в случае IgG+, IgM+ и IgА+ к эпитопам RBD и NCP коронавируса. В то же время долгосрочное присутствие циркулирующих В-клеток памяти, направленных как против основных SARS-CoV‑2‑нейтрализующих таргетов (Spike и RBD), так и против не нейтрализующего таргета (NCP), свидетельствует о клеточной памяти, сохраняющейся после естественного воздействия вируса. Это может быть использовано для планирования ревакцинации. Тот факт, что почти все RBD- специфические IgG+-В-клетки памяти экспрессировали CD27, свидетельствует о долгосрочной иммунной памяти.
Анализ полученных данных говорит о том, что снижение нейтрализующих и других антител к SARS-CoV‑2 после клинического выздоровления вовсе мунитета. Просто с развитием и сохра- нением памяти В-клеток, способных активизироваться при встрече с новыми штаммами коронавируса, уровень антител в сыворотке снижается, в то время как IgА-ответ слизистых сохраняется на постоянном уровне в течении всего периода наблюдения.
Клеточный ответ
Процент больных с обнаруживаемыми циркулирующими CD8+-Т-клетками памяти через месяц после возникновения симптомов составил 70 %. К 6–9 месяцам клетки обнаруживались у 50 % выздоровевших пациентов. Фенотипические маркеры показали, что большинство SARS-CoV‑2‑специфичных CD8+-Т-клеток представлены терминально дифференцированными клетками памяти.
Циркулирующие SARS-CoV‑2‑специфичные CD4+-Т-клетки памяти через месяц после начала заболевания обнаруживались у 93 % пациентов. Через 6–9 месяцев уровень этих клеток был стабильным, а сами они выявлялись у более чем у 90 % пациентов, перенесших COVID‑19. Причем это касалось как Spike-специфичных, так и мембраноспецифичных CD4+-Т-клеток памяти.
Интересно, что при сравнении параметров иммунного ответа у больных с тяжелым и легким течением инфекции гуморальные показатели были более высокими у тяжелых больных, в то время как CD8+-Т-клетки были стабильными, а CD4+ — более низкими в тяжелых случаях заболевания. Объяснений этому феномену нет, важно, что слабый ответ Т-клеток наблюдается в острой фазе заболевания. Кроме того, важна и методология исследования клеточного им-мунитета.
Нарушения клеточного ответа проиллюстрированы дефицитом интерферонов I и II типов у пациентов с тяжелыми и среднетяжелыми формами COVID‑19 по сравнению с легкими и бессимптомными случаями заболевания. Это может быть связано с подавлением воспаления интерлейкином‑12 (IL‑12) и развитием вторичного дефекта клеточного иммунитета.
Иммунное взаимодействие
Большой интерес представляет изучение взаимодействия гуморального и клеточного ответа на SARS-Cov‑2. В исследованиях RBD-IgG, Spike IgА, RBD-В-клеток памяти, CD8+- и CD4+-Т-клеток в динамике у одних и тех же пациентов установлено, что у большинства из них (64 %) положительные показатели отмечались через 1–2 месяц после начала заболевания. Через 5–8 месяцев число реконвалесцентов, позитивных на пять тестов, снизилось до 43 %. В то же время как минимум три из пяти тестов были положительными спустя 6–9 месяцев. Важно отметить, что IgG на Spike дает на порядок больше положительных ответов, чем на RBD-антиген. Попытки связать гуморально- клеточные взаимодействия не привели к успеху из-за неоднородности участников исследования и методик оценки иммунного ответа.
Неопределенный результат
В метаанализе 22 исследований (4969 пациентов) установлены неблагоприятные признаки тяжелых форм болезни и летальных исходов, такие как лимфопения и нейтрофилез. Поскольку CD4+-Т-клетки необходимы для сбалансированного и эффективного иммунного ответа, неудивительно, что низкий уровень лимфоцитов может отражать гипервоспалительные процессы и способствовать более тяжелому течению заболевания и повышенной смертности.
Нейтрофилы как неотъемлемая часть врожденной защиты контролируют баланс микробиоты и элиминацию продуктов клеточной деструкции за счет производства активных форм кислорода и высвобождения нейтрофильных внеклеточных ловушек в венозном кровотоке. Лимфопения (менее 500 клеток в 1 мкл) указывает на повышение риска тяжелой формы заболевания и смертельных исходов при COVID‑19 в 3 раза. Стойкий нейтрофилез со сдвигом влево свидетельствует об истощении костномозгового резерва, а при сдвиге вправо отражает нарушения выхода клеток в ткани. Этот легко контролируемый анализом крови параметр указывает на более чем семикратное увеличение для пациента риска заболеть тяжело и погибнуть от COVID‑19.
Попытки выявить закономерности иммунного ответа на SARS-CoV‑2 оказались пока безуспешными.
Во-первых, можно сделать вывод, что переболевшие коронавирусной инфекцией сохраняют иммунную память в последующие 6–9 месяцев. Дальнейшие динамические исследования покажут, в какие сроки наступает снижение иммунного ответа, требующее профилактической вакцинации и (или) ревакцинации.
Во-вторых, и это очень интересно, каждый изученный компонент иммунного ответа и иммунной памяти демонстрирует различную кинетику. Это связано с индивидуальным ответом на инфекцию, наличием преморбида и частого превращения моноинфекции в смешанные инфекции SARS-CoV‑2 с активизировавшейся микробиотой больного.
В-третьих, неоднородность ответа может быть центральным признаком, характеризующим иммунную память к SARSCoV‑2. Биологические специфические IgG имеют 21 день периода полураспада, уровень антител с течением времени отражает продукцию короткоживущих, а потом и долгоживущих плазматических клеток. С точки зрения исчезновения возбудителя в течение нескольких дней после появления клиники, процесс наработки антител должен быть снижен к 6 месяцам, но, если SARS-CoV‑2 Spike и RBD IgG сохраняются дольше 8 месяцев, это означает, что вирус персистирует в организме хозяина или его микробиоте. Нельзя исключать и связь с пролонгированным иммунным ответом естественной реиммунизации циркулирующими эпидемическими альфа-коронавирусами, поддерживающими иммунный ответ.
В-четвертых, выявление и анализ SARSCoV‑2‑специфических В-клеток памяти потенциально могут применяться в качестве маркера гуморального ответа при вакцинации. Сейчас исследования поствакцинального иммунного ответа проводятся с использованием иммунофлуоресцентного анализа с оценкой IgM- и IgG-антител в качестве маркеров эффективности вакцины (рис. 3). Методы ИФА-диагностики, к сожалению, не стандартизованы едиными белками S, RBD, NCP, качество которых зависит от очистки антигена. Поскольку количество В-клеток памяти стабильно с течением времени, они могут представлять собой более надежный маркер продолжительности гуморальных иммунных реакций, чем иммуноглобулины сыворотки крови.
Таким образом, из результатов исследований иммунного ответа у больных COVID‑19 невозможно сделать какие-либо выводы о защитном иммунитете при новой коронавирусной инфекции. Ведь изучение антител и клеток памяти при этом заболевании пока еще не завершено. А значит, обсуждаемые механизмы защитного иммунитета против SARS-CoV‑2 у людей окончательно не определены.
Источник: Газета «Педиатрия сегодня» №6, 2021
