днк полиморфизм что это
Днк полиморфизм что это
Огромное количество информации о последовательности ДНК, полученное в результате работы над проектом «Геном человека» от многих сотен индивидуумов во всех странах, предоставило возможность предварительно охарактеризовать типы и частоты полиморфных изменений в последовательности ДНК человека.
В результате начато формирование каталогов разнообразия последовательности ДНК человека. Полиморфизм ДНК может быть классифицирован по тому, как в разных аллелях изменяется последовательность ДНК.
Однонуклеотидный полиморфизм ДНК
Самый простой и наиболее частый вариант полиморфизма — однонуклеотидный полиморфизм (ОНП). SNP обычно имеет только два аллеля, соответствующих двум основаниям, занимающим конкретную позицию в геноме. SNP встречаются часто, в среднем в каждой 1000 пар оснований, что означает около 3 000 000 различий между любыми двумя геномами человека.
Общее число варьирующих локусов среди всех людей значительно больше и оценивается числом более 10 000 000, хотя и эта оценка, вероятно, занижена, поскольку пока еще нет полного каталога всех, особенно редких, вариантов в каждой этнический группе по всему земному шару. В популяциях разных стран уже каталогизировано много миллионов SNP.
Приблизительно 10% наиболее частых SNP отобрано в качестве маркеров для высокоточной карты генома человека, известной как карта гаплотипов (НарМар — haplotype map).
Значение огромного количества полиморфных SNP для здоровья — предмет активного исследования. То, что SNP бывают так часто, не означает, что они должны оказаться нейтральными и не оказывать влияния на здоровье или длительность жизни. Это может значить, что влияние частых SNP скорее слегка изменяет восприимчивость к болезни, чем прямо вызывает тяжелые недуги.
Полиморфизм инсерций-делеций ДНК
Следующий класс полиморфизма — результат изменений, вызываемых инсерцией или делецией от 2 до 100 нуклеотидов (инделов). Число инделов измеряется в геноме сотнями тысяч. Приблизительно половина всех инделов называется простыми, поскольку они имеют только два аллеля, т.е. либо присутствие, либо отсутствие включенного или удаленного сегмента; другая половина — мультиаллельная из-за переменного числа сегментов ДНК, повторяющихся тандемно в конкретной позиции. Мультиаллельные инделы подразделяются на микросателлитные и мини-сателлитные полиморфизмы.
Микросателлиты. Микросателлиты — последовательности ДНК, состоящие из блоков длиной в два, три или четыре нуклеотида, например, TGTG. TG, СААСАА. САА или АААТАААТ. АААТ, повторяющихся от одного до нескольких десятков раз. Разные аллели при микросателлитном полиморфизме — результат различающегося числа повторов нуклеотидных блоков, содержащихся в микросателлите, поэтому их часто называют полиморфизмом коротких тандемных повторов или STRP.
Микросателлитный локус часто имеет множество аллелей (числа повторов) в популяции и может быть легко генотипирован определением размера ПЦР-фрагментов, сгенерированных праймерами, фланкирующими микросателлитные повторы. В геноме человека известны десятки тысяч микросателлитных полиморфных локусов.
Мини-сателлиты. Другой класс индел-полиморфизма вызван последовательными инсерциями переменного числа (обычно сотен тысяч) копий последовательности ДНК от 10 до 100 пар оснований, известных как мини-сателлиты. Этот класс полиморфизма имеет множество аллелей, различающихся числом тандемно повторяющихся копий мини-сателлита, так называемое переменное число тандемных повторов (VNTR).
Наиболее информативные маркеры имеют несколько десятков или больше аллелей, так что вероятность для не имеющих родственных отношений людей иметь одинаковые аллели очень мала. Хотя полагают, что большинство инделов, независимо от того, простые, они, STRP или VNTR, не имеют никакого значения для здоровья, некоторые VNTR вовлечены в развитие болезней.
Мини-сателлитные последовательности повторов, обнаруживаемые в большинстве случаев полиморфизма типа VNTR, достаточно сходны друг с другом, что делает возможным обнаружение многих локусов одновременно при использовании одного мини-сателлитного фрагмента как зонда в одном анализе блот-гибридизации по Саузерну.
Только идентичные близнецы показывают неразличимые анализы, поэтому одновременное обнаружение полиморфизма множества мини-сателлитов было одним из первых методов ДНК типирования, использованных для установления идентичности образцов. Обнаружение полиморфизма мини-сателлитов блоттингом по Саузерну в основном заменено типированием микросателлитов с помощью ПЦР. Например, Федеральное бюро расследований в Соединенных Штатах к настоящему времени использует 13 STRP-маркеров для панели типирования ДНК. Два человека (кроме монозиготных близнецов) с настолько малой вероятностью могут иметь идентичные генотипы по всем 13 локусам, что панель позволяет точно определить, происходят ли два образца от одного и того же человека.
Полиморфизм числа копий ДНК
Последняя, совсем недавно открытая форма полиморфизма у человека — полиморфизм числа копий (CNP). CNP представляет собой изменения в числе копий больших сегментов генома, в диапазоне от 200 пар оснований до почти 2 миллионов пар. CNP могут иметь только два аллеля (т.е. присутствие или отсутствие сегмента) или многочисленные аллели из-за присутствия 0,1, 2, или 3 или больше копий сегмента ДНК в тандеме. CNP выявлены только недавно, поскольку удаленный или повторяющийся участок обычно слишком мал, чтобы быть видимым при цитогенетическом исследовании, но слишком велик для обнаружения секвенированием ДНК.
Однако CNP легко обнаруживается при применении новой технологии — сравнительной матричной (чиповой) гибридизации генома. Как и для всего полиморфизма ДНК, влияние различных аллелей CNP на здоровье и восприимчивость к болезням в основном неизвестно, но интенсивно исследуется. CNP составляет основу общей изменчивости, которая окажется понятной, если будут правильно интерпретированы изменения в количестве копий, наблюдаемом у пациентов.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Генетика: основные понятия и диагностика
Специализация: генетика, гинекология
Основные понятия
Геном – совокупность наследственного материала, заключенного в клетке организма [1]. Геном содержит биологическую информацию, необходимую для построения организма и поддержания его функций.
Первоначальный смысл этого термина указывал на то, что понятие генома, в отличие от генотипа, является генетической характеристикой вида в целом, а не отдельной особи. С развитием молекулярной генетики значение данного термина изменилось, и сегодня под «геномом» понимают совокупность наследственного материала конкретного представителя вида.
Большинство геномов, в том числе геномы человека и геномы всех остальных клеточных форм жизни, построены из ДНК*. Практически у всех эукариотических организмов все гены организованы в более крупные макромолекулярные комплексы – хромосомы.
У человека наследственный материал соматической клетки представлен 23 парами хромосом (22 пары аутосом и пара половых хромосом), находящихся в ядре, а также клетка обладает множеством копий митохондриальной ДНК. 22 аутосомы, половые хромосомы Х и Y, митохондриальная ДНК человека содержат вместе примерно 3,1 млрд пар оснований [1].
В настоящее время в молекулярной биологии установлено, что гены – это участки ДНК, несущие какую-либо целостную информацию о строении одной молекулы белка или одной молекулы РНК. Эти и другие функциональные молекулы определяют развитие, рост и функционирование организма.
Изначально термин «ген» появился как теоретическая дискретная единица передачи наследственной информации. История биологии помнит споры о том, какие молекулы могут являться носителями наследственной информации. Большинство исследователей считали, что такими носителями могут быть только белки, так как их строение из 20 аминокислот позволяет создать больше вариантов, чем ДНК, состоящая всего из четырех видов
нуклеотидов. Позже было экспериментально доказано, что именно ДНК включает в себя наследственную информацию, что было выражено в виде центральной догмы молекулярной биологии.
Мономеры, составляющие каждую из цепей ДНК, представляют собой сложные органические соединения, включающие в себя азотистые основания: аденин (А), тимин (Т), цитозин (Ц), гуанин (Г), пятиатомный сахар (пентозу) – дезоксирибозу, а также остаток фосфорной кислоты. Эти соединения носят название нуклеотидов (Рис. 1).
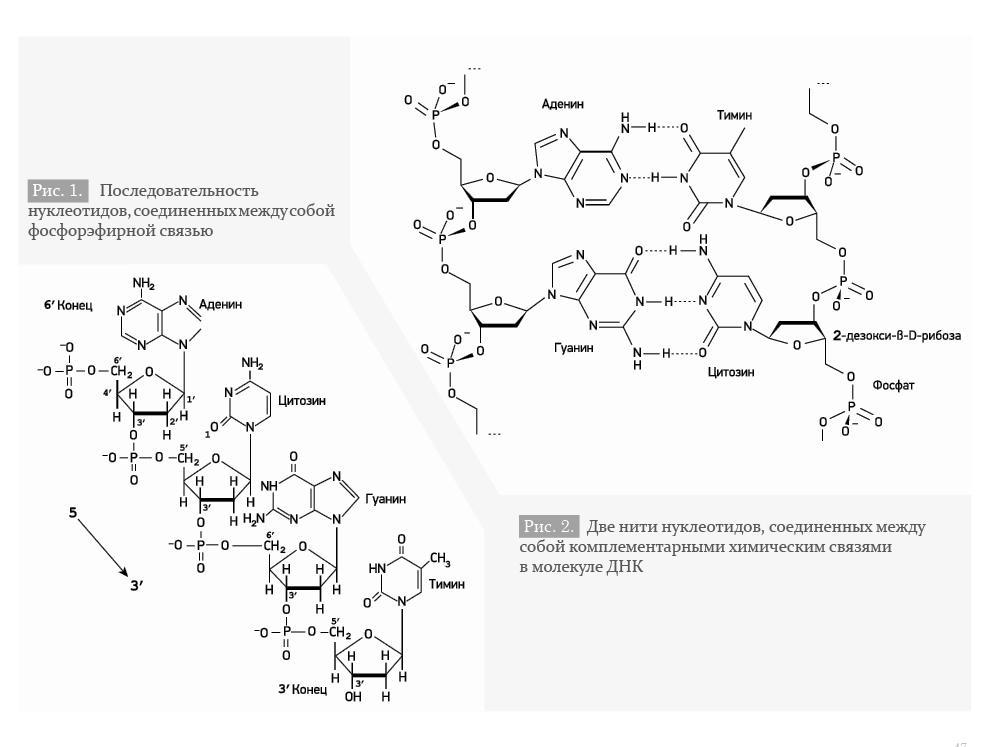
Гены могут подвергаться мутациям – случайным или целенаправленным изменениям последовательности нуклеотидов в цепи ДНК. Мутации могут приводить к изменению последовательности, а следовательно, изменению биологических характеристик белка или РНК, что, в свою очередь, может привести к их общему или локальному изменению или аномальному функционированию. Такие мутации являются патогенными, так как их результатом является заболевание, или летальными на эмбриональном уровне. Однако далеко не все изменения последовательности нуклеотидов приводят к изменению структуры белка или к существенному изменению последовательности и не являются патогенными. В частности, геном человека характеризуется такими особенностями, как однонуклеотидные полиморфизмы и вариации числа копий генов (англ. copynumbervariations), которые составляют около 1% всей ДНК человека [2].
Однонуклеотидный полиморфизм (Single nucleotide polymorphism, SNP) – отличие последовательности ДНК размером в один нуклеотид. Если две последовательности ДНК – AAGCCTA и AAGCTTA – отличаются на один нуклеотид, в таком случае говорят о существовании двух аллелей: C и T. SNP возникают в результате точечных мутаций (как правило, типа замен) и, в частности, определяют различные аллели одного гена.
Разнообразием последовательностей ДНК у людей, возможно, объясняется то, как у них происходит течение различных заболеваний, реакции в ответ на патогены, прием лекарств, вакцин и т. п. Знание об однонуклеотидном полиморфизме, вероятно, поможет в понимании фармакокинетики и фармакодинамики действия различных лекарств на человека. Этиология широкого спектра заболеваний, таких как рак, инфекционные, аутоиммунные заболевания, серповидноклеточная анемия и многие другие, включает однонуклеотидные полиморфизмы [3].
Полиморфизмы генов
Именно полиморфизмы генов в большой степени определяют индивидуальные различия в развитии тех или иных физических и психических качеств индивидума. Масштабы полиморфизмов генов у человека таковы, что между последовательностями ДНК двух людей существуют миллионы различий. Эти различия условно подразделяют на четыре основные категории: а) фенотипически не выраженные; б) вызывающие фенотипические различия; в) играющие роль в патогенезе заболевания (при полигенных болезнях); г) играющие основную роль в развитии заболевания (при моногенных болезнях).
На сегодняшний день сформированы обширные базы полиморфизмов, очень гибкие и быстро растущие.
Они постоянно обновляются за счет информации, которую поставляют в клиники и лаборатории по всему миру научные организации, в которых работает множество специалистов в области системной и молекулярной биологии, биоинформатики.
Вариантные формы некоторых генов в определенных условиях могут привести к развитию болезней. Сочетания вариантных генов предрасположенности несут в себе генетические риски множества заболеваний. Тестирование генетических предрасположенностей помогает выявить индивидуальный риск возможности заболевания и установить подверженность влиянию и воздействию негативных факторов окружающей среды.
По клиническим группам полиморфизмов различают патологии систем свертывания крови, обмена фолиевой кислоты, обмена белков костной ткани, гормонов щитовидной железы, стероидных гормонов и еще десятки других групп полиморфизмов.
В настоящее время в лаборатории CL определяются генетические полиморфизмы генов системы свертывания крови: ген F2 (20210_G>A), ген F5 (1691_G>A), ген F7 (10976_G>A), ген F13 (103_G>Т), ген FGB (455_G>A), ген ITGA 2/интегрин α-2/(807_С>Т), ген ITGВ 3/интегрин β-3/ (1565_Т>С), ген PAI-1 (675_5G>4G). Результат исследования содержит интерпретацию и описание рисков, связанных с тем или иным сочетанием. В ближайшее время планируется значительное расширение спектра определяемых полиморфизмов в CL.
Детекция результатов ПЦР проходит в режиме реального времени. Управление прибором осуществляет программное обеспечение. Программа позволяет использовать простое и интуитивное управление с использованием функции «Тест», что значительно сокращает время создания протоколов исследований. Программное обеспечение содержит приложения для количественной оценки ДНК/кДНК, анализа кривых, определения уровня экспрессии генов, исследования биоценозов и SNP-анализа, позволяет использовать функцию «дополнительных стандартов» и формировать протоколы исследования с автоматической трактовкой полученных результатов.
Научно-технический прогресс привел к одному незаменимому открытию в области молекулярной биологии – открытию метода полимеразной цепной реакции (ПЦР), который позволяет обнаружить даже небольшой фрагмент искомого генома. Полимеразная цепная реакция поначалу применялась исключительно в научных лабораториях. Однако вскоре метод нашел свое место в медицине. В 1993 году, Kary Mullis, ученому, открывшему метод ПЦР, была присуждена Нобелевская премия в области химии.
Диагностика полиморфизмов генов в медицинской лаборатории CL
Выявлять полиморфизмы сегодня позволяют методы современной молекулярно-генетической диагностики. В лаборатории CL исследования полиморфизмов проводят с 2012 года методом полимеразной цепной реакции (ПЦР), c помощью детектирующего амплификатора DtPrime производства российской компании «ДНК-Технология». Принцип ПЦР построен на методе многократного комплементарного достраивания матрицы нуклеиновой кислоты до двухцепочечной структуры, которую способен «увидеть» прибор и распознать полиморфизм. Метод ПЦР, помимо быстроты выполнения и манипулятивной простоты, является еще и весьма чувствительным и специфичным. Очень наглядно принцип метода охарактеризован в среде лабораторных работников так: «найти иглу в стоге сена, а затем построить стог из этих игл».
Для того чтобы исключить неточности, один и тот же участок гена исследуется многократно. Вся цепь ДНК разбивается на участки, затем ведется поиск участков, где прогнозируются полиморфизмы. После чего эти участки вырезаются и сопоставляются. С помощью ПЦР количество таких участков увеличивается до 10 в 36–40 степени. Каждый участок вновь прочитывается десятки раз. Только после этого можно выстроить статистически верную кривую.
Результаты и интерпретация
Информация о наличии полиморфизмов, знание их влияния на определенные виды обмена и уровень чувствительности к лекарственным препаратам позволяют оценить риск развития заболевания, предупредить его развитие и назначить верное лечение.
Важным фактом является то, что генные полиморфизмы в течение жизни не меняются и определяются один раз! Результаты не изменяются в течение жизни и не зависят от физиологического состояния организма.
Генетическое тестирование позволяет в досимптомный период выявить существующие пока только в геноме наследственные тенденции к развитию болезней и наметить пути их ранней профилактики.
Для врачей важна интерпретация результатов анализа полиморфизмов: необходимо понять, как связан тот или иной полиморфизм с вероятностью развития патологического состояния. Следует учитывать, что ни один полиморфизм не является нозологией как таковой, только ее элементом, но зачастую решающим.
Наличие полиморфизмов можно учесть при назначении лекарственных средств. Так, врач-клиницист, руководствуясь рекомендациями генетика, может изменить концентрацию или дозу препарата, который будет влиять на компонент свертывания крови. Безусловно, важны также режим, диета, физиопроцедуры, но основная роль отведена медикаментозному лечению. А это – область фармакогенетики, которая изучает реакции организма на определенные препараты согласно особенностям генома человека.
Интеграция наук
15 лет назад было заявлено, что расшифрован геном человека. Это открытие стало возможным благодаря многолетней работе ученых различных отраслей науки, уровень которой достиг тех высот, в которых информация и знания из одной области проникают в другую. Такая «интеграция наук» выводит на качественно новый уровень дальнейшее развитие биотехнологий, медицины, генетики, геномики. Каких горизонтов достигнут ученые при детальном знании генома человека, прогнозировать трудно. Можно быть готовым лишь к тому, что природа поставит перед человеком новые, не менее сложные задачи и амбициозные цели.
Днк полиморфизм что это
Большинство оценок частоты мутаций использует обнаружение патологических мутаций с явным влиянием на фенотип. Тем не менее существует масса непатогенных мутаций, считающихся относительно нейтральными; а некоторые могут даже быть полезными. В ходе эволюции устойчивый приток новых изменений нуклеотидов гарантировал высокую степень генетического разнообразия и индивидуальности.
Это распространяется на все области генетики человека и медицинской генетики. Генетическое разнообразие может проявляться в виде изменений в окраске хромосом, изменения числа копий сегментов ДНК, нуклеотидных замен в ДНК, изменений в белках или же как болезнь.
ДНК последовательности каждого участка хромосомы в высшей степени сходны у большинства людей в мире. Фактически произвольно выбранный сегмент ДНК человека размером около 1000 пар оснований содержит, в среднем, только одну пару, отличающуюся на двух гомологичных хромосомах, унаследованных от родителей (если предположить, что родители не родственники).
Эта почти в 2,5 раза больше, чем оценка доли гетерозиготных нуклеотидов для кодирующих белок областей генома (примерно 1 на 2500 пар оснований). Различие неудивительное, поскольку интуитивно понятно, что регионы, кодирующие белок, находятся под более жестким давлением отбора, и таким образом встречаемость мутаций в таких регионах в эволюции должна быть более низкой.
Когда вариант встречается настолько часто, что его обнаруживают более чем в 1% хромосом в общей популяции, его называют генетическим полиморфизмом. Аллели с частотами менее чем 1% принято называть редкими вариантами. Хотя много патологических мутаций, приводящих к генетическим болезням — редкие варианты, нет простой корреляции между частотой аллеля и его влиянием на здоровье. Много редких вариантов не имеют патогенных эффектов, тогда как некоторые варианты, достаточно частые, чтобы считаться полиморфизмами, предрасполагают к тяжелым болезням.
Существует много типов полиморфизма. Некоторые полиморфизмы — следствие вариантов, вызванных делециями, дупликациями, утроениями и так далее, сотен миллионов пар оснований ДНК, и не связаны с каким-либо известным патологическим фенотипом; другие изменения аналогичного размера оказываются редкими вариантами, явно вызывающими тяжелые болезни. Полиморфизмами могут оказаться изменения в одном или нескольких основаниях ДНК, расположенных между генами или в интронах, не связанные с функционированием генов и обнаруживаемые только прямым анализом ДНК.
Изменения последовательности нуклеотидов могут располагаться в кодирующей последовательности самого гена и приводить к образованию различных вариантов белков, в свою очередь вызывающих четко очерченные фенотипы. Изменения в регуляторных областях также могут быть важными в определении фенотипа, влияя на транскрипцию или стабильность мРНК.
Полиморфизм — ключевой элемент в исследовании и практическом использовании генетики человека. Способность различать унаследованные формы генов или других сегментов генома обеспечивают инструментальные средства, необходимые для широкого спектра приложений. Как показано в этой и последующих главах, генетические маркеры — мощное научно-исследовательское инструментальное средство картирования генов на конкретном регионе хромосомы при анализе сцепления или аллельной ассоциации.
Они уже широко используются в медицине — от пренатальной диагностики наследственных болезней до обнаружения гетерозиготного носительства, а также в банках крови и тканей для типиро-вания перед переливаниями и пересадками органов (см. далее в этой главе).
Полиморфизм — основа для развивающихся мероприятий по обеспечению основанной на геномике персонализированной медицины, когда медицинские мероприятия индивидуально подбирают на основе анализа полиморфных вариантов, увеличивающих или уменьшающих риск частых болезней взрослого возраста (например, заболевания коронарных сосудов сердца, опухолей и сахарного диабета), возникновения осложнений после хирургических вмешательств или влияющих на эффективность и безопасность конкретного лекарственного препарата. Наконец, анализ полиморфизма стал мощным новым средством в судебных приложениях, например, определении отцовства, определении останков жертв преступления или для сопоставления ДНК подозреваемого и преступника.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Генетический полиморфизм, ассоциированный с риском развития тромбофилии
Тромбофилия (от греч. trhombos – сгусток и philia – склонность) – состояние системы крови, которое проявляется в нарушении гемостаза, склонности к развитию рецидивирующих сосудистых тромбозов (преимущественно венозных) различной локализации и часто возникает в
связи с беременностью, после хирургического вмешательства, травмы или физического пере-
напряжения. Заболевание обусловлено генетической (у 30–50 % с тромботическим состоянием) или приобретенной патологией клеток крови, а также дефектами свертывающей системы крови. При этом тромбофилия еще не тромбоз, но при этом наблюдается готовность организма к тромбообразованию.
Генетическая предрасположенность к тромбофилии может реализоваться через генетические дефекты как свертывающей, так и противосвертывающей (антикоагулянтной и фибринолитической) систем крови, при которых имеется готовность к тромбозу. Тромбозом называют прижизненное образование сгустков крови в просвете сосудов или в полостях сердца.
Тромбозы играют одну из главных ролей в развитии заболеваний сердечно-сосудистой системы, которые стоят на первом месте в инвалидизации и преждевременной смертности жителей экономически развитых стран. На сегодняшний день доля этих заболеваний в структуре смертности составляет 40–60 % (примерно 14 миллионов смертей ежегодно). При этом продолжающийся рост заболеваемости и поражение людей все более молодого возраста делает сердечно-сосудистые заболевания (ССЗ) важнейшей медико-социальной проблемой здравоохранения. Показатели смертности от ССЗ в России в 2–4 раза выше, чем в западноевропейских странах, США, Канаде, Австралии, и в настоящее время наблюдается тенденция к росту смертности. Согласно статистике последних лет, опубликованной на сайте http://www.critical.ru, в структуре смертности от ССЗ в российской популяции 85,5 % приходится на долю ИБС (46,8 %) и мозгового инсульта (38,7 %). Наследственная тромбофилия играет важную роль в структуре акушерских и гинекологических осложнений, таких как потери плода, привычное невынашивание беременности, повторные неудачи при ЭКО, тромбоэмболии у беременных.
Еще одной важной проблемой является назначение оральных контрацептивов. Оральная контрацепция является одним из самых надежных способов предотвращения нежелательной беременности, но сопряжена с риском тромбозов. Показано, что сама по себе гормональная контрацепция незначительно повышает риск тромбозов, но при носительстве определенного генотипа опасность резко возрастает. Согласно Национальным медицинским критериям приемлемости методов контрацепции 2012 года и четвертой редакции «Медицинских критериев приемлемости для использования методов контрацепции», разработанных ВОЗ в 2009 году, для предотвращения тромбозов и тромбоэмболических осложнений при приеме оральных контрацептивов рекомендовано выявление тромбогенных мутаций (F2 – протромбиновая мутация, F5 – фактор Лейдена).
Генетический анализ позволяет выявить полиморфизмы генов факторов системы гемостаза, обусловливающих их аномальный синтез или нарушение функциональной активности. Это помогает оценить риски развития сердечно-сосудистой патологии и акушерско-гинекологических осложнений, тромбоэмболии, венозных и артериальных тромбозов. Скрининг генетических особенностей тромбофилий помогает на раннем этапе выявить группу риска и внести соответствующие коррективы в тактику ведения пациентов.
Показания к назначению профиля «генетика тромбофилии»:
единичный до 50 лет;
в любом возрасте при наличии семейного анамнеза;
необычной локализации (портальные, брыжеечные, мозговые вены);
непонятной этиологии после 50 лет;
массивные хирургические вмешательства;
Полиморфизм гена коагуляционного фактора II(G20210A) (протромбин)
Настоящая мутация наследуется по аутосомно-доминантному типу и в гетерозиготном состоянии встречается у 2,3 % людей в общей популяции. Клинически ее можно заподозрить по постоянно высокому уровню протромбина в плазме крови (у 87% носителей превышает 115%). Риск развития тромбоза у носителей гетерозиготной аномалии повышается в 3 – 5 раз и более значительно при использовании оральных контрацептивов.
Показания к назначению: инфаркт миокарда, гиперпротромбинемия, тромбоэмболические состояния в анамнезе, невынашивание беременности, фетоплацентарная недостаточность, внутриутробная гибель плода и задержка развития плода, отслойка плаценты, перед большими полостными операциями.
Биологический материал для анализа : цельная кровь, стабилизированная ЭДТА
Полиморфизм гена коагуляционного фактора V (акцелератор-глобулин) (Лейден)
Мутация наследуется по аутосомно-доминантному типу. Аллельная частота от 2,9 до 7,8% (в среднем 4,4%). FVL (Лейден) увеличивает риск преимущественно венозного тромбоза у лиц моложе 40 – 45 лет в 3 – 4 раза, особенно на фоне беременности, послеродового периода, длительной иммобилизации, больших хирургических вмешательств и приема оральных контрацептивов.
Показания к назначению: венозный тромбоз, тромбоэмболические заболевания в молодом возрасте, рецидивирующие тромбоэмболии, сердечно-сосудистые заболевания в семейном анамнезе, невынашивание беременности, фетоплацентарная недостаточность, внутриутробная гибель плода и задержка развития плода, отслойка плаценты, перед большими полостными операциями, прием пероральных контрацептивов.
Биологический материал для анализа : цельная кровь, стабилизированная ЭДТА
Полиморфизм гена коагуляционного фактора VII(G10976A) (проконвертин)
Вариант 353Gln (10976A) приводит к понижению производительности (экспрессии) гена фактора VII и является защитным фактором в развитии тромбозов и инфаркта миокарда. Распространенность данного варианта в европейских популяциях составляет 10-20%. При исследовании пациентов со стенозом коронарных артерий и инфарктом миокарда обнаружено, что наличие мутации 10976A приводит к понижению уровня фактора VII в крови на 30% и 2-х кратному понижению риска инфаркта миокарда даже при наличии заметного коронарного атеросклероза.
Показания к назначению: оценка риска инфаркта миокарда и фатального исхода при инфаркте миокарда, тромбоэмболические заболевания в анамнезе.
Биологический материал для анализа : цельная кровь, стабилизированная ЭДТА
Полиморфизм гена коагуляционного фактора XIII(G103T) (фибриназа)
Биологический материал для анализа : цельная кровь, стабилизированная ЭДТА
Полиморфизм гена коагуляционного фактора I(G455A) (фибриноген)
Показания к назначению: повышенный уровень фибриногена плазмы, повышенное кровяное давление, повышенная вероятность тромбообразования, инсульт.
Биологический материал для анализа : цельная кровь, стабилизированная ЭДТА
Полиморфизм гена ингибитора активатора плазминогена PAI-1(5G/675/4G)
Показания к назначению: портальный тромбоз и другие тромбоэмболические состояния в анамнезе, инфаркт миокарда, ИБС, повышение концентрации ингибитора активатора плазминогена в крови, мутация ITGB3, ожирение.
Биологический материал для анализа : цельная кровь, стабилизированная ЭДТА
Полиморфизм гена тромбоцитарного рецептора (интегрина) ITGA2(C807T)
Данный рецептор, влияет на адгезию тромбоцитов на коллагене и других субстратах, а также участвует в реорганизации межклеточного матрикса. Генетические варианты GPIa могут приводить к изменению кинетики адгезии тромбоцитов. Вариант C807T встречается с частотой 5,7% и является маркером кардиоваскулярных заболеваний и артериальным тромбоэмболиям. Исследование 177 пациентов с инфарктом миокарда (средний возраст 57 лет) и 89 здоровых доноров показало значительную разницу в распределении частот вариантов 807C и 807T между двумя группами. Более высокая частота гомозиготного варианта 807T у пациентов соответствовала почти 3-кратному повышению риска инфаркта
Показания к назначению: cемейный анамнез ранней ИБС, инфаркт миокарда, тромбоэмболические состояния в анамнезе, постангиопластические тромбозы, неонатальная тромбоцитопения, антитромботическая терапия аспирином.
Биологический материал для анализа : цельная кровь, стабилизированная ЭДТА
Полиморфизм гена тромбоцитарного рецептора (интегрина) ITGB3(T1565C)
Ген тромбоцитарного рецептора фибриногена (ITGB3) кодирует бета-3 субъединицу интегрин-комплекса поверхностного рецептора тромбоцитов GPIIb/IIIa, известную также как гликопротеин-3а (GPIIIa). ITGB3 участвует в межклеточной адгезии и сигнализации. ITGB3 обеспечивает взаимодействие тромбоцита с фибриногеном плазмы крови, что приводит к быстрой агрегации (склеиванию) тромбоцитов. Мутация 33P GPIIIa способствует повышенной склонности тромбоцитов к агрегации, что увеличивает риск развития сердечно-сосудистых заболеваний. У пациентов с этим вариантом часто отмечается пониженная эффективность аспирина как дезагрегантного препарата. Частота встречаемости мутации 33P в европейских популяциях составляет 8-15%.
Показания к назначению: Семейный анамнез ранней ИБС, инфаркт миокарда, тромбоэмболические состояния в анамнезе, постангиопластические тромбозы, неонатальная тромбоцитопения, антитромбозная терапия аспирином.
Биологический материал для анализа : цельная кровь, стабилизированная ЭДТА

